Clear Sky Science · zh
CCL11 通过增强免疫抑制性的 CCR5+ CD206+ M2 型巨噬细胞并促进肿瘤侵袭性,促进肝细胞癌术后复发
为何肝癌术后会复发
肝脏手术通常是早期肝癌患者最有希望的治疗手段,但许多患者在数年内出现肿瘤复发。本研究提出了一个简单却关键的问题:人体对手术产生的炎性修复反应是否无意中助长了残留癌细胞的生长与扩散?研究者聚焦于一种名为 CCL11 的信号分子,展示了术后该分子激增如何既削弱抗癌免疫,又使残存肿瘤细胞更具侵袭性。
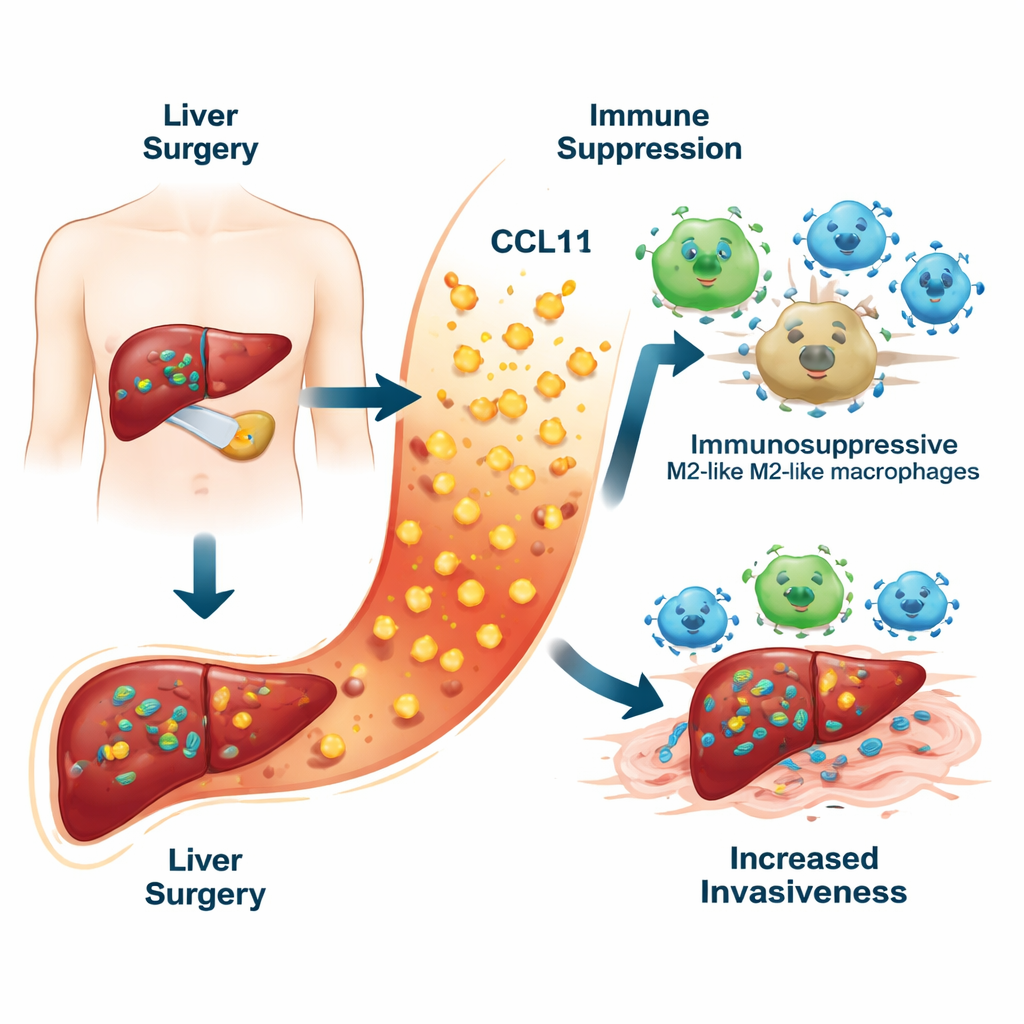
愈合反应中的隐性危险
外科医生切除肝肿瘤时需夹闭血管并损伤周围组织。这些损伤会触发一波有助肝脏愈合的炎症反应。研究团队在术后一周对患者血液中十种不同炎性分子进行测定,发现一种趋化因子 CCL11 显著突出。术后随后复发的患者其 CCL11 水平明显高于无复发者,高 CCL11 水平也与更差的生存率相关。将 CCL11 与常规临床资料(如血液检查和肿瘤特征)结合后,研究者构建了一个风险“记分卡”,其对五年复发的预测优于传统模型。
看似正常的肝组织仍然重要
癌症研究多数聚焦于肿瘤本身,但本研究显示周围“正常”肝组织同样关键。在来自 100 多名患者的样本中,非肿瘤肝组织中的 CCL11 水平实际上高于癌结节或健康供体肝。邻近肝组织产生更多 CCL11 的患者更可能出现晚期疾病、远处转移和术后复发。在模拟手术中短暂缺血再灌注的小鼠模型中,肝脏损伤迅速推动了 CCL11 水平上升。在体外低氧条件下,肝支持细胞如肌成纤维细胞和血管内皮细胞也产生更多 CCL11,提示手术应激使肝残端整体被“抚育”为促癌环境。
CCL11 如何将免疫防御变为旁观者
为探明 CCL11 对免疫的影响,作者聚焦于巨噬细胞——这类多能白细胞既可攻击肿瘤也可保护肿瘤。他们发现,在非肿瘤肝组织中,较高的 CCL11 与更多携带 CCR5 标志并呈现所谓 M2 样、亲肿瘤表型的巨噬细胞共同存在。在患者中,富含这些 CCR5+ M2 样巨噬细胞的肝组织与更差的生存相关。在细胞培养实验中,加入 CCL11 会促使单核细胞分化为这种免疫抑制型巨噬细胞,增加 PD-L1、IL-10 等分子的表达,并释放其他招募并偏向化免疫细胞的信号。这些经 CCL11 调节的巨噬细胞进一步促使初始辅助 T 细胞分化为调节性 T 细胞——一类已知会抑制抗肿瘤反应的细胞。机制性实验表明,CCL11 在巨噬细胞内启动一连串信号,最终激活 NF-κB 通路并促使 PD-L1 产生,从而帮助肿瘤细胞免受免疫攻击。
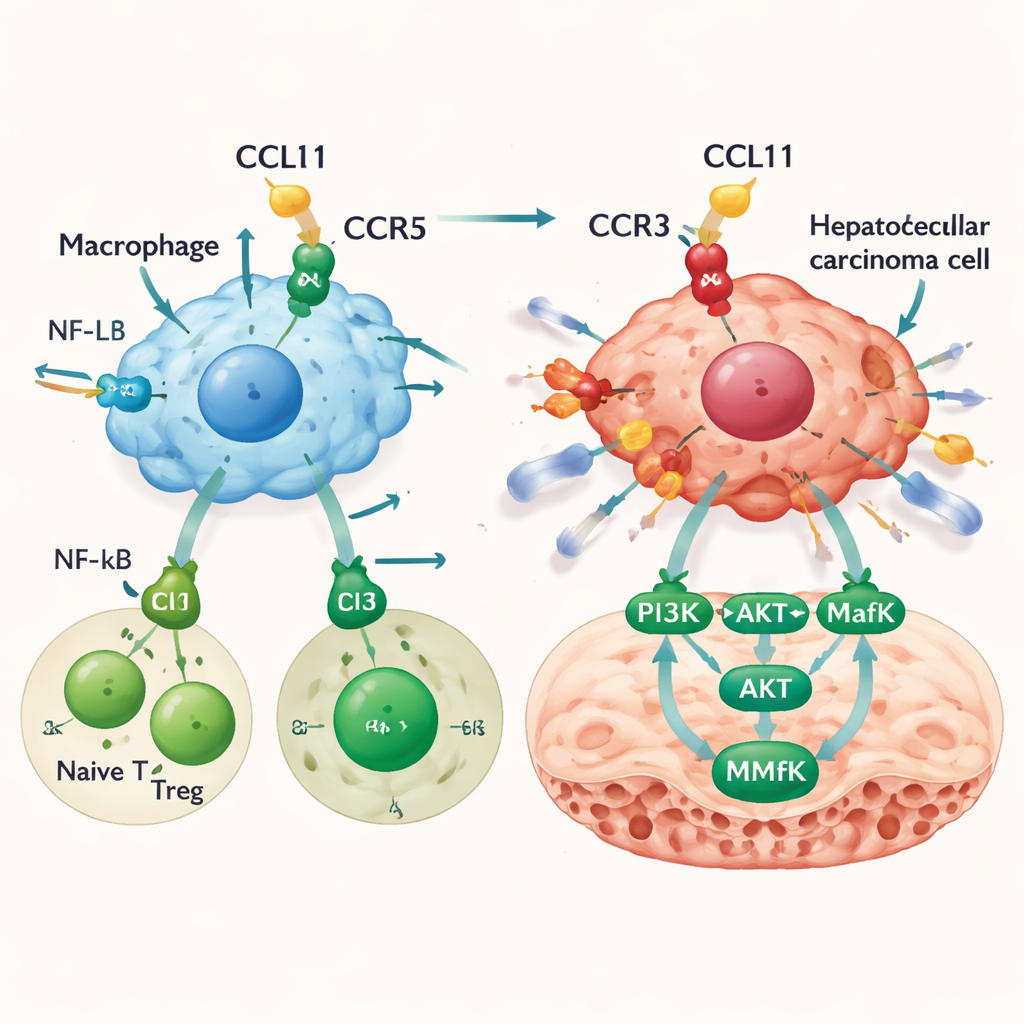
CCL11 如何使残留癌细胞更具侵袭性
CCL11 不仅重塑免疫景观,还直接作用于肝癌细胞。尽管肿瘤细胞本身很少产生 CCL11,但它们表达其中一种受体 CCR3。在体外实验中,CCL11 并未加速肝癌细胞增殖,但确实使其更易迁移并穿过屏障——这是转移潜力的特征。阻断 CCR3 受体可在很大程度上消除这一效应。基因分析指向这样一条通路:CCL11–CCR3 信号激活 PI3K 和 AKT,进而激活转录因子 MafK,MafK 又提升基质金属蛋白酶 MMP13 的产生,MMP13 可分解周围基质并为癌细胞扩散开辟通路。在小鼠模型中,将 CCL11 输注入肝脏会增加肿瘤负荷并导致更多转移,同时肿瘤内 PI3K–AKT–MafK–MMP13 通路水平升高。
将危险信号转为治疗契机
鉴于 CCL11 既能压制免疫防线又能增强残留癌细胞的韧性,研究者测试了术后阻断它是否能改变结局。在行肝肿瘤切除术的小鼠中,使用中和 CCL11 的抗体治疗显著降低了肝内癌症复发率并改善了生存,且未见明显副作用如体重下降。总体而言,这些发现将 CCL11 描绘为将手术损伤与免疫抑制、利于侵袭的肝环境连接起来的关键开关。对患者而言,该研究提示术后检测 CCL11 可帮助识别复发高风险人群,且未来针对 CCL11–CCR5/CCR3 轴的药物或可成为防止肝癌复发的策略之一。
引用: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
关键词: 肝癌复发, CCL11 趋化因子, 肿瘤微环境, 免疫抑制, 癌症转移