Clear Sky Science · zh
癌相关成纤维细胞通过METTL1介导的NET1 m7G修饰促进非小细胞肺癌细胞对奥希替尼的耐药
为何某些肺癌会停止对“靶向”药物产生反应
像奥希替尼这样的靶向药已改变了许多常见类型肺癌患者的治疗,较传统化疗能延长生存并减少副作用。然而对大多数患者而言,这些益处是暂时的:肿瘤最终会想出办法躲过药物。本研究提出了一个看似简单但影响深远的问题:肿瘤的支持性组织——尤其是称为癌相关成纤维细胞的细胞——是否在悄悄帮助癌细胞逃避奥希替尼的作用?
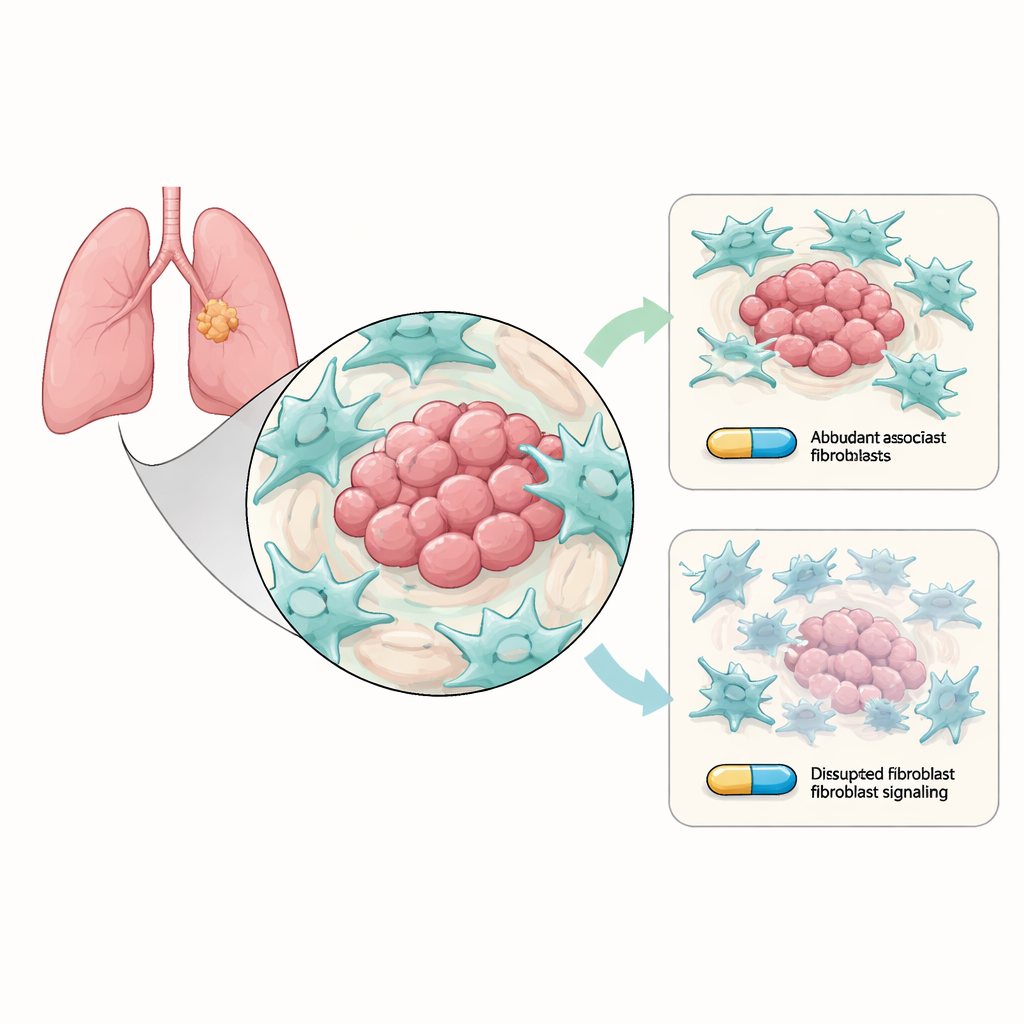
暗中保护肿瘤的“帮手”细胞
非小细胞肺癌在一个由非癌细胞组成的热闹“邻里”中生长,这被称为肿瘤微环境。其中最丰富的居民之一是癌相关成纤维细胞(CAFs),一种重塑肿瘤周围基质的结缔组织细胞。研究人员在体外将携带常见对奥希替尼敏感的EGFR突变的肺癌细胞与CAFs共同培养。他们发现,在有CAFs存在时,癌细胞更难被奥希替尼杀死:它们形成更多克隆,自毁(凋亡)较少,并表现出更强的“干性”特征,这与长期存活和复发相关。换言之,尽管药物仍然作用于癌细胞,周围的成纤维细胞却在默默帮助它们耐受药物。
改变规则的RNA化学标记
研究团队随后将视线从基因本身转向装饰RNA的化学标记——RNA是细胞内基因信息的工作拷贝。其中一种称为m7G的标记可以影响RNA分子的稳定性以及其翻译成蛋白的效率。通过生化检测和全基因组定位,研究者显示CAFs会增加肺癌细胞内RNA的总体m7G标记。这一增加主要由一种甲基转移酶METTL1驱动,METTL1在信使RNA上添加m7G标记。METTL1在肺肿瘤中的水平高于邻近正常组织,并与更晚期疾病和更差的患者生存相关,提示该酶的作用不仅限于微调常规细胞功能。
一种分泌信号与脆弱的分子链
CAFs如何在癌细胞中上调METTL1?研究指向了CAFs分泌到其周围环境中的一种蛋白HMGB1。与癌细胞相比,CAFs分泌的HMGB1量大得多。当研究人员向肺癌细胞添加HMGB1时,METTL1水平和m7G标记上升;当他们在CAFs条件培养基中阻断HMGB1时,这一效应减弱。进一步深入研究,他们确定了METTL1的一个关键RNA靶标:NET1,这个基因有助于驱动细胞生长和迁移。CAFs增加了NET1 RNA和蛋白的m7G修饰及丰度,且METTL1能与NET1 RNA物理结合以使其稳定。减少METTL1会导致NET1的修饰减少、癌细胞生存信号减弱以及对奥希替尼的敏感性增加。
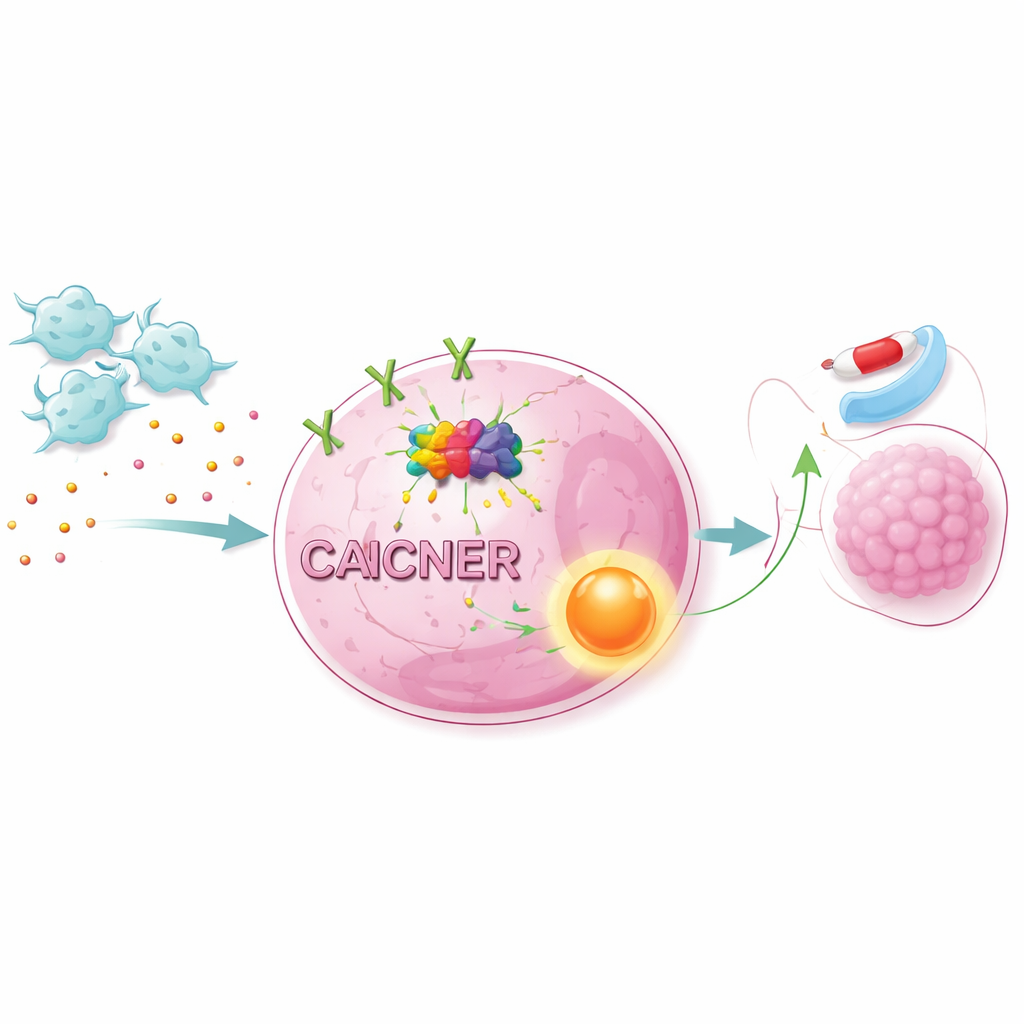
在癌细胞内开启生存通路
增强的NET1信号并非孤立发生。通过结合大规模RNA数据与通路分析,科学家们显示CAFs激活了细胞内一条主要的生长与生存通路,即AKT/NF-κB通路。使用特定抑制剂阻断AKT或NF-κB可使肺癌细胞即便在CAFs存在下也对奥希替尼更为脆弱。改变NET1水平也产生类似效果:降低NET1削弱了CAFs的保护作用,而提高NET1则增强了耐药性。在带有人源肺癌细胞移植的小鼠模型中,加入CAFs使肿瘤生长更快且对奥希替尼反应变差。在癌细胞中敲低METTL1可降低m7G标记、减少NET1及通路激活,并显著抑制由CAFs驱动的肿瘤生长。
这对未来肺癌治疗意味着什么
对于面临EGFR突变肺癌的患者,这项工作提供了一种新的视角,解释为何像奥希替尼这样的强效药物最终会失效。研究并非仅将责任归咎于癌细胞中新出现的突变,而是强调了一条从肿瘤细胞外发起的分子链——CAFs分泌HMGB1,经由METTL1、NET1上的m7G修饰,到激活削弱药物效应的生存通路。理论上,在这一链条的任何一点进行干预都可能恢复或延长对治疗的敏感性。尽管直接靶向METTL1、HMGB1或特定m7G标记RNA的药物仍处于早期阶段,研究表明将奥希替尼与瞄准肿瘤支持细胞或其RNA修饰信号的疗法联合使用,可能有助于更长时间地控制这类肺癌。
引用: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
关键词: 奥希替尼耐药, 非小细胞肺癌, 癌相关成纤维细胞, RNA甲基化, METTL1 NET1通路