Clear Sky Science · zh
ERRα-KDM5C 限制 STING 增强子活性以调节乳腺癌进展中的 I 型干扰素信号
阻止癌细胞伪装
癌细胞不仅仅是不受控制地生长——它们还学会了躲避免疫系统的监视。本研究揭示了某些乳腺癌细胞如何调低一种重要的细胞内警报系统,称为 STING 通路,该通路通常用于向免疫系统发出危险信号。通过理解这一“关闭开关”,科学家希望找到使肿瘤对免疫系统更可见的新方法,并改善包括化疗在内的现有治疗效果。
受压的细胞警报系统
STING 通路像是细胞内的内置安保系统。当检测到 DNA 损伤或类似病毒的信号时,STING 会促使产生 I 型干扰素——这些强效的免疫信使会召集包括杀伤性 T 细胞在内的防御力量。许多肿瘤通过沉默这套警报使自己更容易不被察觉并得以扩增。本文作者聚焦于乳腺癌细胞,提出问题:哪些分子负责抑制 STING 活性?这种控制如何接入细胞的基因“配线板”——即增强子(短小的 DNA 区域,可增强邻近基因活性)?
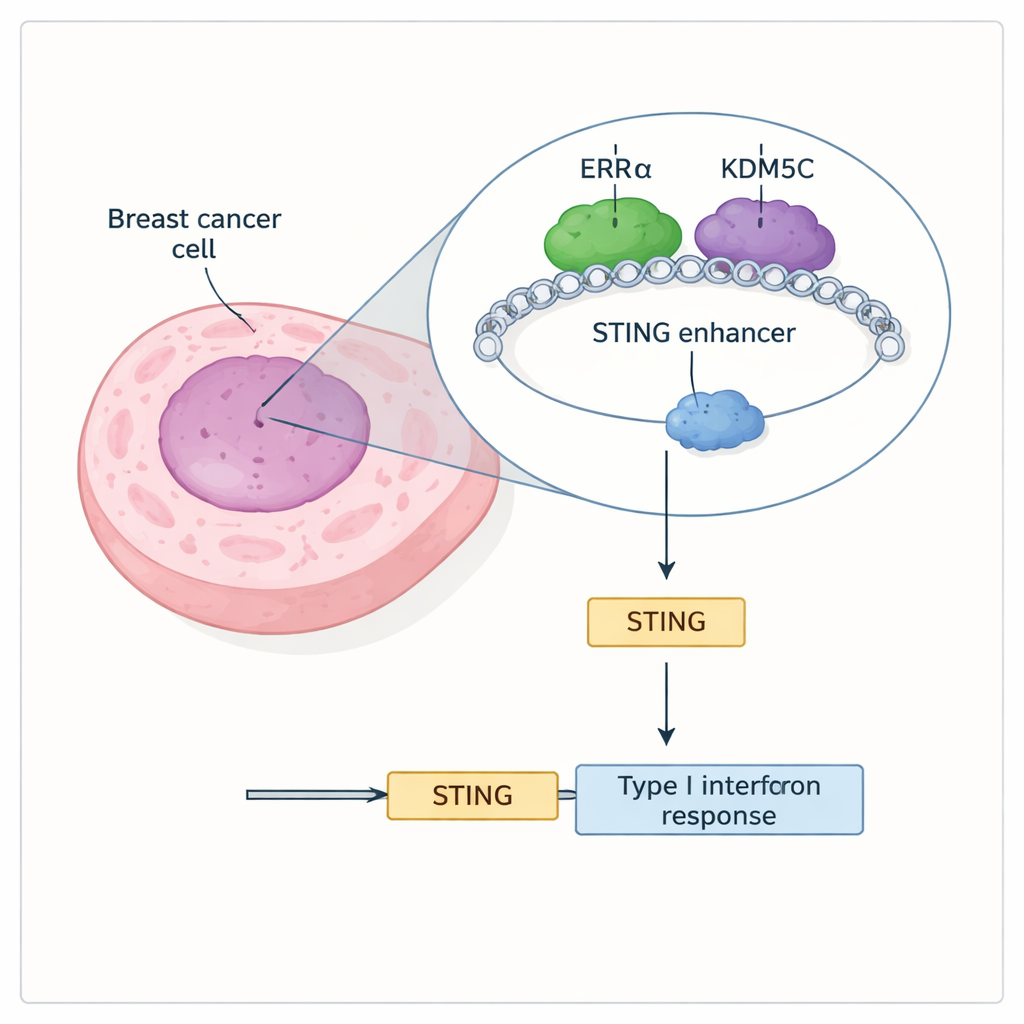
两种蛋白联手压制 STING
研究人员发现,一种名为 ERRα 的核受体和一种名为 KDM5C 的酶在物理上相互作用,并共同定位于许多活跃的增强子区域,包括调控 STING 基因的增强子。ERRα 已知帮助癌细胞重编程代谢并抗拒细胞凋亡,而 KDM5C 是一种“染色质编辑器”,可擦除与强基因激活相关的化学标记(H3K4me3)。通过全基因组结合位点图谱,团队显示 ERRα 和 KDM5C 常共同占据带有高度活性标记并产生增强子 RNA 的位点,这表明这些开关处于开启状态。特别是在 STING 的增强子处,两种蛋白都存在,并且它们的存在与 STING 输出被抑制相伴。
释放免疫信号的刹车
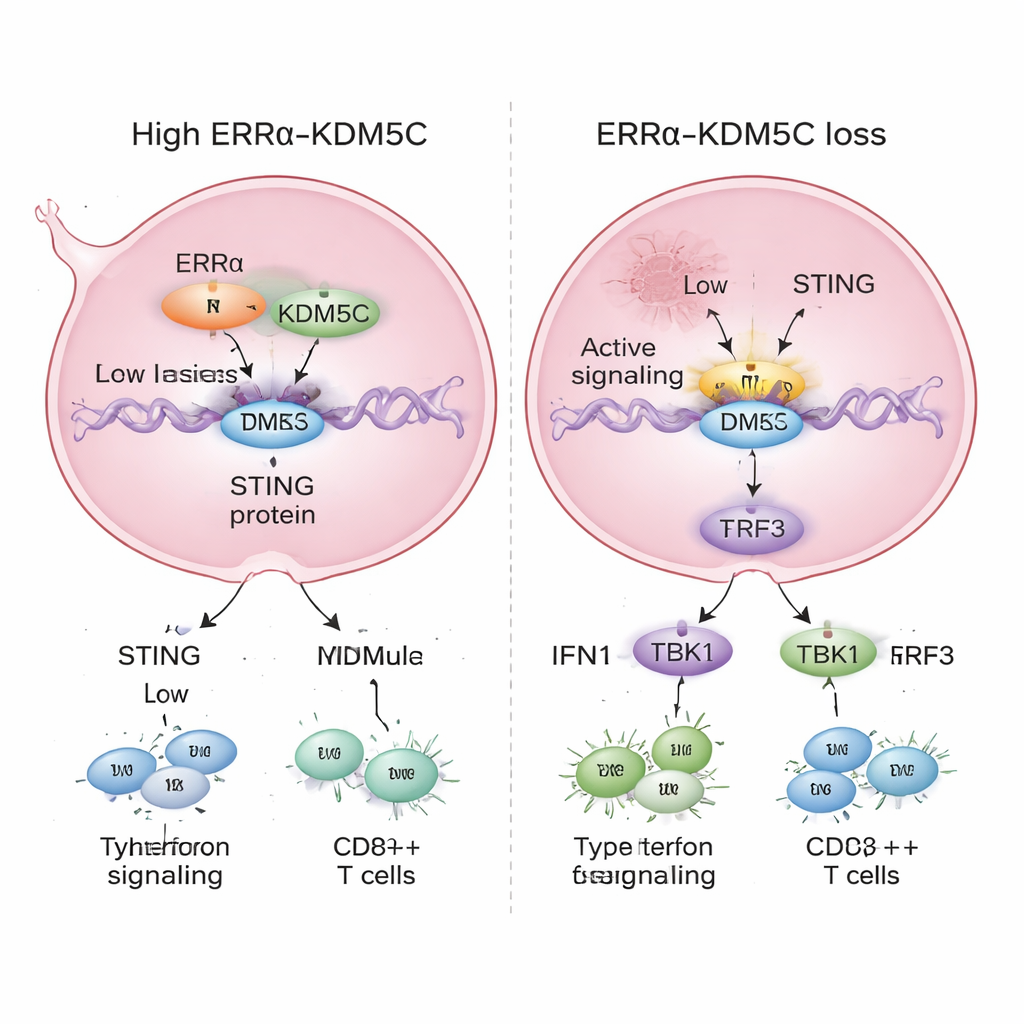
当科学家降低乳腺癌细胞中 ERRα 或 KDM5C 的水平时,STING 增强子变得过度活跃。与强激活相关的化学标记增加,与弱状态相关的标记减少,增强子 RNA 产生增加。随后 STING 基因和蛋白水平上升,其下游通路被更强烈激活,包括驱动 I 型干扰素产生的关键中继蛋白 TBK1 和 IRF3。因此,细胞开始表达更高水平的干扰素及干扰素刺激基因,这些基因是抗病毒防御和抗肿瘤免疫的核心。换言之,去除 ERRα 或 KDM5C 就像把被压制的警报变成了刺耳的警笛。
减缓肿瘤生长并增强疗效
这些分子变化对癌细胞行为产生了明显影响。降低 ERRα 或 KDM5C 的乳腺癌细胞生长更慢,体外形成的克隆更少。在小鼠模型中,来源于 ERRα 缺失细胞的肿瘤更小、更轻,表明其体内生长受抑制。重要的是,当同时沉默 STING 时,这种生长抑制大部分被逆转,表明激活 STING 是 ERRα 和 KDM5C 缺失限制肿瘤的关键机制。团队还测试了导致 DNA 损伤并可激活 STING 的化疗药物依托泊苷(etoposide)。阻断 ERRα 使依托泊苷在缩小肿瘤方面更有效,提示放松这一刹车可通过放大全身免疫刺激信号来增强常规治疗的效果。
对患者意味着什么
通过分析患者数据,研究者发现人类乳腺癌组织中 ERRα 水平高于正常乳腺组织,且高表达与较差的生存率以及肿瘤内较少的抗癌 CD8+ T 细胞相关。综合看来,这项工作勾勒出一幅清晰图景:ERRα 和 KDM5C 形成一个控制模块,使 STING 警报保持沉默,帮助乳腺肿瘤生长并躲避免疫攻击。对于普通读者,关键信息是某些乳腺癌利用这对组合来隐藏自己。靶向 ERRα、KDM5C 或它们对 STING 增强子的结合,可能有助于“揭露”肿瘤、增强免疫反应,并提高现有疗法的效力。
引用: Xu, ZH., Chen, J., He, Y. et al. ERRα-KDM5C restrains STING enhancer activity to modulate type I interferon signaling in breast cancer progression. Cell Death Dis 17, 228 (2026). https://doi.org/10.1038/s41419-026-08499-2
关键词: 乳腺癌, STING 通路, I 型干扰素, 表观遗传调控, 肿瘤免疫