Clear Sky Science · zh
ΔNp63α驱动丝氨酸合成以促进非小细胞肺癌对卡铂的耐药性
为什么剥夺“非必需”营养物质会影响癌细胞
大多数人把癌症治疗想象成直接杀死肿瘤细胞的强效药物。但这项研究表明,癌细胞的“饮食”同样重要。研究人员发现,某些肺癌会重编程其合成和利用氨基酸丝氨酸的方式,从而帮助它们抵抗常用化疗药物卡铂。通过理解并针对这种隐秘的代谢策略,医生未来或许能通过将药物与改变肿瘤获取特定营养的方式相结合,使标准治疗更有效。
滋养顽固肺肿瘤的供给线路
肺癌是全球癌症死亡的主要原因,非小细胞肺癌(NSCLC)约占病例的85%。在NSCLC中,称为肺鳞状细胞癌(LUSC)的亚型相比其他形式可用的靶向治疗要少得多,仍主要依赖以卡铂为基础的化疗。作者聚焦于丝氨酸——一种被癌细胞用作合成DNA、蛋白质和脂质的构件,并是其抗氧化防御的重要组成的氨基酸。尽管人体可以合成丝氨酸,但侵袭性肿瘤似乎同时提高了其生产和摄取,表明它们可能对这种营养物质的生长和存活有异常的依赖。
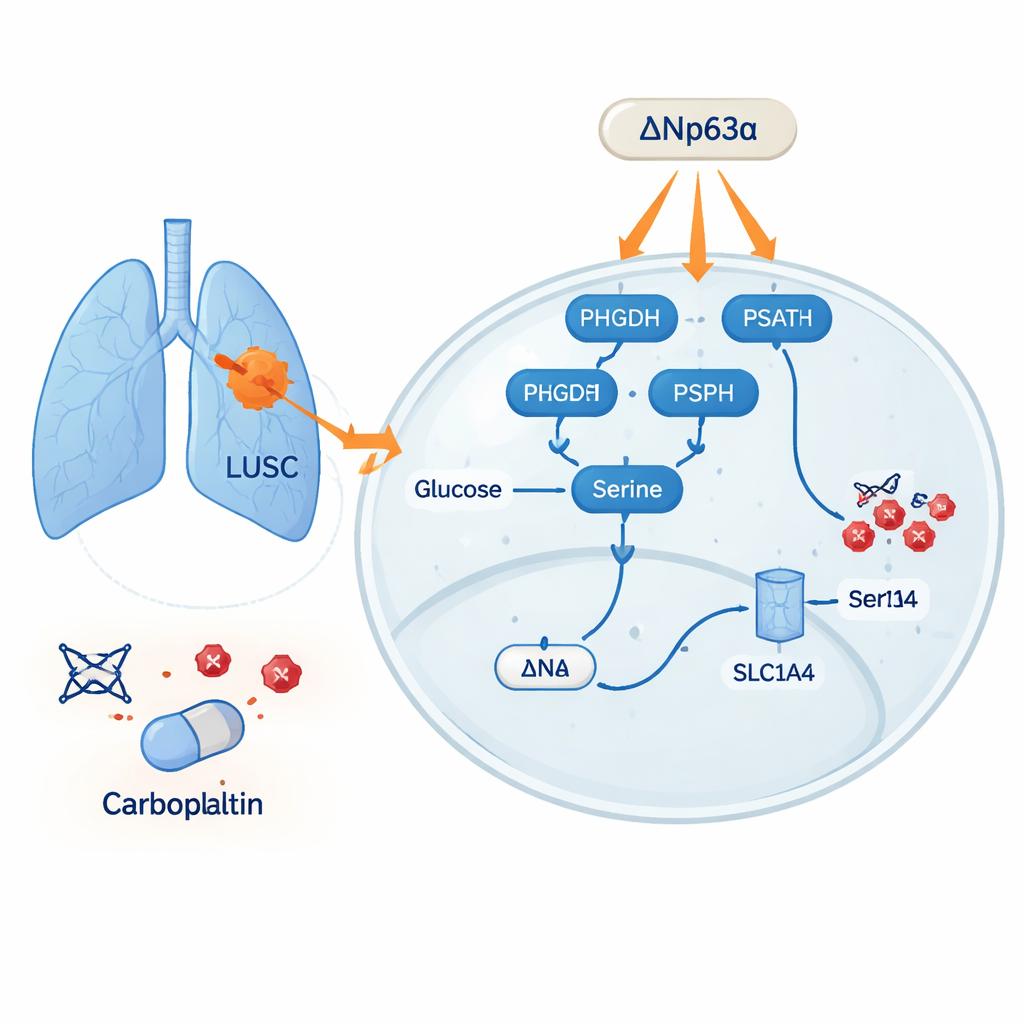
驱动耐药性的代谢通路
通过分析大量患者数据集和肿瘤样本,团队显示了参与丝氨酸合成与摄取的多种蛋白——PHGDH、PSAT1、PSPH 和转运蛋白 SLC1A4——在肺癌中相比正常肺组织持续升高。这些丝氨酸相关基因的高表达与更差的生存率相关。该效应在LUSC中尤为明显,LUSC不仅这些酶含量更高,丝氨酸含量也高于肺腺癌。在细胞培养中,含有更多丝氨酸的癌细胞对卡铂的敏感性较低,额外补充丝氨酸能帮助它们抵御药物的作用。在小鼠实验中,饲喂高丝氨酸饮食的动物体内肿瘤对卡铂产生抵抗,而处于低丝氨酸饮食的老鼠在相同治疗下肿瘤缩小更多。
将丝氨酸生产开到最高的谱系基因
研究人员接着探究为何LUSC细胞如此擅长合成丝氨酸。他们把注意力集中在ΔNp63α上,这是一种在鳞状癌中作为“谱系”调控因子的蛋白,常用于LUSC的诊断。通过挖掘公开基因表达数据并进行分子实验,他们发现ΔNp63α高表达的肿瘤也同时显示出四个关键丝氨酸通路基因的高表达。在细胞系中,提升ΔNp63α会增加细胞内丝氨酸含量,而降低ΔNp63α则会减少。进一步的测试显示,ΔNp63α直接与这些丝氨酸通路基因的调控区结合并开启它们,充当一个主控开关,在鳞状肺癌细胞中提升丝氨酸的合成与摄取。
额外的丝氨酸如何保护癌细胞免受化疗
卡铂主要通过损伤DNA并增加称为活性氧(ROS)的有害氧基分子来杀死癌细胞。丝氨酸通过两种关键方式帮助细胞:它为合成DNA的构件提供原料,并为谷胱甘肽的生成提供原料——谷胱甘肽是清除ROS的主要抗氧化剂。当科学家从细胞培养基中去除丝氨酸及其近亲甘氨酸时,卡铂会导致更多的DNA断裂和显著升高的ROS水平。补回甲酸(丝氨酸用于DNA合成的产物)或抗氧化剂可以部分挽救细胞,同时两者合用几乎恢复了细胞存活。在那些本来就大量合成丝氨酸的鳞状肺癌细胞中,用药物(NCT‑503)抑制酶PHGDH能显著增强卡铂的疗效,既在细胞培养中如此,在小鼠肿瘤模型中也如此。
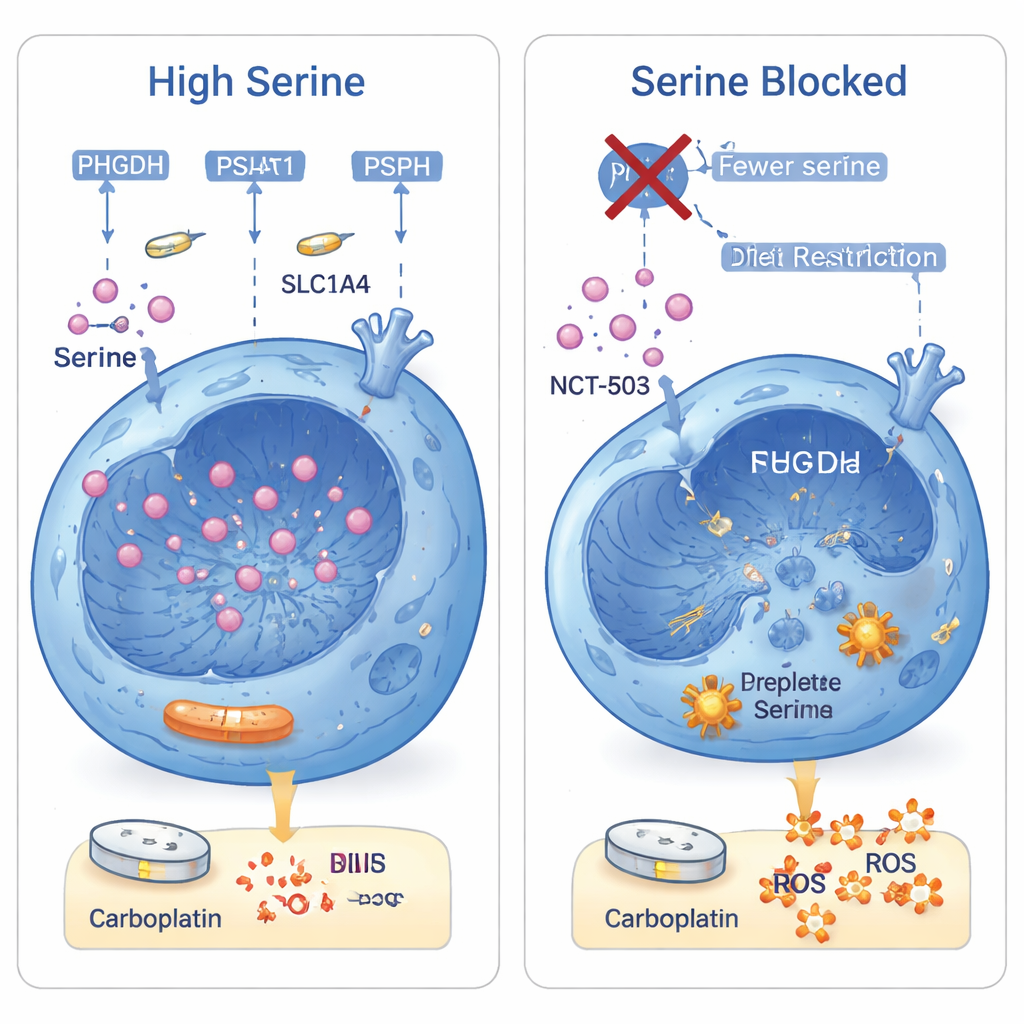
将弱点变为治疗机会
对普通读者来说,关键的信息是:一些鳞状肺癌通过过度合成单一氨基酸丝氨酸(受ΔNp63α基因控制)来幸存于化疗。这额外的丝氨酸使肿瘤细胞能够修复卡铂诱导的DNA损伤并中和否则会杀死它们的有毒分子。研究表明,如果同时切断内部的“工厂”——丝氨酸合成通路——和外部的“补给线”——饮食供给,卡铂的效果会大幅提升。换言之,通过将标准化疗与阻断丝氨酸生成的药物及经过精心管理的饮食策略相结合,医生或许能在一种难治的肺癌形式中战胜一大耐药机制。
引用: Deng, L., Yang, X., Zhang, J. et al. ΔNp63α drives serine synthesis to promote carboplatin resistance in NSCLC. Cell Death Dis 17, 227 (2026). https://doi.org/10.1038/s41419-026-08497-4
关键词: 丝氨酸代谢, 肺鳞状细胞癌, 卡铂耐药, ΔNp63α, 癌症代谢治疗