Clear Sky Science · zh
mTOR 驱动的自噬抑制定义了对 CDK4/6 抑制剂耐药的 HR+/HER2− 乳腺癌的代谢易感性
这对乳腺癌患者为何重要
由于一种称为 CDK4/6 抑制剂的药物可以减缓肿瘤细胞分裂速度,许多晚期乳腺癌患者的生存期得以延长。但不幸的是,大多数肿瘤最终会学会逃避这些药物。本研究提出一个充满希望的问题:当乳腺癌对 CDK4/6 药物产生耐药性时,是否会出现一种新的弱点,医生可以利用现有且相对简单的代谢类药物(如二甲双胍或二氯乙酰胺 DCA)来加以针对?
当细胞周期抑制药失效时
临床上,医生常用激素治疗联合 CDK4/6 抑制剂(如帕博昔利 Palbociclib 或利博昔利 Ribociclib)治疗最常见的乳腺癌类型——激素受体阳性、HER2 阴性疾病。这些药物靶向推动细胞进入分裂周期的蛋白质。然而,随着时间推移,部分癌细胞会适应并变得强烈耐药,即使在高剂量药物存在下仍继续增殖。研究者在实验室中通过让乳腺癌细胞系(T47D 和 MCF7)长期暴露于逐渐增加剂量的 CDK4/6 抑制剂来重现这一问题。最终,他们得到两类幸存者:部分耐药的细胞,以及一小群对治疗反应显著下降的高度耐药克隆。
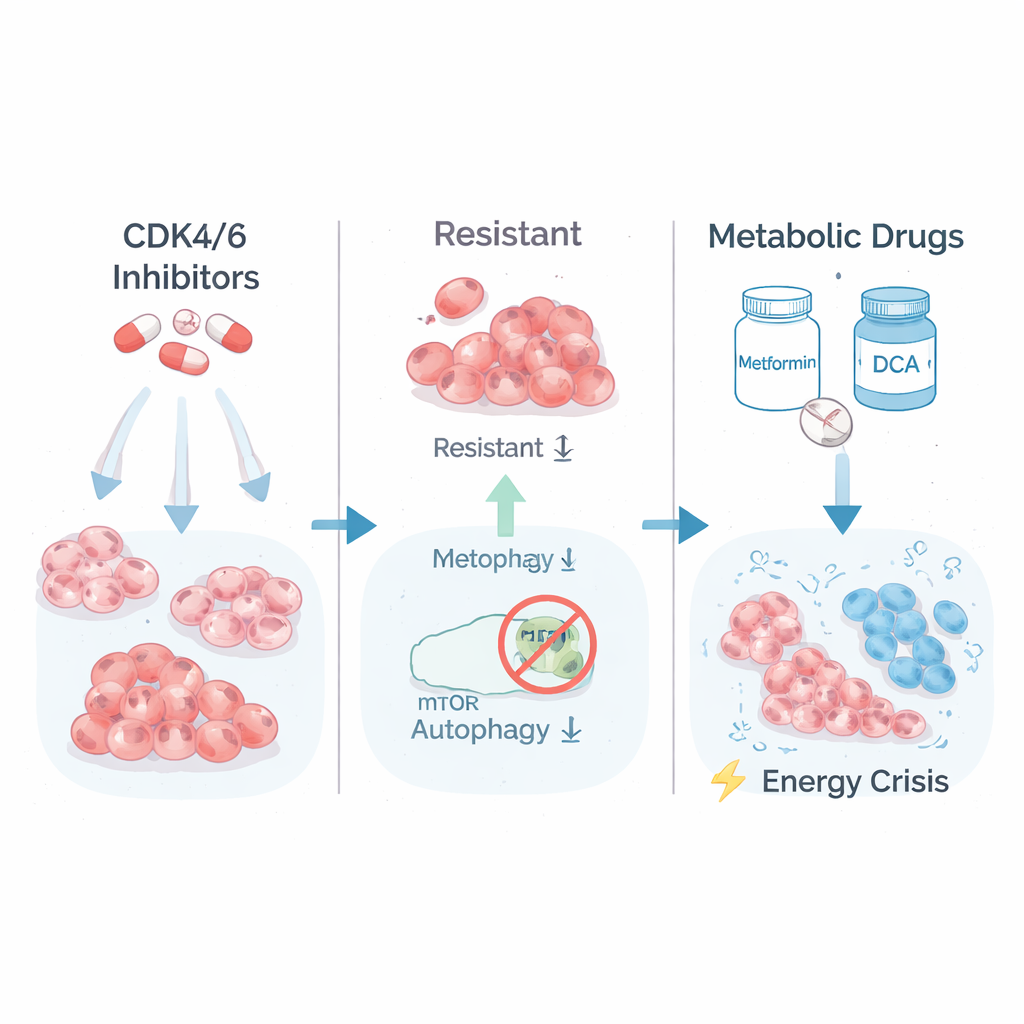
肿瘤能量利用中的隐藏弱点
为了解高度耐药细胞的不同之处,研究团队检查了哪些基因被开启或关闭。他们发现最耐药的细胞增强了与糖酵解(燃烧糖)相关的通路以及由称为 mTORC1 的蛋白复合体控制的生长信号。换言之,这些细胞处于“高速”代谢状态,以高耗能维持增殖。科学家随后检验能否利用这种“高档位”代谢反过来攻击细胞:他们用常见的降糖药二甲双胍(扰乱细胞的能量工厂)和 DCA(促使细胞更高效地处理燃料)处理耐药与原代细胞。令人注目的是,最耐药的克隆反而最脆弱:在代谢治疗下,这些克隆在培养皿中的长期生长崩溃,而原代和仅部分耐药的细胞受影响要小得多。
被阻断的自我清理与能量崩溃
为什么这些逃逸的癌细胞会对能量压力如此敏感?答案在于另一项基本的生存机制:自噬——细胞内固有的“回收与清理”系统。通常,当能量匮乏时,细胞会分解并重复利用自身成分以维持存活。研究者表明,在高度耐药的克隆中,mTORC1 过度活跃并通过化学修饰抑制了 ULK1(自噬启动的关键蛋白)。利用灵敏的报告系统,他们证明这些细胞即便在代谢药物刺激下也无法正确启动或增强自噬。因此,二甲双胍和 DCA 导致了严重的能量危机:能量低下的感应信号被触发,脂质合成被关闭,并且不可逆细胞死亡的标志物在强耐药细胞中特异性出现。
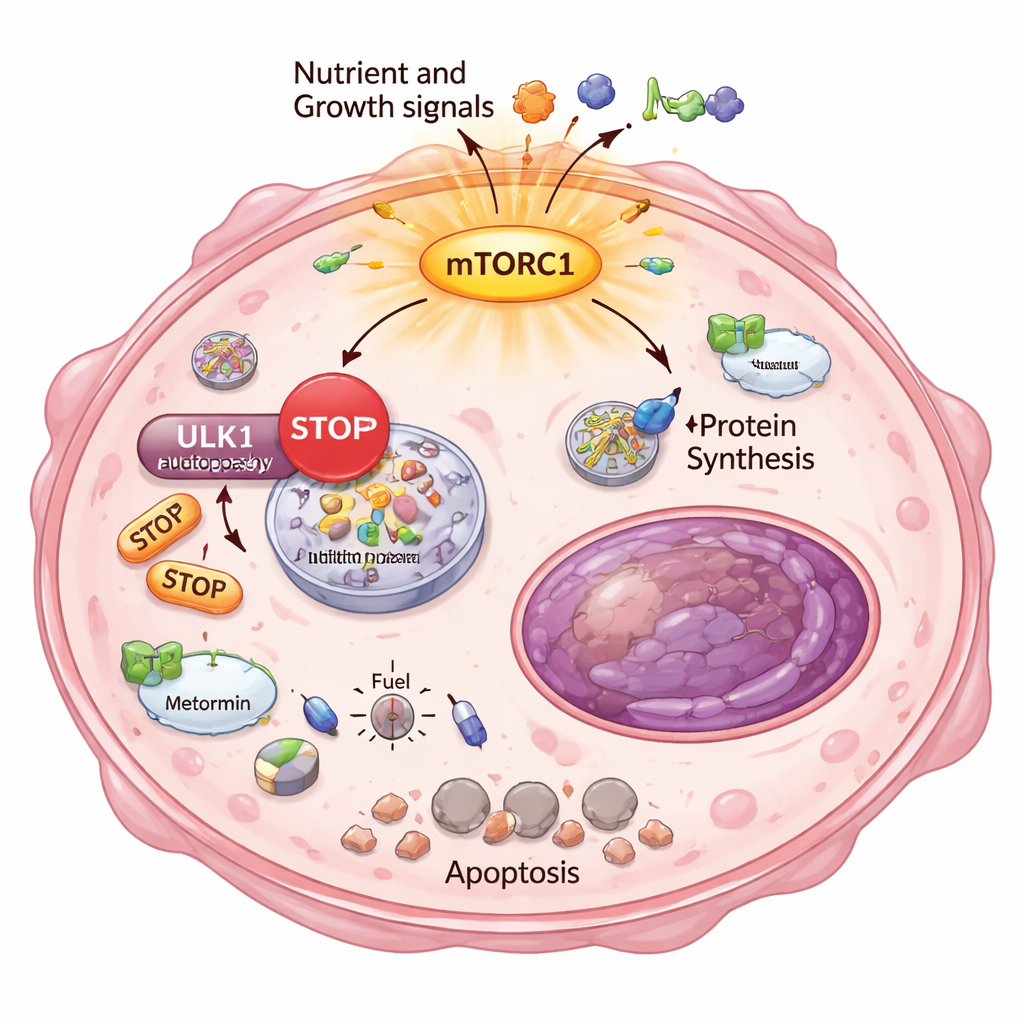
来自真实患者肿瘤的证据
实验室模型并不总能反映患者体内的情形,因此研究团队转向人体乳腺肿瘤样本。他们对一百多例癌症标本进行染色,检测 mTORC1 活性的标志(磷酸化的 4E-BP1)以及 p62——在自噬被阻断时积累的蛋白。具有高 mTORC1 活性的肿瘤往往伴随更多的 p62,支持了“过度驱动的生长信号加上低效回收”这一模式存在于真实乳腺癌中的观点,而不仅限于细胞系。这表明一部分患者的肿瘤可能具有与实验室中相同的代谢弱点。
这对未来治疗可能意味着什么
对非专业读者而言,核心信息是:当乳腺癌进化出逃避强效 CDK4/6 药物的能力时,它们也可能将自己逼入一个代谢上的窘境。通过将生长信号永久打开并关闭细胞回收机制,这些肿瘤变得高度依赖持续的能量供应。研究显示,这种状态可以被像二甲双胍和 DCA 这样的代谢药物利用——这些药物在其他疾病中已有充分认识。重要的是,作者提出可通过简单的组织学检测 mTORC1 活性和自噬标志物来筛选出那些其耐药肿瘤可能适合此类代谢性攻击的患者,从而为 CDK4/6 抑制剂失败后的更个体化救援治疗打开了可能性。
引用: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
关键词: 乳腺癌, CDK4/6 抑制剂耐药, mTOR, 自噬, 代谢治疗