Clear Sky Science · zh
通过切换促癌BCS1L异构体的剪接抑制卵巢癌进展并破坏线粒体功能
癌细胞内的发电厂
我们体内的每个细胞都依赖于被称为线粒体的小型发电厂。快速生长和扩散的癌细胞对能量有更高的需求。本研究揭示了卵巢癌如何重编程其关键的线粒体协助因子之一,并表明温和地切换该分子的“开关”可以使肿瘤断粮,同时在很大程度上保护健康组织。
为什么肿瘤依赖其“引擎”
卵巢癌细胞像许多癌症一样,能够灵活地利用不同的能量来源。研究者通过梳理大型患者数据库和单细胞谱,发现许多卵巢肿瘤将线粒体置于一种称为氧化磷酸化(OXPHOS)的高档运行模式。具有这种增强线粒体活性的肿瘤更具侵袭性,且在晚期疾病中更常见。在构建线粒体能量机器的众多蛋白中,有一个特别突出:BCS1L,一种辅助复合体III装配的伴护蛋白。高OXPHOS的肿瘤及某些肿瘤细胞亚型表现出尤其强的BCS1L活性,提示癌细胞在很大程度上依赖该协助因子来维持其“引擎”运转。
线粒体协助因子的两面性
团队发现BCS1L基因可以产生两种蛋白版本,即异构体。全长形式BCS1L-L带有一个内置的定位标签,将其送入线粒体,在那里支持复合体III的正确装配和强劲的能量输出。较短的形式BCS1L-S缺失关键片段,不能进入线粒体;相反,它位于细胞质和细胞核中,不支持能量产生。在健康组织中,短形式较为常见,但在卵巢癌中这种平衡发生翻转:长的线粒体定位形式占主导。当细胞被迫产生更多BCS1L-L时,它们的线粒体产生更多能量,维持更强的膜电位,产生更少的有害氧副产物,并更能抵抗细胞死亡。相反,当BCS1L减少时,线粒体破碎,能量产出下降,有害的氧分子上升,癌细胞更容易走向死亡。
癌细胞如何重写信息
产生长或短BCS1L依赖于细胞如何编辑其RNA信息,这一过程称为剪接。研究者寻找与BCS1L RNA相互作用并影响该选择的蛋白质。他们锁定了USP39,这是一种已与多种癌症相关的剪接因子。在卵巢癌细胞中,USP39结合在将成为BCS1L外显子2的RNA片段附近,促进其被包含,从而偏向产生长的、指向线粒体的形式。当沉默USP39时,细胞更常跳过该片段,转向短的BCS1L-S形式。这一转变削弱了复合体III,降低了线粒体呼吸和ATP产量,增加了氧化应激,并触发了癌细胞死亡。在这些细胞中恢复BCS1L-L可挽救大部分线粒体功能和存活,表明USP39主要通过BCS1L驱动了一个关键的线粒体开关。
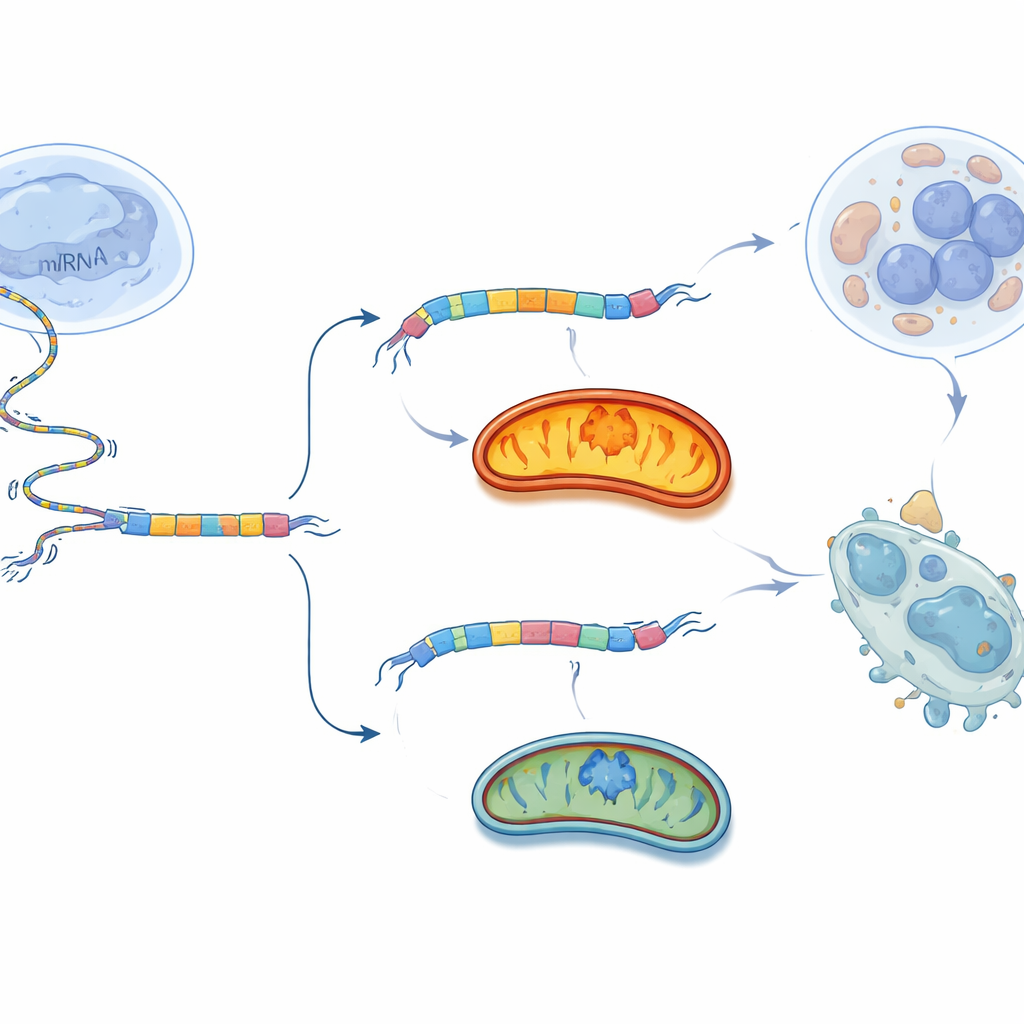
把开关反过来对抗肿瘤
研究团队没有选择广泛阻断线粒体(这可能伤及多种组织),而是采取更外科式的策略:直接推动BCS1L的剪接选择。他们设计了短片段的遗传材料,称为反义寡核苷酸(ASO),这些ASO结合在BCS1L RNA的外显子2两侧。ASO像微小的夹子一样改变剪接机器读取信息的方式,鼓励细胞跳过外显子2。在培养皿中的卵巢癌细胞中,效果最好的ASO显著减少了长的BCS1L-L形式并增加了短的BCS1L-S形式。结果是线粒体呼吸和ATP生成下降,有害氧水平上升,更多细胞经历程序性死亡。当将同一ASO注入小鼠的卵巢癌肿瘤中时,肿瘤生长减缓且肿瘤重量下降,对癌细胞的影响明显强于对正常成纤维细胞的影响。
这对患者可能意味着什么
简而言之,这项工作表明许多卵巢癌依赖一种“增压”版本的线粒体辅助蛋白来为其增长提供燃料。一种剪接因子USP39使细胞的RNA编辑机制偏向产生更多这种增压版本,从而保持肿瘤的线粒体处于最佳状态。通过使用精确设计的ASO将剪接选择切换回较弱的版本,研究者可以选择性地削弱癌细胞的线粒体,触发其死亡,同时让大多数正常细胞受到的影响较小。尽管将此类ASO药物递送到肿瘤仍是一个重大挑战,该研究将BCS1L的剪接开关指认为治疗卵巢癌的一个有前景且高度特异的新靶点。
引用: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
关键词: 卵巢癌, 线粒体, RNA 剪接, BCS1L, 反义寡核苷酸