Clear Sky Science · zh
NSD2通过氧化磷酸化抑制PD-L1表达以控制肝细胞癌中的免疫监视
为什么这个肝癌研究重要
肝细胞癌是最常见的肝癌类型,常常在晚期确诊且对多种治疗耐受性强。阻断肿瘤细胞上PD-L1“隐身斗篷”的免疫治疗药物对部分患者有效,但大多数患者无显著获益。本研究揭示了一个意想不到的参与者——一种名为NSD2的蛋白,它将肝癌细胞的能量生成方式与其被免疫系统识别的程度联系起来。理解这一联系可能指向增强现有疗法的新途径,并帮助识别哪些患者更可能受益。
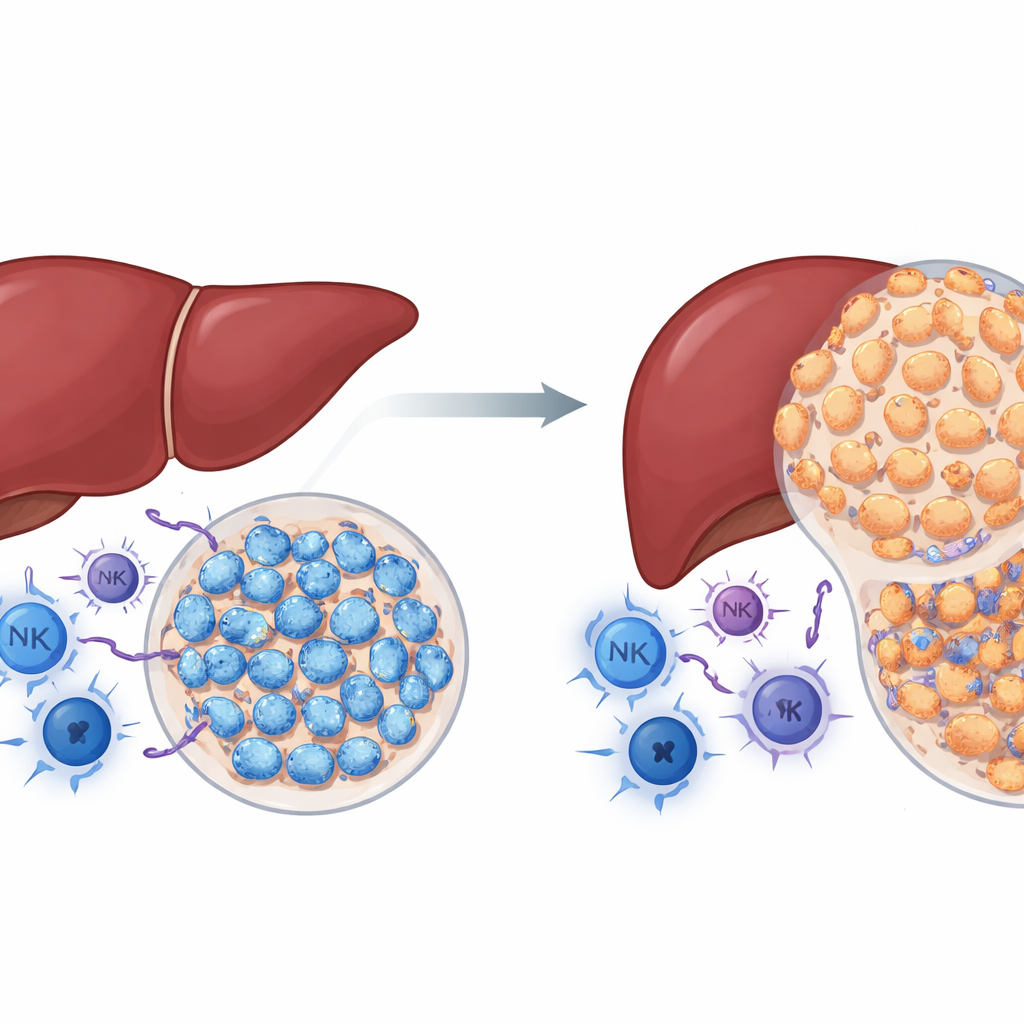
已知癌症蛋白的令人意外的角色
NSD2是一种修饰组蛋白的酶,组蛋白是DNA缠绕的蛋白质。在许多癌症中,NSD2被视为驱动肿瘤生长的因子。作者探讨了在肝癌中是否也如此。研究者使用基因工程小鼠,使NSD2在肝细胞中特异性过表达,并用一种可靠诱发肝肿瘤的化学物质处理动物。与预期相反,NSD2过表达的小鼠比对照小鼠形成的肿瘤明显更少且更小,肝脏损伤、纤维化和细胞增殖也更低。与此同时,来自NSD2过表达肝脏的肿瘤含有更多抗癌免疫细胞,包括辅助T细胞、杀伤性T细胞和自然杀伤细胞。这些发现表明,在完整免疫系统存在时,NSD2在肝癌中表现得更像是制动器而不是加速器。
肿瘤细胞的能量工厂与燃料利用
为了解NSD2如何抑制肿瘤,研究团队对肝组织的基因活性进行了分析。他们发现NSD2过表达显著抑制了参与氧化磷酸化的基因,氧化磷酸化是线粒体——细胞的“发电厂”——利用氧气产生能量的过程。随后的小鼠和人类肝癌细胞系实验显示,提升NSD2降低了许多氧化磷酸化基因的表达,减少了氧气消耗和ATP产生,并使线粒体膜电位下降,这是线粒体活性减弱的标志。同时,这些细胞消耗更少的葡萄糖,但并未转向更依赖糖酵解,表明总体能量产出减少。NSD2丧失则产生相反的效果,增强了线粒体能量和燃料利用率。
NSD2如何重编能量代谢与免疫可见性
进一步研究中,研究者将全基因组染色质图谱与基因表达数据结合,鉴定出一组在NSD2存在时被直接激活的基因。其中两个基因Camk2d和Prkce已知能抑制线粒体活性。NSD2在它们的启动子处增加了一种特定的组蛋白标记(H3K36me2),从而提升了它们的表达。将这些基因重新引入缺失NSD2的肝癌细胞可减少线粒体的氧气使用和ATP产生,证实它们是NSD2对氧化磷酸化下游的制动因子。重要的是,先前研究表明线粒体高度活跃有利于肿瘤细胞上高水平的PD-L1。与此一致,作者发现NSD2过表达降低了PD-L1水平,而NSD2丧失则在肝癌细胞和肿瘤组织中提高了PD-L1表达。
降低防护并唤醒免疫攻击
这些分子变化的功能性影响通过小鼠实验得到检验:研究者向小鼠肝脏注入经过基因改造以增加或缺失NSD2的癌细胞。缺失NSD2的细胞迅速形成更大的肿瘤,表达更多PD-L1,并且浸润的T细胞和自然杀伤细胞更少,尤其是活化的杀伤性T细胞明显减少。当研究者化学抑制线粒体复合体V(氧化磷酸化的关键组成部分)时,NSD2缺失细胞的PD-L1水平回落至接近正常,免疫细胞更能诱导肿瘤细胞死亡。同样,将Camk2d或Prkce在NSD2缺失细胞中过表达,或用抗PD-L1抗体处理肿瘤,均能减小肿瘤体积并恢复免疫细胞浸润。在患者数据集中,低NSD2表达与较差的生存相关,但有趣的是与对PD-L1靶向疗法更好的反应相关,这提示NSD2状态可能有助于预测谁能从此类药物中受益。
这对未来肝癌治疗意味着什么
对普通读者而言,关键结论是:本研究在存在功能性免疫系统的情况下,将NSD2重新定义为肝癌中的一种抑瘤因子。通过降低细胞的基于氧的能量产生,NSD2间接减少了肿瘤细胞上的PD-L1,削弱了它们的“隐身斗篷”,使免疫细胞能够识别并攻击它们。新描述的NSD2–能量–PD-L1链条提出了两种可行的思路:其一,肿瘤缺乏NSD2的患者可能是PD-L1阻断药物的优选候选者;其二,将抑制线粒体能量产生的药物与免疫疗法联合使用,可能为肝癌提供一种强有力的组合治疗策略。
引用: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
关键词: 肝细胞癌, NSD2, 氧化磷酸化, PD-L1, 肿瘤免疫治疗