Clear Sky Science · zh
SNRPD2介导的DDX39B剪接调控通过抑制CTSC隐匿外显子活化促进子宫内膜癌进展
为何癌基因中的“隐藏信息”至关重要
子宫内膜癌是常见的子宫肿瘤,全球发病率上升,但许多晚期患者仍然缺乏有效治疗选择。本研究揭示了细胞内一种微妙的过程——基因信息的剪切与拼接,如何推动子宫内膜肿瘤的生长和转移。通过描绘癌细胞依赖的脆弱“电路图”,这项工作指出了利用精准基因药物关停肿瘤的新途径。
一个亟待新解答的增长性癌症
子宫内膜癌已成为许多西方国家最常见的妇科恶性肿瘤,病例和死亡人数在西方和中国均稳步上升。手术、放疗、化疗、激素治疗和免疫治疗都有应用,但远非完善。切除子宫会终止生育,激素治疗常常失效,侵袭性肿瘤也常复发。这些挑战促使研究者深入癌细胞内部,寻找可用于更精确治疗的分子弱点。
细胞的剪接机械可能是薄弱环节
基因要发挥作用,首先被转录为长的RNA分子,这些分子必须在一个称为剪接的过程中被修剪和拼接。被称为剪接体的专门蛋白机器决定哪些片段被保留、哪些被丢弃,实际上就是对细胞制造蛋白质的“剧本”进行编辑。研究团队聚焦于剪接体成分SNRPD2,它属于帮助组装剪接体的一类“Sm”蛋白。通过挖掘大型癌症基因和蛋白数据库并分析患者样本,他们发现SNRPD2在子宫内膜肿瘤中的表达显著高于正常子宫内膜,且肿瘤中SNRPD2水平较高的患者预后更差。
关闭一位主控编辑者能抑制肿瘤
为检验SNRPD2是路人还是主动驱动因子,研究者在体外培养的子宫内膜癌细胞系中降低了其表达。沉默SNRPD2后,细胞分裂速度减慢,克隆形成减少,迁移和穿膜侵袭能力下降——这些行为与转移相关。当这些被改变的细胞移植到小鼠体内时,形成的肿瘤体积明显更小,处于活跃分裂的细胞减少。重要的是,团队设计了反义寡核苷酸——短小、类药物的合成DNA片段,能特异性靶向SNRPD2的RNA。在患者来源的异种移植模型(人体肿瘤片段在免疫缺陷小鼠中生长)中,这些反义药物显著降低了SNRPD2水平和肿瘤体积,提示SNRPD2具有临床可药性。
从剪接错误到癌症生长的三步链条
深入基因组数据后,研究者探究了SNRPD2缺失如何重编RNA信息。他们发现当SNRPD2减少时,一个关键的RNA加工酶DDX39B开始出错。正常情况下,DDX39B有助于从其自身转录本中剪除特定的内含子——应被切除的RNA片段。缺乏足够的SNRPD2时,该内含子保留,产生了异常的DDX39B RNA,细胞很快将其降解。DDX39B水平下降随后在另一个基因CTSC上产生连锁效应;CTSC编码一种已知支持肿瘤生长与扩散的蛋白酶。在健康状态下,CTSC RNA中有一个被忽略的“隐匿”外显子,使细胞得以生成全长、活性的CTSC蛋白。DDX39B减少时,这个隐匿外显子被错误包含,向RNA插入早停信号。畸形的CTSC信息被降解,无法产生大量蛋白,癌细胞因此丧失部分侵袭性。
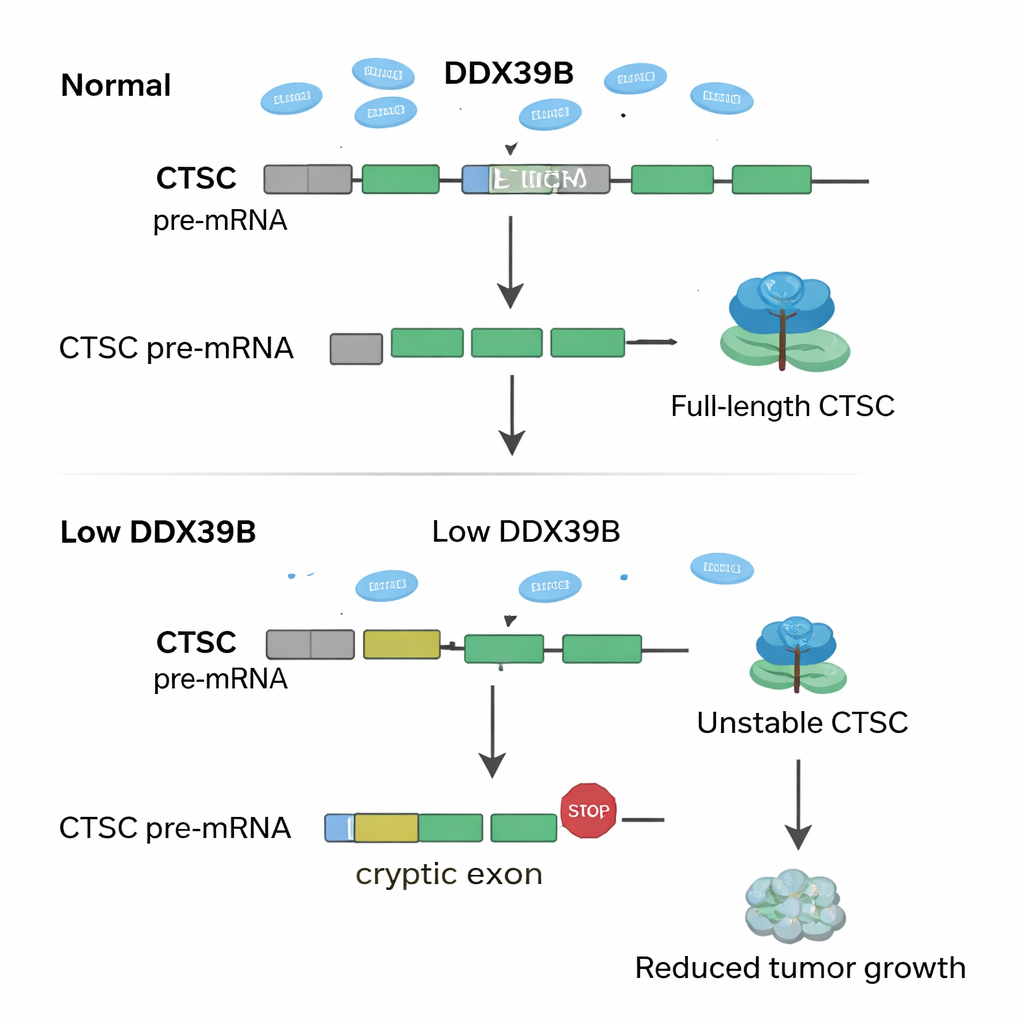
这对未来治疗意味着什么
简而言之,作者揭示了一个被子宫内膜癌细胞利用的传导系统——SNRPD2 → DDX39B → CTSC。高水平的SNRPD2维持DDX39B的丰度;DDX39B又阻止CTSC激活有害的隐匿外显子,从而保持有利于肿瘤生长和扩散的全功能CTSC蛋白。当SNRPD2被抑制时,这条链条崩溃,CTSC水平下降,肿瘤减弱。对于非专业读者,关键观点是癌细胞依赖极为精确的RNA编辑,即便是小幅度的“强制错误”也能选择性地抑制其生长。用反义药物靶向SNRPD2,或直接促使CTSC使用隐匿外显子,可能为子宫内膜癌患者提供新的、更个性化的治疗选择。
引用: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
关键词: 子宫内膜癌, RNA剪接, SNRPD2, DDX39B, CTSC