Clear Sky Science · zh
DNMT2通过下调5’tiRNAGly-GCC的生成抑制未分化甲状腺癌进展
为何这种隐蔽的RNA化学很重要
未分化甲状腺癌是人类最致命的癌症之一,尽管接受手术、放疗和化疗,患者常在数月内死亡。本研究揭示了癌细胞内部一个令人意外的元凶:转运RNA(tRNA)上的微小化学标记——这些分子负责帮助合成蛋白质。作者表明,当一种特定酶DNMT2缺失或减少时,甲状腺肿瘤生长更快、转移更易发生,并对常用化疗药阿霉素(doxorubicin)产生耐药。更有趣的是,他们鉴定出在DNMT2低表达时出现的一段小RNA片段,并证明阻断该片段可能成为一种新的治疗策略。
失去的保护性酶
转运RNA(tRNA)通常将氨基酸输送到细胞的蛋白合成机构,其稳定性依赖于精细的化学修饰。DNMT2是一种在tRNA特定位点加入甲基等修饰的酶。在许多癌症中,DNMT2水平升高并被认为助长肿瘤,但在这里情况相反。通过分析大量患者数据库和肿瘤样本,研究者发现未分化甲状腺癌组织中的DNMT2水平显著低于正常甲状腺。肿瘤中DNMT2较高的患者通常具有更长的无恶化生存期,这提示在这种疾病中DNMT2更像是制动器而非加速器。
低DNMT2如何助长侵袭性行为
为观察DNMT2在癌细胞中的实际作用,团队在体外培养的未分化甲状腺癌细胞系和小鼠模型中操纵其表达水平。降低DNMT2后,细胞增殖更快、更容易穿过基质并形成更多集落,均为侵袭性肿瘤的典型特征。这些细胞对阿霉素也变得不那么敏感。在小鼠体内,经工程化使DNMT2下降的肿瘤长得更大且更易转移到肺,而提高DNMT2表达则呈相反效应。研究者部分将这些变化追溯到上皮–间质转化(EMT)程序的激活,该程序使癌细胞更具移动性与侵袭性。
从受损tRNA到有害的小片段
进一步探究显示,DNMT2在三种特定tRNA的C38位点上添加甲基标记。失去这种保护后,这些tRNA更容易被另一种酶血管生成素(angiogenin)切割。该切割产生了一段来自tRNA-Gly-GCC的短RNA片段,称为5’tiRNAGly-GCC。通过测序和生化实验,作者发现当DNMT2表达低时,这种片段尤其是来源于载甘氨酸的tRNA的片段会积累。在试管实验中,加入甲基标记可强烈保护tRNA免遭切割,证实DNMT2通常保护这些分子不被裂解成更小、可能有害的片段。
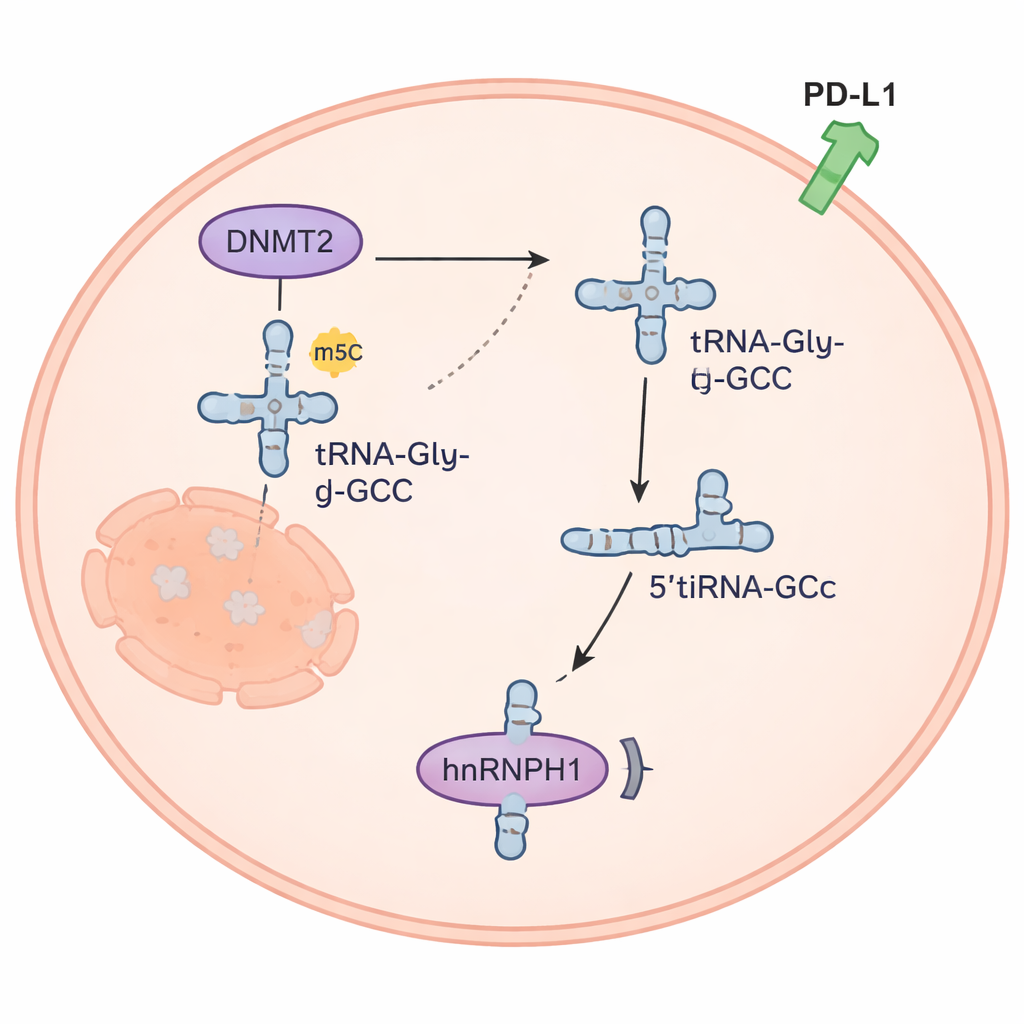
微小RNA片段重塑癌症信号
5’tiRNAGly-GCC片段不仅是分子残骸。它在未分化甲状腺癌细胞中丰度很高,而在正常甲状腺细胞中则很少。当研究者人为提高其水平时,癌细胞增殖更快、侵袭性增强且对阿霉素抵抗性增加;降低该片段则产生相反效果。在小鼠中,一种化学修饰的5’tiRNAGly-GCC抑制剂减缓了肿瘤生长,并且将该抑制剂与阿霉素联合使用的效果优于任何一种单独治疗。团队发现5’tiRNAGly-GCC能结合蛋白质hnRNPH1并降低其细胞内含量。由于hnRNPH1通常有助于抑制免疫相关蛋白PD-L1的水平,失去hnRNPH1会导致PD-L1升高,这一变化可帮助肿瘤逃避免疫攻击,并与肿瘤周围调节性T细胞(Treg)的累积相关联。
对未来治疗的意义
简言之,这项研究揭示了一条链式反应:当DNMT2降低时,某些tRNA失去保护性标记,被切成小片段,其中一段(5’tiRNAGly-GCC)抑制了限制PD-L1的蛋白。结果是癌症更具侵袭性、耐药且更易逃避免疫。与其直接尝试提升DNMT2——这在其他组织可能存在风险——作者建议针对有害的RNA片段本身。他们在小鼠中的5’tiRNAGly-GCC抑制剂实验,尤其是与阿霉素联合使用时,为中断这一微观RNA回路以驯服这种最致命甲状腺癌形式提供了早期证据。
引用: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
关键词: 未分化甲状腺癌, DNMT2, tRNA片段, 化疗耐药, PD-L1