Clear Sky Science · zh
揭示ZNF124作为神经退行性疾病中新决定因子:通过MSX2转录调控协调光感受器稳态
这一发现为何关乎视力
视网膜色素变性是导致遗传性失明的主要原因之一,但在近40%的患者中,医生仍无法确定致病基因。本研究发现了一个新的遗传因子,称为ZNF124,它有助于维持眼内感光细胞的生存。通过展示该基因的突变如何破坏视网膜内的一系列分子“开关”,研究人员为诊断并潜在地为正在失去视力的人群开发靶向治疗开辟了新途径。
一种隐匿的遗传性视力丧失原因
研究团队研究了一个大家族,其中若干儿童出现了典型的视网膜色素变性症状:早年夜盲、周边视野缩小以及中心视力逐步丧失。细致的眼科检查显示视网膜变薄和对光的电生理反应减弱,这两项都是杆细胞和锥细胞损伤的标志。然而,在已知的80多种视网膜色素变性基因中,这些患者均未发现明显缺陷,这提示一个尚未被发现的基因可能是他们疾病的罪魁祸首。
找到一个出问题的遗传开关
通过全外显子测序——读取DNA中编码蛋白的部分——团队发现了ZNF124基因中一个罕见且此前未报道的突变。该突变改变了该基因RNA的拼接方式,在一个关键的连接位点删除了几个碱基。因此,ZNF124蛋白被截短并丧失了其锌指结构,该结构通常用于识别并结合特定的DNA序列。由于锌指蛋白常作为主控开关,控制许多其他基因的开启或关闭,受损的ZNF124可能对视网膜细胞产生广泛影响。
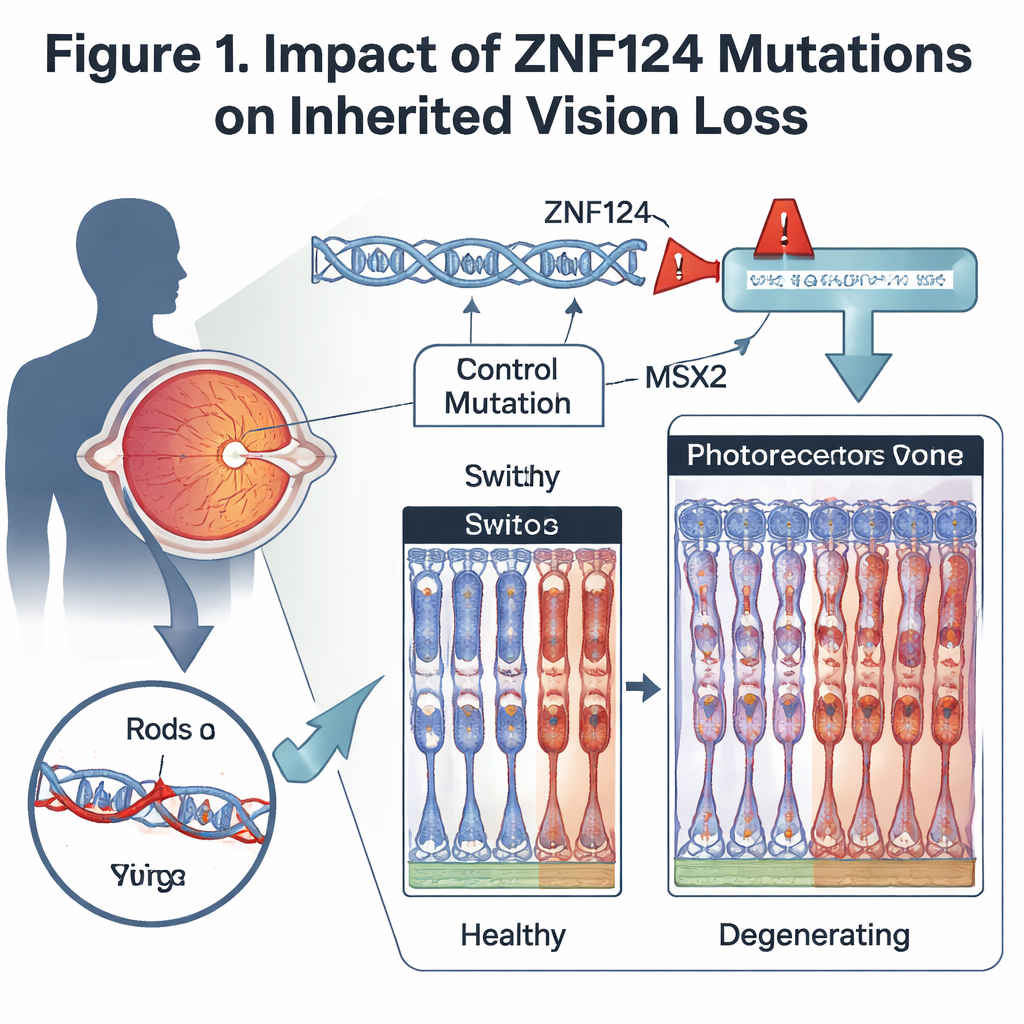
在动物模型中检验该基因
为观察该开关丢失如何影响眼睛,科学家们在视网膜中有选择性地敲除了小鼠中最接近ZNF124的同源基因Gm20541。随着年龄增长,这些动物出现了视功能下降:它们对弱光和强光的电生理反应减弱,显微检查显示含有光感受器的视网膜层逐步变薄。支持夜视的杆细胞和支持色觉与昼视的锥细胞均表现出外段变短和关键视觉蛋白丢失。其他视网膜细胞,例如某些双极细胞,也减少了,而支持细胞被激活,这是对慢性视网膜损伤的常见反应。
揭开ZNF124–MSX2调控通路
接下来的问题是ZNF124通常控制哪些基因。通过将蛋白在DNA上的结合位点绘制出来的生化方法,结合来自小鼠视网膜的全局RNA表达数据,团队发现ZNF124结合并激活另一个名为MSX2的基因。在健康细胞中,ZNF124附着于MSX2“开启区”中的特定短序列并增强其活性。在缺失Gm20541的小鼠中,MSX2的表达下降了超过一半。当研究人员在杆细胞中有选择性删除MSX2时,这些动物也出现了光感受器层变薄和外段缩短,重现了类似缺失ZNF124模型小鼠的缺陷。这将MSX2置于ZNF124下游的关键通路中,对于光感受器的生存至关重要。
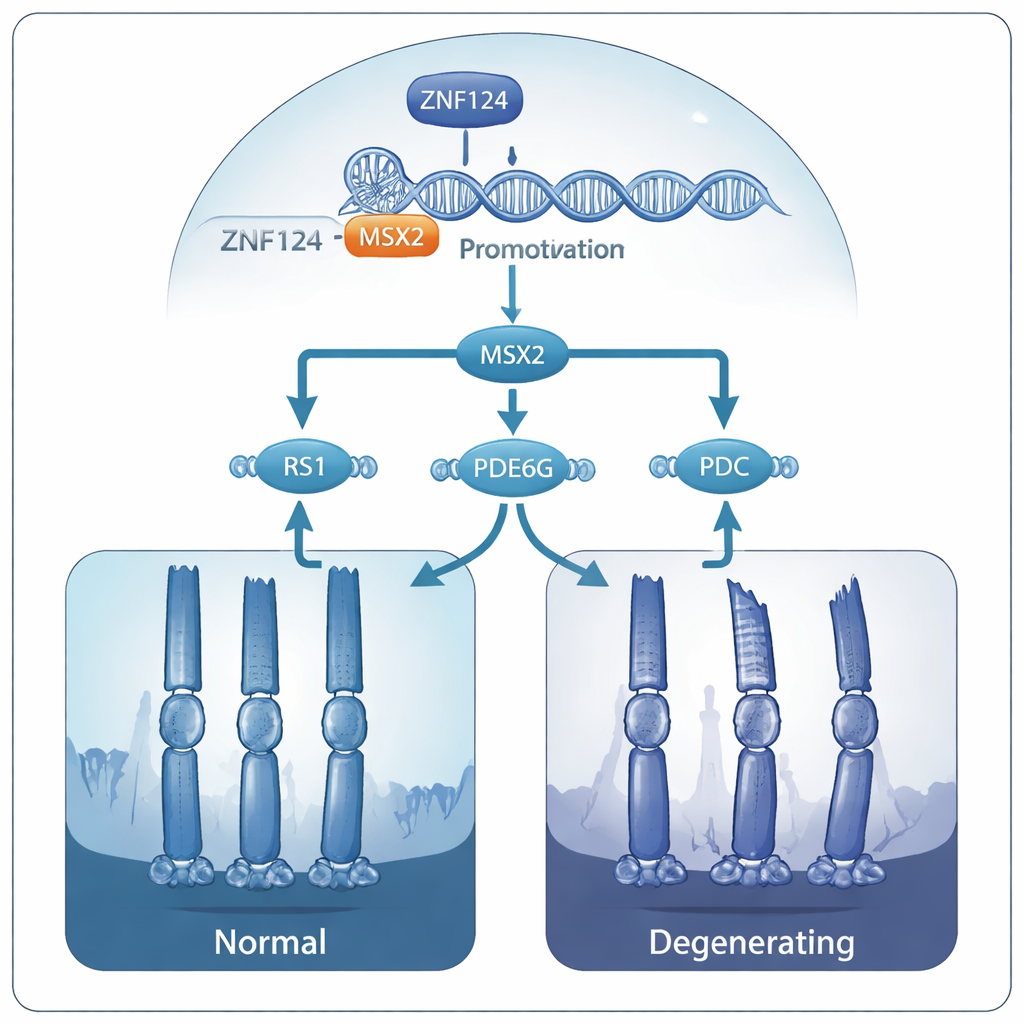
从基因开关到脆弱的光感受器
进一步分析显示,MSX2反过来有助于维持若干已知与遗传性视网膜疾病相关的基因:RS1、PDE6G和PDC。这些基因支持视网膜的结构以及视觉信号的化学过程。当MSX2减少时,这三种基因的活性都下降,其蛋白产物也相应减少。作者提出,在携带损伤性ZNF124突变的人群中,这整个级联被削弱:ZNF124无法充分激活MSX2,MSX2无法维持RS1、PDE6G和PDC,随着时间推移,光感受器失去结构完整性并死亡,导致进行性视力丧失。
对患者与治疗的意义
对非专业读者而言,核心信息是视网膜依赖于精细调控的遗传开关层级。该研究将ZNF124确认为一个新的顶层开关,其功能失效可通过特定的下游伙伴MSX2及其靶基因引起遗传性失明。在临床上,ZNF124现在可以被纳入基因检测面板,帮助更多家庭获得精确诊断。从长期看,恢复ZNF124、MSX2或受影响下游基因活性的疗法,可能有助于稳定或挽救光感受细胞,为目前原因不明的视网膜色素变性患者带来新的希望。
引用: Yang, Y., Jiang, X., Li, S. et al. Unveiling ZNF124 as a novel determinant in neurodegeneration: orchestration of photoreceptor homeostasis through MSX2 transcriptional regulation. Cell Death Dis 17, 234 (2026). https://doi.org/10.1038/s41419-026-08487-6
关键词: 视网膜色素变性, 光感受器, ZNF124, MSX2, 遗传性视网膜疾病