Clear Sky Science · zh
UBE3A介导的mH2A1泛素化激活TERT转录以促进胰腺癌的衰老抗性
这项研究对患者的重要性
胰腺癌是最致命的癌症之一,部分原因在于肿瘤细胞特别擅长逃避机体固有的“衰老刹车”。本研究揭示了一个隐蔽的分子“破坏回路”,帮助胰腺癌细胞保持年轻、持续分裂并抵抗治疗。通过理解这一回路,研究者指出了一种新的策略:诱导肿瘤细胞进入衰老状态,然后选择性清除它们,从而为更智能的组合疗法打开了可能性。
衰老:机体天然的肿瘤刹车
所有细胞都带有一个内部时钟,最终会让它们停止分裂,这一过程称为衰老。在胰腺早期病变中,这个时钟可以通过使癌前细胞永久停用来减缓肿瘤发展。许多抗癌疗法也部分依赖于将肿瘤细胞推入这种“老化”状态。然而,如果这些衰老细胞未被清除,它们可能促发炎症并助长癌症复发。这催生了一种新治疗思路:先将癌细胞诱导为衰老态,然后用专门对衰老细胞有毒性的“清老药”将其消除。
聚光灯下的促癌酶
为寻找帮助胰腺癌细胞抗衰的基因,团队挖掘了大量患者数据库,并在肿瘤样本与细胞系中验证了发现。他们锁定了名为UBE3A的蛋白,这是一种将其他蛋白标记以便降解的酶。胰腺肿瘤中的UBE3A水平明显高于邻近正常组织,且UBE3A较高的患者常伴随肿瘤更大、分期更晚和生存率更低。在体外培养的细胞中,提升UBE3A加速了细胞生长,降低了细胞衰老的典型标志,并减少了衰老细胞常见的炎性分泌物。沉默UBE3A则产生相反效应,并且在小鼠模型中显著抑制了肿瘤生长和肝转移。 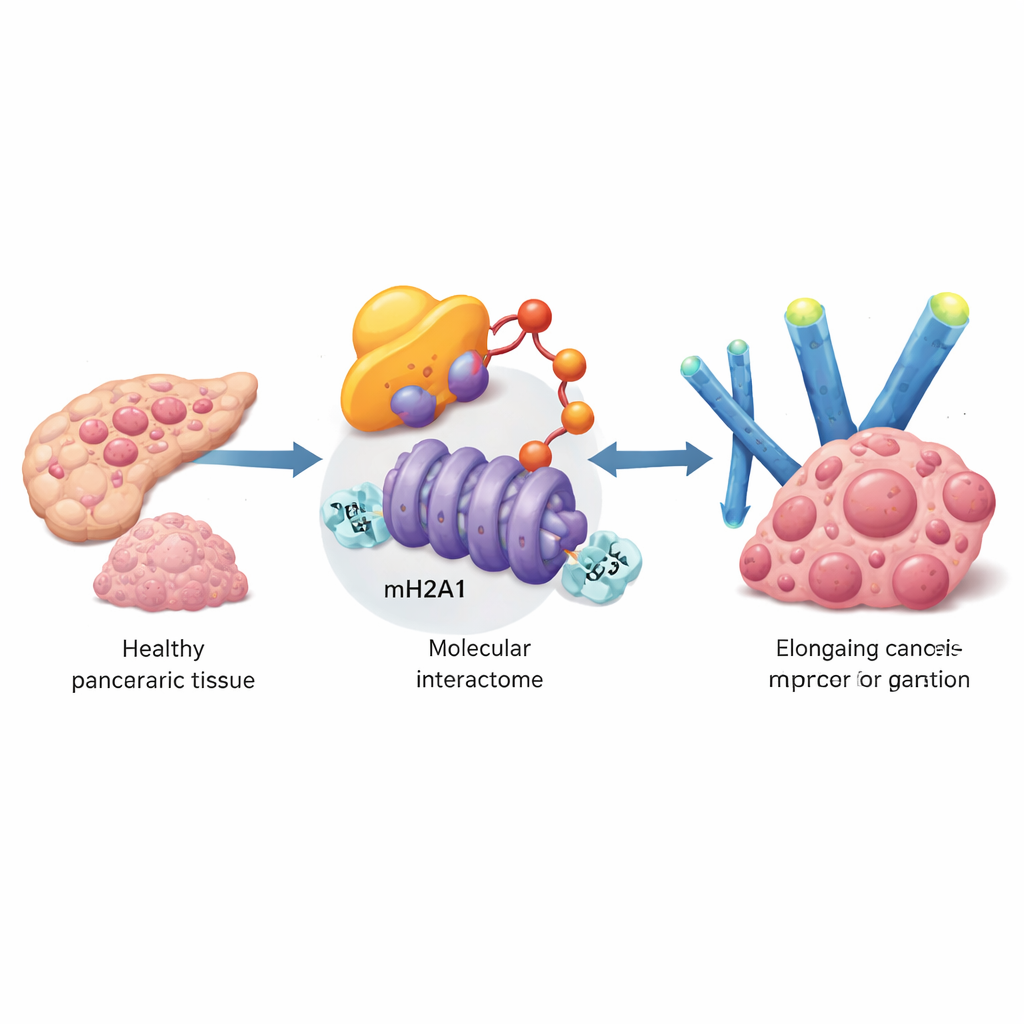
癌细胞如何抹去染色质刹车
深入研究时,研究者探查了UBE3A作用的分子对象。借助先进的质谱筛查,他们发现UBE3A结合并化学性地标记一种特殊的组蛋白变体——macroH2A1(mH2A1),该变体有助于染色质致密化,通常作为基因活性抑制的刹车。UBE3A在mH2A1的特定位点上附加一串“我要被销毁”的标记,使其被细胞的蛋白质降解系统切割。在胰腺肿瘤中,mH2A1水平在UBE3A高表达处较低,恢复mH2A1可以抵消UBE3A阻断衰老并促进肿瘤生长的能力。这揭示了关键步骤:胰腺癌细胞通过利用UBE3A去除mH2A1,从而剥夺了一道保护性的染色质标记。
解锁端粒酶以保持细胞年轻
下一个问题是mH2A1被移除后哪些基因被释放。通过结合RNA测序和DNA结合位点图谱,团队确定端粒酶基因TERT是一个核心目标。端粒酶维持染色体末端的保护帽,使细胞得以持续分裂而不进入衰老。研究表明,mH2A1通常位于TERT基因内的一个增强子区域,在那里它招募另一种酶EZH2,在附近组蛋白上沉积抑制性化学标记。这一组合使TERT被压低并允许端粒缩短。当UBE3A破坏mH2A1时,抑制复合体解体,增强子被激活,TERT打开,端粒得到维持,胰腺癌细胞因此获得抗衰老能力。不能为蛋白打标记的UBE3A突变体,或无法被标记的mH2A1突变体,会破坏这一回路并恢复衰老刹车。
将衰老诱导与清老清理相结合
最后,研究者检验了能否将此通路用于治疗。关闭UBE3A使胰腺癌细胞趋向衰老,并增加它们对BCL‑2家族抗凋亡蛋白的依赖——这是衰老细胞的已知弱点。团队随后将UBE3A抑制与ABT‑263(一种针对这些存活蛋白的清老药)联合使用。在培养细胞中,组合治疗使更多癌细胞经历程序性死亡,明显优于任一单独治疗。在小鼠模型中,当动物接受ABT‑263时,UBE3A降低的肿瘤进一步缩小,肿瘤内的增殖标志显著下降。 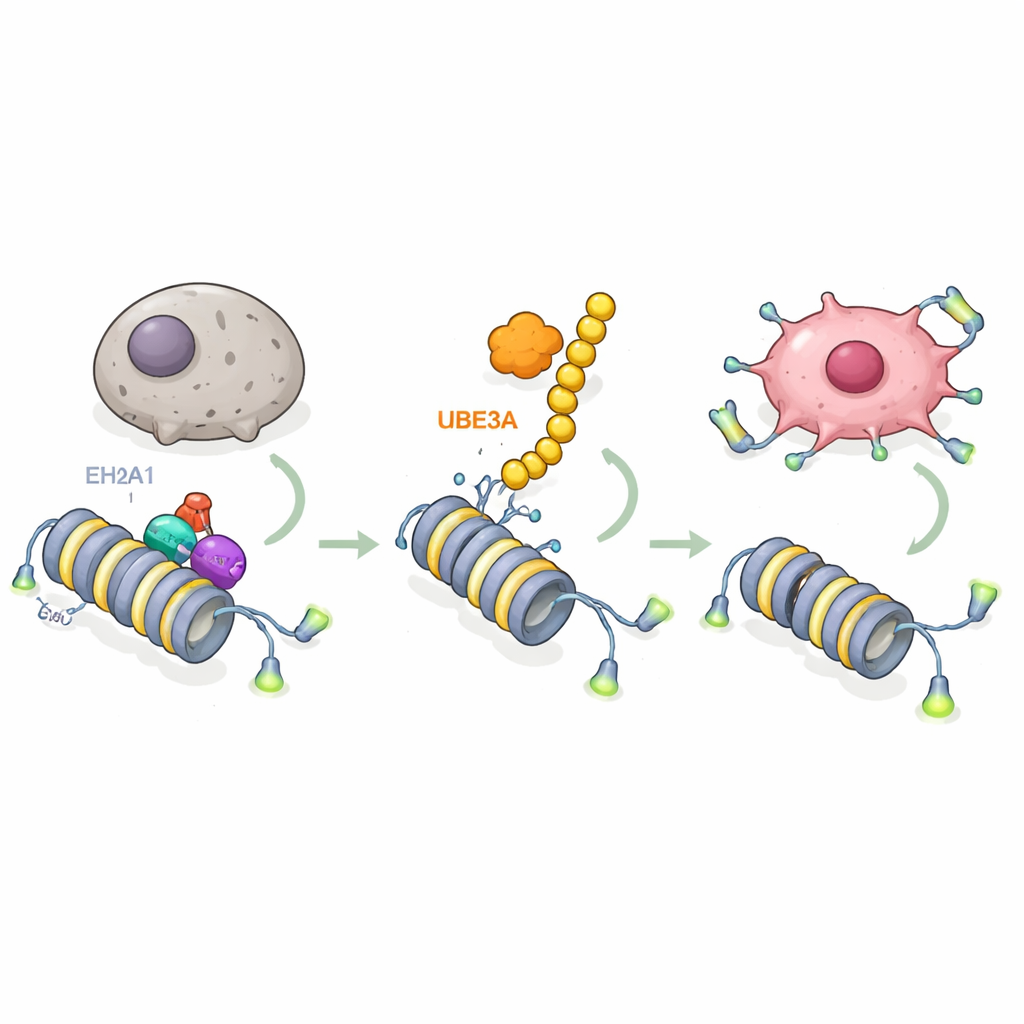
对未来治疗的意义
这项工作揭示了胰腺癌细胞如何避免衰老的一条详细事件链:UBE3A破坏染色质刹车mH2A1,进而解除对端粒酶基因TERT的抑制并维持端粒,使细胞得以持续分裂。通过靶向UBE3A,医生可能能重新激活细胞的天然衰老程序,然后使用像ABT‑263这样的清老药选择性清除这些脆弱的衰老肿瘤细胞。尽管仍需更多研究将该机制转化为临床疗法,但UBE3A–mH2A1–TERT轴为对抗这一最具治疗耐受性的癌症之一提供了一个有前景的新切入点。
引用: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
关键词: 胰腺癌, 细胞衰老, 端粒酶, 泛素连接酶, 清老药疗法