Clear Sky Science · zh
Semaphorin 6D 驱动抗肿瘤 I 型干扰素反应以重编结直肠癌肿瘤微环境
这项研究对结肠癌患者的重要性
结直肠癌是全球主要致死癌症之一,部分原因在于许多肿瘤对现有疗法(包括最前沿的免疫治疗药物)具有抗性。本研究揭示了结肠肿瘤内一个经常被关闭的天然“刹车系统”,并展示了如何重新启动它以重启免疫系统的抗癌作用。理解这一隐蔽的控制开关,可能帮助医生更好地预测病程并设计联合疗法,使免疫治疗对更多患者有效。
肿瘤细胞内的沉默守护者
研究的核心分子是 Semaphorin 6D(SEMA6D),最初以引导神经生长和参与心脏发育而闻名。研究者发现,在结直肠癌中 SEMA6D 实际上具有抑瘤作用:在健康结肠组织中可检测到它,但在癌变组织中其表达显著降低。在多个患者数据集和肿瘤样本中,低水平的 SEMA6D 与肿瘤体积更大、侵袭更深、转移更多以及生存显著更差相关。即便在考虑其他临床因素后,这一模式仍然存在,表明 SEMA6D 是评估结直肠癌侵袭性的重要独立标志。
肿瘤如何关闭这道防线
研究团队进而探究为何 SEMA6D 在肿瘤中常被缺失。他们发现该基因常通过启动子高甲基化被关闭——即在基因控制区附加的化学标签,像是覆盖开关的分子胶带。通过细致的 DNA 绘图,他们显示 SEMA6D 控制区的关键片段在癌细胞中高度甲基化,而在正常结肠细胞中则不是。当用一种用于血液癌症的去甲基化药物处理癌细胞时,甲基标记被去除,SEMA6D 的表达得以恢复。最低的 SEMA6D 水平出现在已知具有高 DNA 甲基化、高基因组不稳定性和强转移倾向的结肠癌亚型中,进一步强化了这种沉默机制与侵袭性疾病之间的联系。
从生长抑制到免疫助推
恢复 SEMA6D 在两个层面改变了肿瘤行为。首先,在癌细胞层面,强制上调 SEMA6D 可减缓细胞增殖,降低迁移和侵袭能力,并逆转上皮–间质转化的特征——这是帮助肿瘤扩散的程序。在培养皿和来自患者肿瘤的三维类器官中,SEMA6D 高表达的细胞形成的克隆更少、更小,并显示出更多的程序性细胞死亡迹象。在小鼠体内,过表达 SEMA6D 的肿瘤生长更慢,肺和肝转移更少,而敲低 SEMA6D 则有相反效果。其次,在免疫层面,免疫健全小鼠中富含 SEMA6D 的肿瘤含有更多 CD4 和 CD8 T 细胞——适应性免疫的主要攻击力量——而 SEMA6D 缺乏的肿瘤则相对缺少这些防御者。当研究者去除 T 细胞时,SEMA6D 的增殖抑制效应大部分消失,表明其许多作用来自于动员免疫系统。
解读细胞内的警报通路
进一步深入研究,团队描绘出将 SEMA6D 与免疫激活连接起来的分子步骤。在肿瘤细胞表面,SEMA6D 通过伴侣受体 Plexin A4 发信号。细胞内,这一对分子与名为 IRF9 的蛋白发生物理相互作用,IRF9 是响应 I 型干扰素(细胞用来对抗感染的抗病毒警报信号)机制的关键组成部分。当 SEMA6D 存在且 Plexin A4 完整时,IRF9 及其伙伴被激活,启动一系列干扰素刺激基因,并帮助肿瘤细胞发出招募并激活 T 细胞的信号。去除 SEMA6D 或 Plexin A4 会打断这条链条并使警报静音;恢复 IRF9 可部分挽救该效应。在小鼠中,具有活跃 SEMA6D–Plexin A4–IRF9 信号的肿瘤有更多浸润的 T 细胞和更低的增殖标志物 Ki-67 水平,这与更强的免疫压力相一致。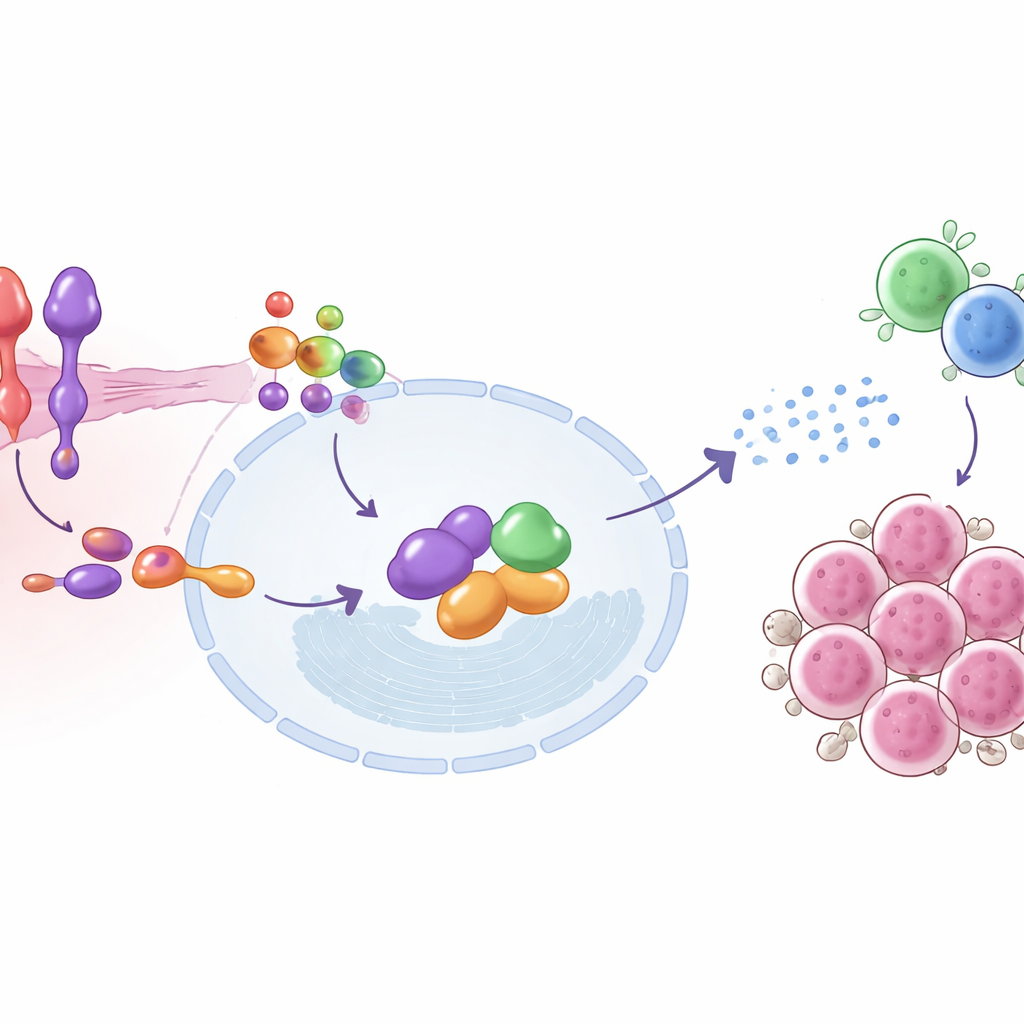
用联合疗法唤醒免疫
鉴于 SEMA6D 被甲基化沉默,作者测试了去甲基化药物是否能在体内重新激活它,从而改善对免疫检查点抑制剂的反应。在小鼠结肠肿瘤中,先用地西他滨处理再施以抗–PD-1 抗体,肿瘤生长远比单独任一治疗慢。该组合治疗提高了 SEMA6D 水平,增强了干扰素通路活性,降低了细胞增殖并增加了 T 细胞浸润。这些结果表明,通过剥离诸如 SEMA6D 等免疫相关基因上的甲基化“锁”,表观遗传药物可将免疫学上“冷”的肿瘤变得更“热”,从而更易受检查点抑制剂攻击。
对未来治疗的意义
对非专业读者而言,结论是部分结肠癌通过化学方式关闭内置的危险信号来躲避免疫系统。本研究将 SEMA6D 确认为这一信号及一个有前景的治疗靶点。测定 SEMA6D 及其甲基化状态可能有助于对肿瘤进行分型、预测预后并指导治疗选择。同样重要的是,这项研究为将去甲基化药物与免疫治疗联合使用以重启免疫监视提供了明确的生物学依据。尽管仍需临床试验验证,这一策略有望在未来把免疫治疗的益处扩展到更多结直肠癌患者群体。
引用: Shi, W., Zhang, F., Sun, WQ. et al. Semaphorin 6D drives anti-tumor type I interferon responses to reprogram the tumor microenvironment in colorectal cancer. Cell Death Dis 17, 256 (2026). https://doi.org/10.1038/s41419-026-08478-7
关键词: 结直肠癌, 肿瘤微环境, 表观遗传治疗, I 型干扰素, 肿瘤免疫学