Clear Sky Science · zh
来源于干细胞的细胞外囊泡可挽救与SHANK3相关的自闭症神经和小鼠模型中的细胞表型及行为缺陷
带来巨大潜力的小型信使
自闭谱系障碍及相关疾病常常可追溯到大脑细胞连接和通讯方式中的细微异常,这些异常在任何症状出现之前就已存在。该研究探讨了一个新兴观念:细胞释放的微观“包裹物”——称为细胞外囊泡——可能既能在脑细胞间传播有害变化,也可能在经过工程改造后帮助逆转这些变化。研究者通过使用人类干细胞衍生的神经元和一个成熟的小鼠模型,考察这些囊泡如何影响与SHANK3基因相关的一种自闭症形式中的脑活动,以及来自健康干细胞的囊泡是否能恢复较为典型的脑功能和行为。
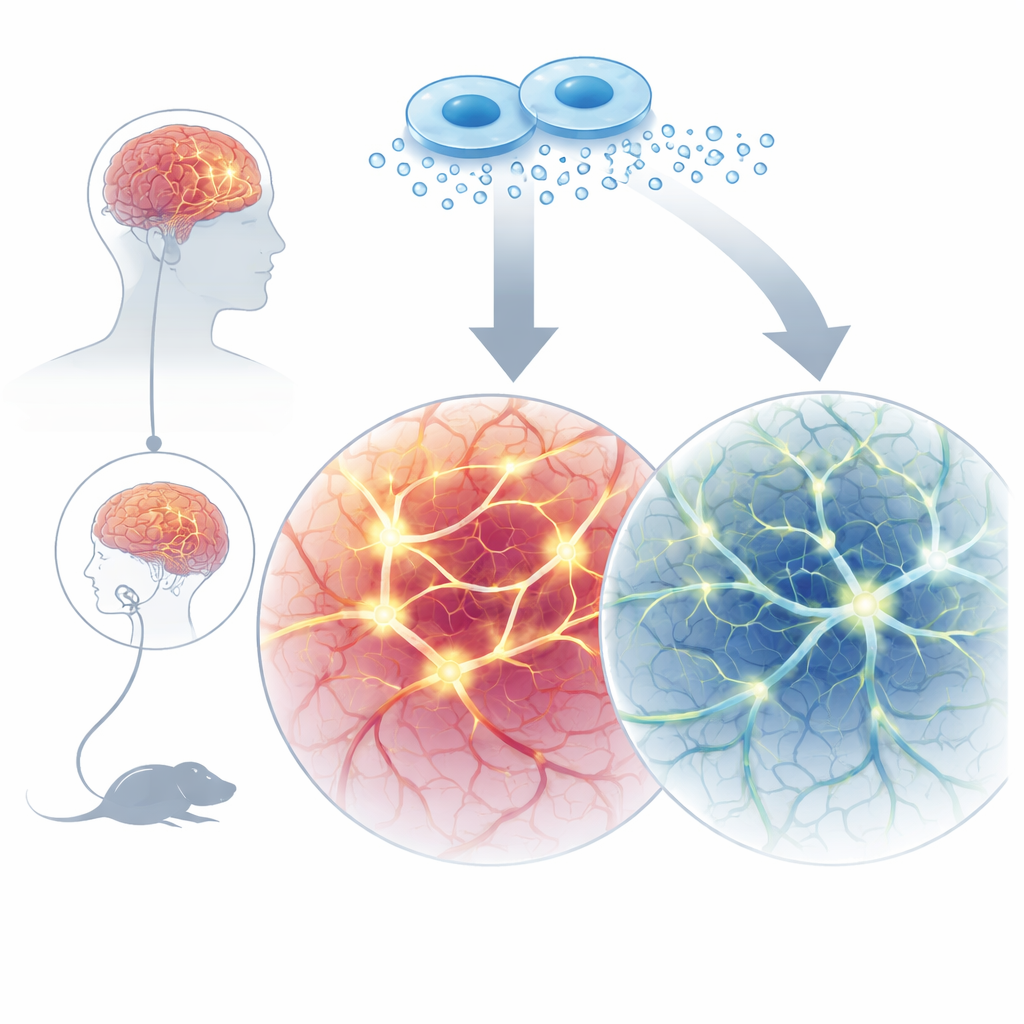
当大脑线路发育过快
一些自闭症或Phelan-McDermid综合征患者携带SHANK3基因的变异,SHANK3有助于组织神经元之间交流的接触点。在早期工作中,团队显示来自携带SHANK3突变患者细胞培养的人类神经元发育异常快速并发放过多电信号,这种模式称为高兴奋性。缺失Shank3的小鼠模型也表现出类似的早期过度活动。这些发现支持这样的观点:在早期发育阶段,某些形式的自闭症并非以脑回路功能弱化为特征,而是以连接和发放的初期激增为起点,随后导致电路失衡。
能传播问题的细胞包裹物
几乎所有细胞,包括神经元,都会释放被膜包裹的微小囊泡,内含蛋白质、RNA及其他分子。这些细胞外囊泡作为传递者,使细胞能够影响邻近细胞。研究者提出疑问:SHANK3突变神经元释放的囊泡是否携带会改变健康神经元行为的信号。他们从一位SHANK3突变患者和一位无突变的近亲分别培养出人类皮质神经元,收集各自的囊泡,然后在培养间“互换”这些囊泡。令人惊讶的是,暴露于SHANK3突变神经元囊泡的健康神经元开始在外观和行为上更像突变细胞:它们发放更多动作电位,显示更强的自发活动,并呈现与高兴奋性一致的电生理特性。相反,当用健康神经元的囊泡处理突变神经元时并未见改善,表明这些囊泡可能缺乏足够的修复性货物。
作为平抑影响的干细胞囊泡
由于囊泡可以跨越生物屏障且比移植细胞更不易引发免疫反应,它们具有吸引人的治疗潜力。因此,研究团队测试了来自两种干细胞来源的囊泡:间充质干细胞(源自骨髓)和诱导多能干细胞(经重编程的成人细胞)。当在SHANK3突变的人类神经元成熟过程中反复添加这些干细胞囊泡时,神经元的行为朝向正常方向转变。它们的钠、钾电流下降,发生动作电位串发的倾向减少,突触信号的强度和频率更接近对照神经元。蛋白质组学分析——对囊泡内蛋白的深度调查——显示突变神经元的囊泡富含与异常接线相关的突触结构蛋白和肌动蛋白调控因子,而干细胞囊泡则携带与突触修剪、可塑性和稳态相关的分子,如补体成分和生长因子。这种差异提示了为何一类囊泡会加剧高兴奋性,而另一类则能对抗它。
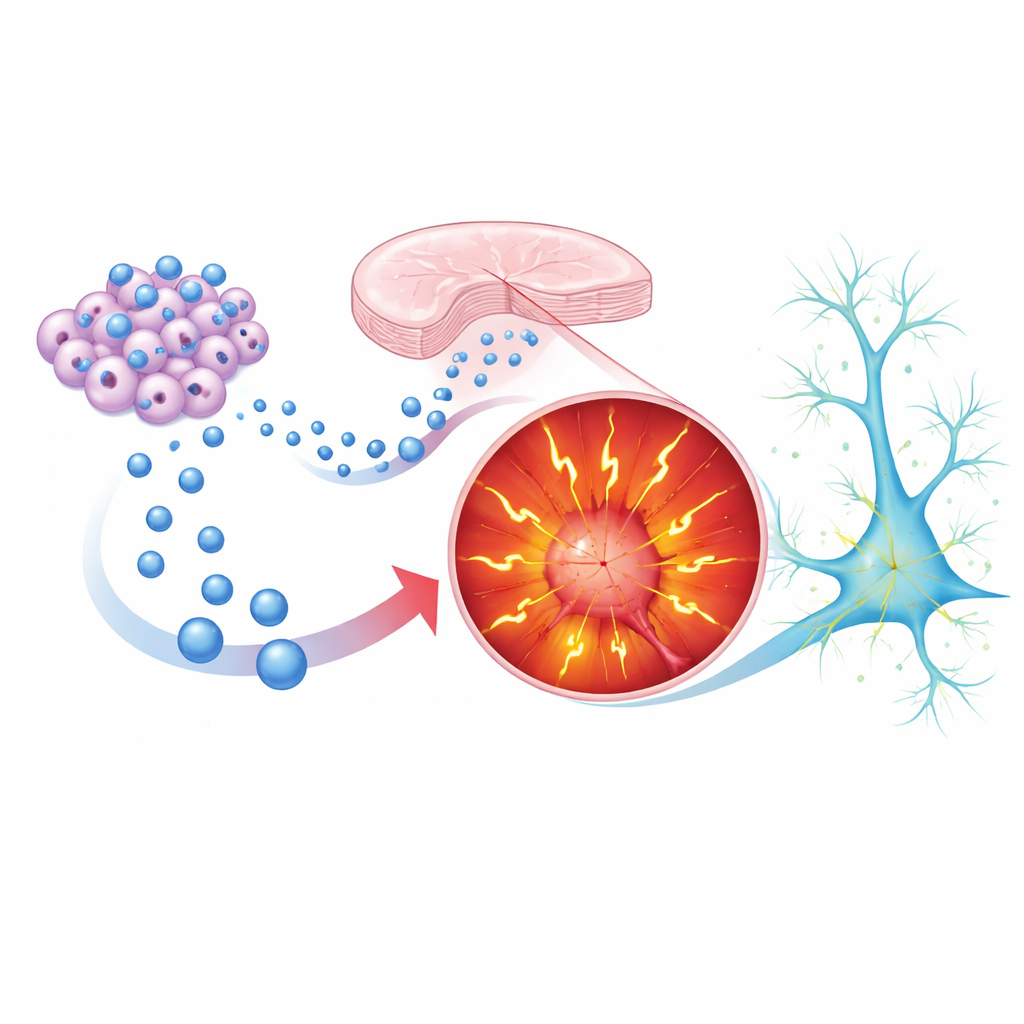
从神经元培养皿到活体行为
为了解这些影响是否超出实验室培养皿,研究者转向Shank3B基因敲除小鼠,这些小鼠表现出类自闭症特征。缺失Shank3的雄性小鼠在对其他小鼠及异性个体的兴趣方面表现正常,但在一项更细微的任务上存在困难:区分一只受压力的小鼠和一只平静的小鼠,这可作为识别他人情绪状态的粗略替代。科学家们通过鼻内给药的方式(从早期婴幼期至幼年期),将来自健康诱导多能干细胞的囊泡不侵入性地递送给小鼠——这种途径已经在脑部疗法中被探索。成年期时,接受治疗的敲除小鼠在情绪识别测试中恢复了清晰的偏好模式,而总体活动量保持不变。这表明干细胞囊泡有助于调整特定的社交处理回路,而不是简单地使动物更活跃或更警觉。
这对未来治疗可能意味着什么
总体而言,研究将细胞外囊泡描绘为双刃信使:来源于SHANK3缺失神经元的囊泡可将高兴奋性特征传播给健康细胞,但来自经过精心选择的干细胞的囊泡则能抑制这种过度活动并在小鼠中挽救部分行为表现。对家庭和临床医生而言,这项工作尚未直接转化为现成的疗法,但它指向了未来的一种可能性:定制的囊泡、携带保护性货物,或能温和地将发育中脑回路重新引导回平衡轨道。由于这些囊泡可在无需手术的情况下递送并能由干细胞规模化生产,它们为针对自闭症及相关神经发育疾病的有针对性、侵入性更低的干预提供了一个有前景的路径。
引用: Choudhary, A., Rosh, I., Hussein, Y. et al. Extracellular vesicles from stem cells rescue cellular phenotypes and behavioral deficits in SHANK3-associated ASD neuronal and mouse models. Cell Death Dis 17, 244 (2026). https://doi.org/10.1038/s41419-026-08474-x
关键词: 自闭症, SHANK3, 细胞外囊泡, 干细胞疗法, 神经发育