Clear Sky Science · zh
集落刺激因子1受体抑制对视网膜脱离中的光感受器具有神经保护作用
这项研究为何与视力相关
视网膜脱离是一种急症,即便手术成功复位视网膜,也可能造成永久性视力丧失。许多持续性损伤来自机体自身的免疫“清理队”,这些细胞在试图清除病变时也可能伤害感光细胞。该小鼠研究探讨通过调低一个关键免疫开关——CSF1R,是否能保护这些脆弱的光感受器,并为保护视力开辟新途径。
眼内的清理队及其可能的反效果
当视网膜从其支持层剥离时,光感受器会突然失去氧气和营养供应。大量细胞发生死亡,组织释放出求救信号。视网膜内的驻留免疫细胞,即小胶质细胞,会改变形态、向损伤处迁移并增强吞噬碎片的活性。与此同时,来自血液的免疫细胞,包括不同类型的单核细胞,会涌入视网膜。它们共同尝试清除死亡细胞并启动修复。但这种有益反应也可能过度,导致额外的炎症,进而杀死仍然可存活的光感受器并加重视力丧失。
一种针对共同免疫开关的药物
驻留小胶质细胞和入侵的单核细胞都依赖同一表面受体CSF1R来维持存活和功能。研究人员使用PLX5622(一种口服抑制剂)阻断CSF1R,探究干预该开关如何改变视网膜脱离时的免疫行为。他们首先描绘了其在血液和视网膜中的影响。在循环系统中,短期治疗并未改变单核细胞总数,但重新平衡了其亚群:促炎的“经典”单核细胞增加,而巡逻型“非经典”单核细胞减少。在眼内,PLX5622 有效耗竭了视网膜小胶质细胞,并改变了进入受损视网膜的血源性免疫细胞数量及其形态和行为。
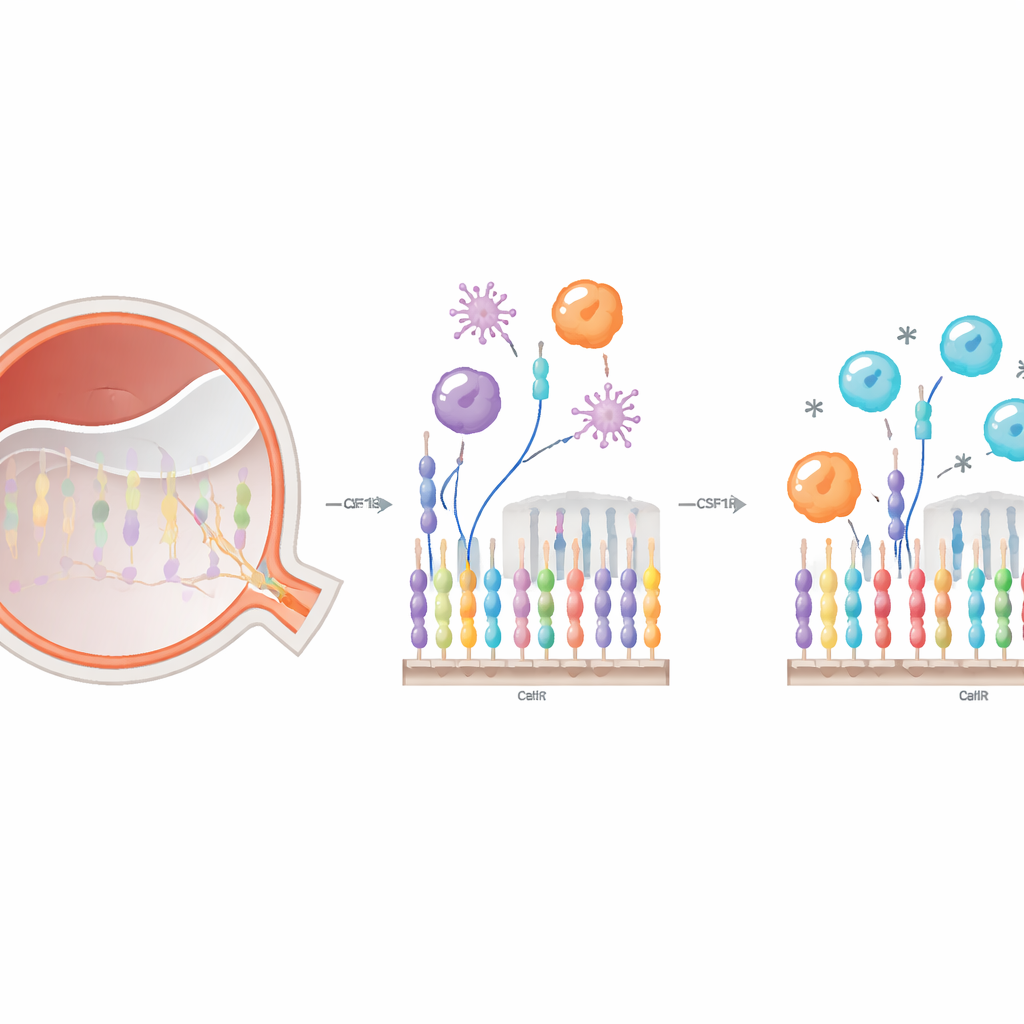
用颜色标签追踪局部与入侵细胞
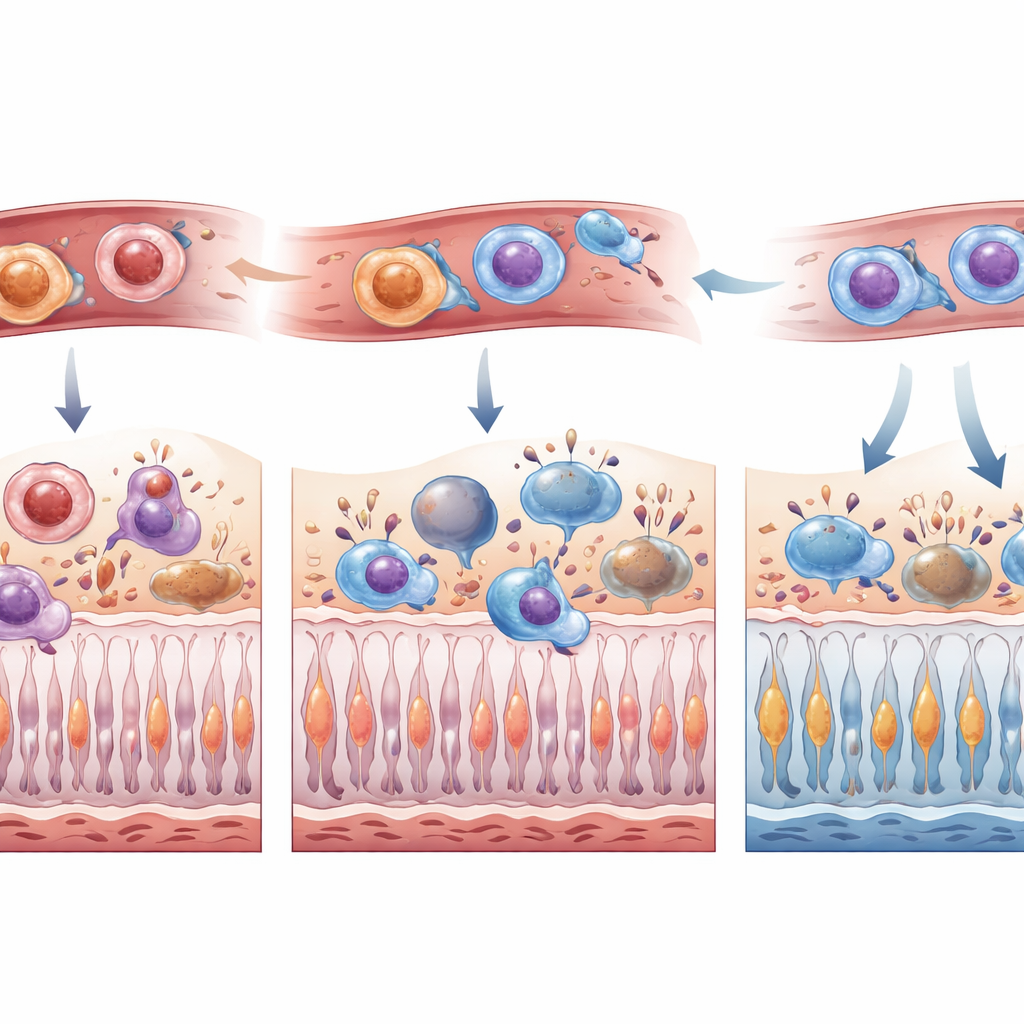
由于小胶质细胞和浸润的单核细胞进入视网膜后可能外形相似,研究团队创建了一种双标记小鼠系统:驻留小胶质细胞发出一种颜色,骨髓来源细胞发出另一种颜色。在诱导可控的视网膜脱离后,他们在一周内追踪这些细胞的迁移与变化。未处理时,小胶质细胞主要在上层视网膜聚集,而骨髓来源细胞则大量进入亚视网膜间隙,经常呈现出变形虫样、高吞噬性的形态。CSF1R 抑制下,小胶质细胞在各层早期明显减少,进入视网膜的骨髓来源细胞(尤其是变形虫样细胞)在受伤后最初几天也较少。到第七天,入侵细胞的潮水在很大程度上赶上了,表明CSF1R 阻断更多是延迟而非永久阻止它们的到达。
改变免疫平衡如何保护光感受器
为了解这些免疫变化对视力的意义,研究人员在多个时间点统计了死亡和存活的光感受器。脱离后的早期数小时内,服用 PLX5622 的动物死亡光感受器更少、存活更多。一周时,无论是短期预处理还是持续用药,都能保留光感受器层的厚度——这一结构学指标反映了细胞存活——并减少亚视网膜间隙中的免疫细胞存在。详细的免疫谱分析显示,尽管整体浸润性白细胞数量下降,但在 CSF1R 抑制下进入视网膜的细胞往往表现出更强的炎性特征。作者认为,这种组合——细胞更少但更倾向于迅速清除碎片——可能加快对死亡光感受器的安全清除,同时保护仍健康的邻近细胞。
对未来治疗的可能意义
这项工作表明,全身性的 CSF1R 抑制剂可以重塑视网膜脱离时的局部和循环免疫反应,并且有些出人意料地显示:更为炎性的但规模更小的“清理队”反而能保护视力。通过暂时耗竭小胶质细胞、延迟首波血源性细胞涌入并调整单核细胞亚型,PLX5622 创造了一个时间窗口,在此期间早期免疫驱动的损伤减少,更多光感受器得以存活。尽管该研究在小鼠中进行,不同眼病中有益与有害炎症的平衡会有所差异,但这些发现支持将 CSF1R 抑制作为设计用于微调免疫反应并在视网膜损伤后保护视力的药物的有希望起点。
引用: Pastor-Puente, S., Jung, R., Gonzalez-Buendia, L. et al. Colony-stimulating factor 1 receptor inhibition is neuroprotective to photoreceptors in retinal detachment. Cell Death Dis 17, 264 (2026). https://doi.org/10.1038/s41419-026-08470-1
关键词: 视网膜脱离, 小胶质细胞, 光感受器存活, 神经炎症, CSF1R 抑制