Clear Sky Science · zh
重塑黑色素瘤细胞命运:TRPM8 调节剂诱导凋亡并增强 NK 细胞细胞毒性
为何把“冷觉传感器”变成对抗皮肤癌的武器很重要
黑色素瘤是一种危险的皮肤癌,常能学会躲避药物和免疫系统。这项研究探讨了黑色素瘤细胞的一个意想不到的弱点:一种名为 TRPM8 的蛋白,最为人熟知的是作为让神经细胞感受冷或薄荷脑的传感器。研究人员表明,精心设计的能抑制 TRPM8 的药物可以促使黑色素瘤细胞自我毁灭,同时也让它们更容易被自然杀伤(NK)细胞识别和清除。这种双重作用指向一种治疗顽固晚期黑色素瘤的新途径。
黑色素瘤细胞上的隐秘开关
通过挖掘大型癌症数据库并在实验室中检查来源于患者的黑色素瘤细胞,研究团队发现 TRPM8 在转移性黑色素瘤中远比正常皮肤(包括健康黑素细胞和真皮成纤维细胞)丰度高。通过成像,他们显示 TRPM8 同时位于细胞表面和内膜,这使其处于能影响细胞行为的关键位置。当他们应用一组新的针对 TRPM8 的分子时,有两种化合物(标为 4 和 9)始终突出:它们随着时间显著降低黑色素瘤细胞的存活率,而对正常皮肤细胞基本无害。遗传学实验证实,去除 TRPM8 后这些药物失去杀伤力,而增加 TRPM8 则使黑色素瘤细胞更敏感,证明该效应依赖于这一特定通道。 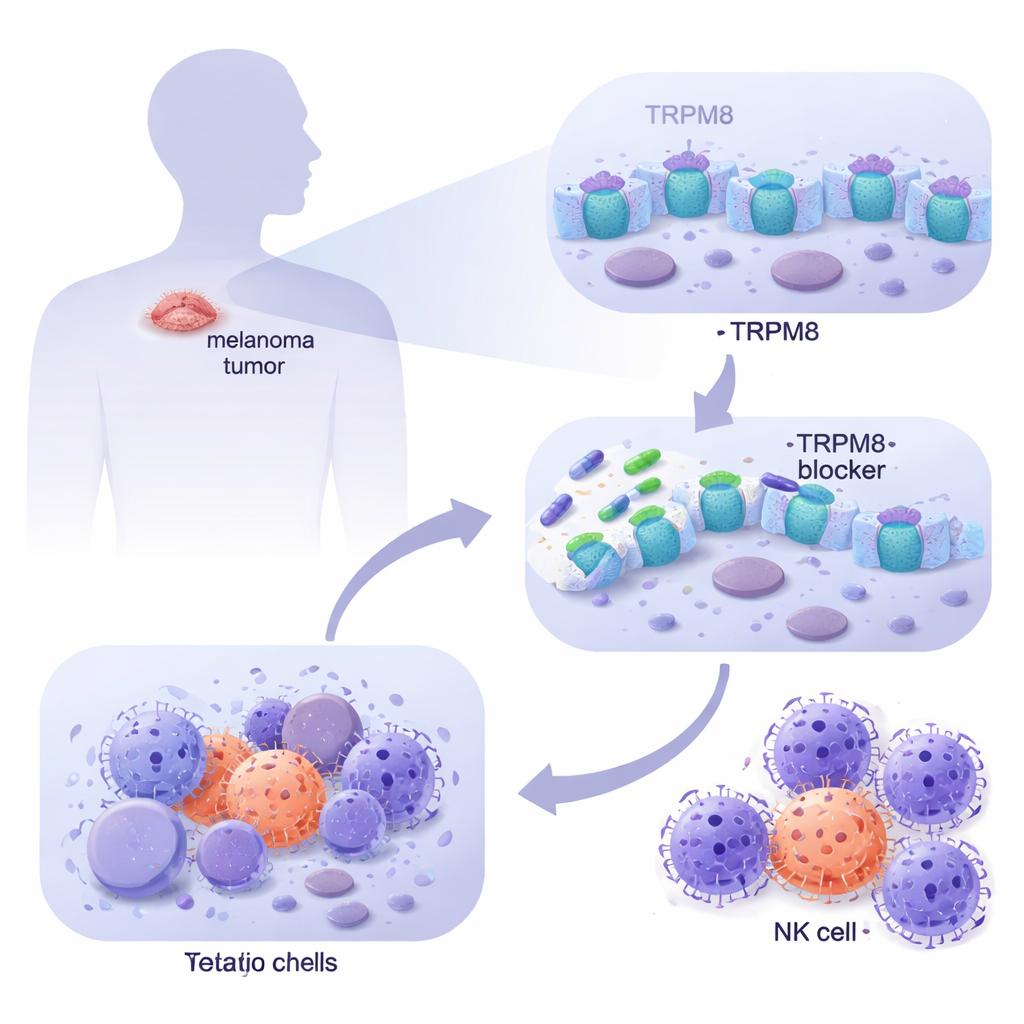
将癌细胞推入能量危机
与薄荷脑等经典 TRPM8 激活剂诱导细胞内钙激增不同,这些新的抑制剂并未引发钙水平变化。相反,它们在黑色素瘤细胞内引发了一波氧化应激。这些化合物快速增加了活性氧,尤其在线粒体这一细胞的能量工厂中。这种氧化爆发造成线粒体膜电位丧失、碎裂并泄漏细胞色素 c,这是启动细胞内部“自杀”程序的重要步骤。清除这些活性分子的抗氧化剂在很大程度上拯救了细胞,表明氧化还原失衡不是副作用而是导致细胞死亡的核心机制。下游的经典死亡标志如半胱天冬酶-3 激活和 PARP 裂解证实,细胞经历的是程序性凋亡而非随机的损伤。
解除生存信号并唤醒守护者
氧化冲击引发了更广泛的应激反应。药物激活了 ATM —— 一个 DNA 损伤感知器,并导致著名肿瘤抑制蛋白 p53 的积累与激活,p53 决定受损细胞是修复还是走向死亡。与此同时,这些化合物削弱了黑色素瘤的一条主要生存通路:PI3K–AKT 途径。通常,TRPM8 与 PI3K 组分发生物理相互作用,以帮助维持 AKT 的活性和促生长状态。处理后,这种相互作用被破坏,AKT 活性下降,使细胞更倾向于死亡。重要的是,这些变化在黑色素瘤细胞中明显,而在非癌细胞中并不显著,提示存在一个治疗窗口,可以在打击肿瘤的同时尽量保护健康组织。
让肿瘤对免疫“打手”更易察觉
黑色素瘤的危险性还在于其逃避免疫监视的能力。因此,研究人员询问在较低剂量 TRPM8 抑制剂长期处理下存活的肿瘤细胞会怎样。他们发现这些残存细胞开始在表面更多地展示一种名为 ULBP1 的标记,类似于被 NKG2D 受体识别的求救信号。其他相关标记未见变化,表明这是选择性的效应。在更好模拟真实肿瘤的三维黑色素瘤球体中,TRPM8 抑制剂的预处理不仅缩小了结构并增加细胞死亡,还使它们对 NK 细胞攻击更脆弱。当用抗体阻断 ULBP1 或 NKG2D 时,这种额外的杀伤大多消失,表明增强的免疫清除通过肿瘤与 NK 细胞之间这一路线性交流实现。 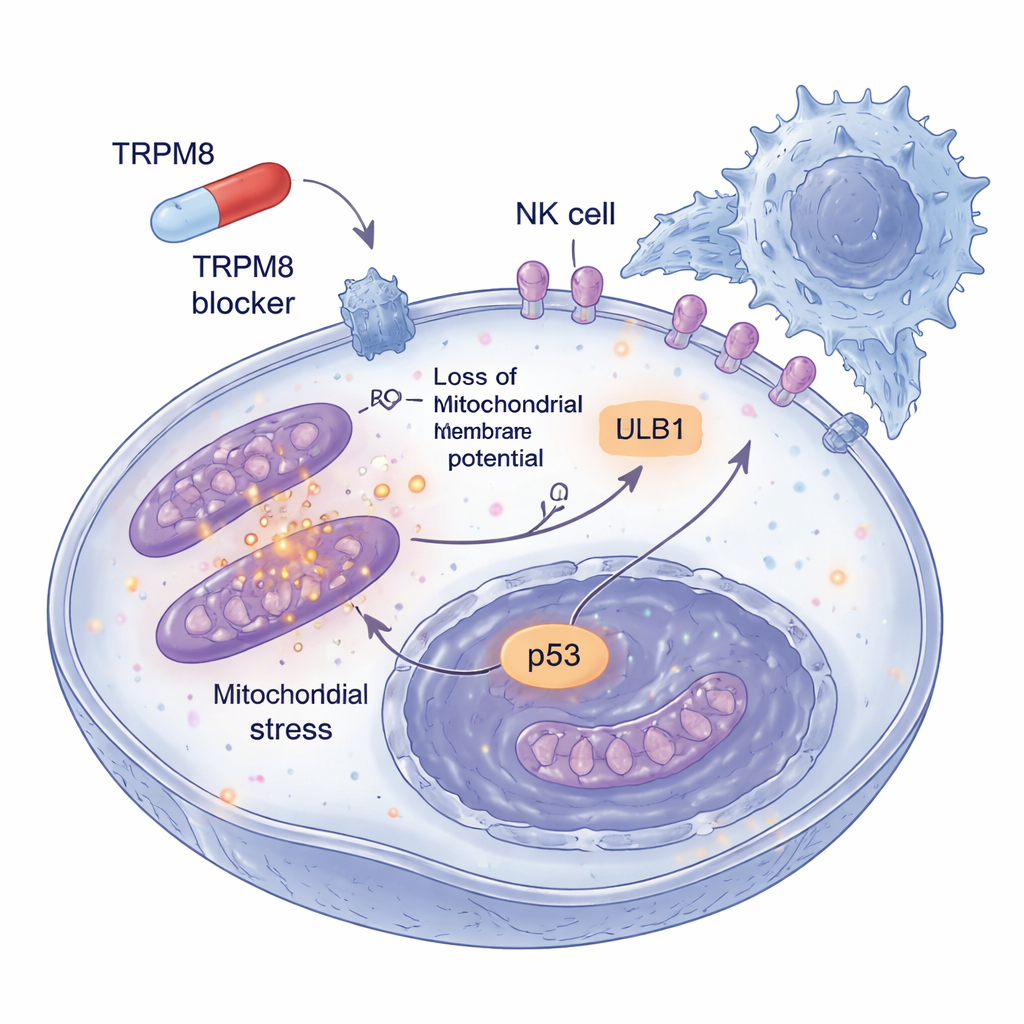
这对未来黑色素瘤治疗可能意味着什么
简单来说,阻断 TRPM8“冷觉传感器”将其转变为一个治疗杠杆:它使黑色素瘤细胞陷入致命的线粒体和 DNA 危机,同时标记它们以便被 NK 细胞清除。由于这些药物对正常皮肤细胞相对无害且不会损伤 NK 细胞本身,它们为新疗法提供了有希望的基础。作者建议将 TRPM8 抑制剂与现有免疫疗法联合使用,以双重策略攻击晚期、耐药的黑色素瘤:直接杀死肿瘤细胞并让残存细胞更容易被免疫系统找到并摧毁。
引用: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
关键词: 黑色素瘤, TRPM8, 线粒体, 氧化应激, 自然杀伤细胞