Clear Sky Science · zh
乳酰化驱动的 TRIM29 通过 hnRNPA1 介导的 Wnt/β-连环蛋白途径在胃癌中诱导侵袭性行为和淋巴结转移
这项研究为何重要
胃癌是全球致死率很高的癌症之一,主要因为它常在早期就扩散到附近的淋巴结,使手术治愈困难。本研究揭示了一种与肿瘤代谢相关的化学修饰如何激活名为 TRIM29 的蛋白,进而帮助癌细胞侵入周围组织、促进新淋巴管形成并抵抗化疗。理解这一连锁反应为阻止或减缓胃癌扩散提供了新的思路。
胃肿瘤中的危险伙伴关系
研究者首先比较了 100 例患者的胃癌样本与邻近健康组织,并结合大型公开基因数据库,发现此前与免疫调节和其他癌症相关的蛋白 TRIM29 在肿瘤细胞中普遍高表达。肿瘤中 TRIM29 水平较高的患者更容易出现淋巴结和血管内癌细胞侵袭,且总体生存率更差。这些模式表明 TRIM29 不仅存在于肿瘤中,而且积极参与促进胃癌更具侵袭性的行为。
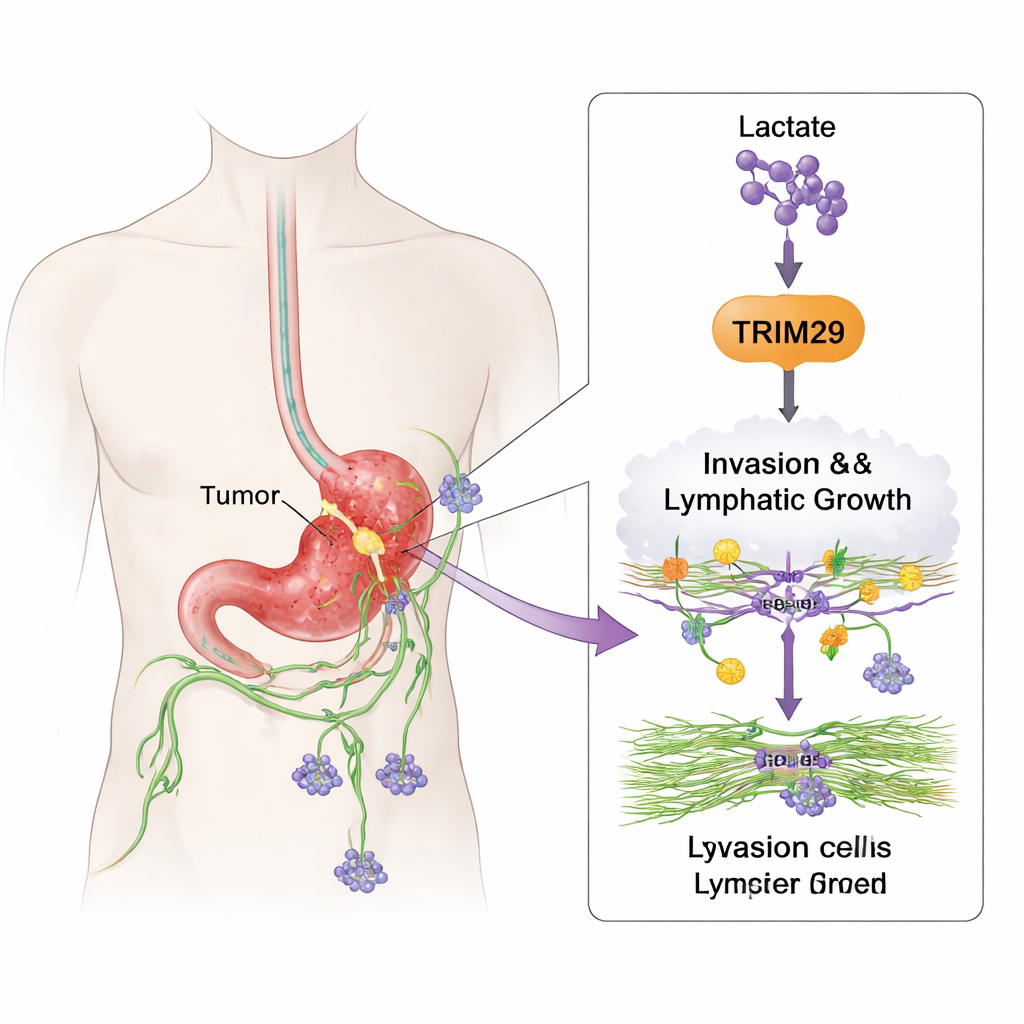
癌细胞如何学会迁移
为了解 TRIM29 的实际作用,团队在胃癌细胞系中改变了其表达水平。降低 TRIM29 后,细胞的迁移能力明显下降,穿透模拟体内组织的三维凝胶的能力也减弱。提高 TRIM29 则产生相反效果,使细胞更具侵袭性。研究者还考察了淋巴管内皮细胞——构成淋巴管内膜的细胞。富含 TRIM29 的癌细胞促使这些血管细胞萌发并形成管状结构,显示出新淋巴管生成的特征。在小鼠模型中,高表达 TRIM29 的肿瘤产生了更多的肝转移和淋巴结转移,而敲低 TRIM29 的肿瘤扩散减少、形成的淋巴管也更少。
分子接力:保护一个关键调控因子
进一步研究表明,TRIM29 能与另一种蛋白 hnRNPA1 直接结合,后者已知参与基因加工并与癌症转移相关。通常 hnRNPA1 会被另一种蛋白酶 ZFP91 标记并通过细胞的降解系统清除。TRIM29 通过与 hnRNPA1 竞争结合,干扰了这一过程。当 TRIM29 丰富时,它保护 hnRNPA1 免于被标记和降解,导致 hnRNPA1 在癌细胞内更稳定并积累,进而触发一系列信号最终激活 Wnt/β-连环蛋白通路——该通路是公认的肿瘤生长与迁移驱动因子。这一过程又促进了 VEGF-C 的产生,VEGF-C 可刺激新淋巴管生成,为癌细胞提供更多“逃逸”通道。
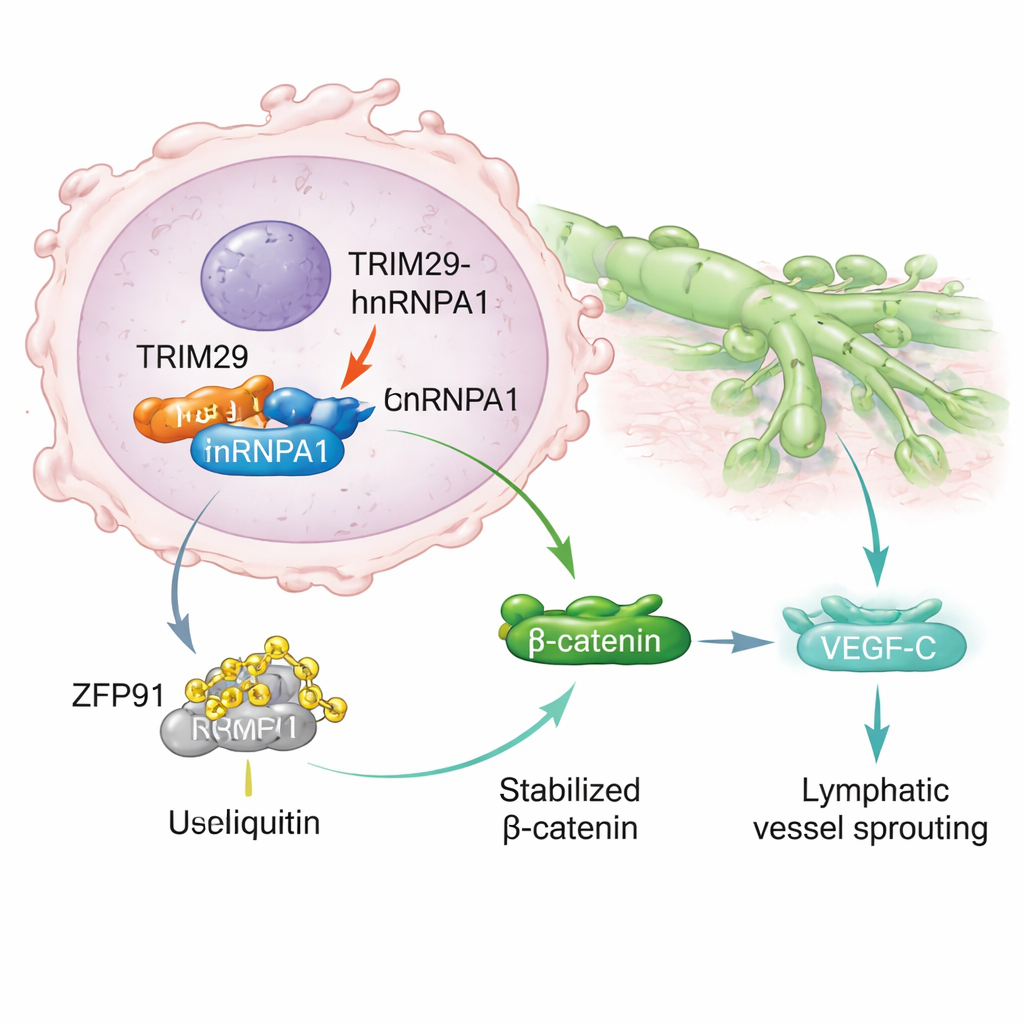
用乳酸为癌症加油
该研究还将这种侵袭性行为与肿瘤的糖代谢联系起来。快速增殖的肿瘤常依赖一种产生大量乳酸的代谢方式,乳酸曾被视为仅有的代谢废物。本文作者表明,乳酸可对帮助包装 DNA 的组蛋白发生化学修饰,尤其是在 H3K9 位点上的“乳酰化”。这种乳酰化像开关一样激活 TRIM29 基因,提升其表达。当研究者用代谢药物降低乳酸产生时,TRIM29 水平下降;反之提高乳酸时,TRIM29 上升。患者的胃癌组织显示出较高的 H3K9 乳酰化水平,这与 TRIM29 增高、更多的淋巴结转移和较差的生存期相关。本质上,肿瘤的代谢改变帮助书写了更具侵袭性的基因程序。
提高化疗效果的新途径
淋巴管不仅运载癌细胞,也可将化疗药物从肿瘤部位排走。研究者在小鼠体内使用来源于患者的肿瘤移植模型,测试抑制 TRIM29 和抑制淋巴管生成是否能增强 5‑氟尿嘧啶(5‑FU,一种常用的胃癌药物)的疗效。抑制 TRIM29 或阻断淋巴管生成均使 5‑FU 在缩小肿瘤和降低细胞分裂方面更为有效。两种策略联合应用产生了最强的反应,提示在晚期疾病中这可能成为克服部分药物耐受的潜在方法。
对患者意味着什么
这项工作描绘了一幅循序渐进的图景:胃肿瘤产生过量乳酸,激活 TRIM29;TRIM29 保护 hnRNPA1,稳定生长通路,并增加淋巴管形成与淋巴结转移。从临床角度看,高水平的 TRIM29 及相关的乳酰化标记可识别出具有更高侵袭性风险的患者。未来,抑制乳酸信号、阻断 TRIM29 或防止淋巴管生成的药物,若与现有化疗联合使用,可能有助于阻止胃癌扩散并提高治疗效果。
引用: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
关键词: 胃癌转移, TRIM29, 乳酸与乳酰化, 淋巴管生成, Wnt β-连环蛋白通路