Clear Sky Science · zh
KIF20A通过抑制TRIM21介导的DHX9泛素化来增强SOX2稳定性,从而促进口腔鳞状细胞癌干性和耐铁死亡性
这项研究为何对口腔癌患者重要
口腔鳞状细胞癌是常见的口腔癌类型,常出现复发并对治疗产生耐受性。手术、化疗和放疗失败的许多原因可归结于一小群顽固的“癌症干细胞”,它们能够重新生长肿瘤并抵抗细胞死亡。本研究揭示了一个关键的分子回路,帮助这些细胞存活并抵抗一种新型细胞死亡方式——铁死亡,同时指出了一种可能使常规化疗更有效的药物策略。
口腔肿瘤中的一个隐藏驱动因子
研究人员首先比较了口腔癌患者的肿瘤样本与邻近的健康组织,发现一种名为KIF20A的蛋白在癌细胞中持续显著升高。在更大的患者数据集中,肿瘤中KIF20A表达较高的患者生存时间往往较短,提示该蛋白与侵袭性疾病有关。 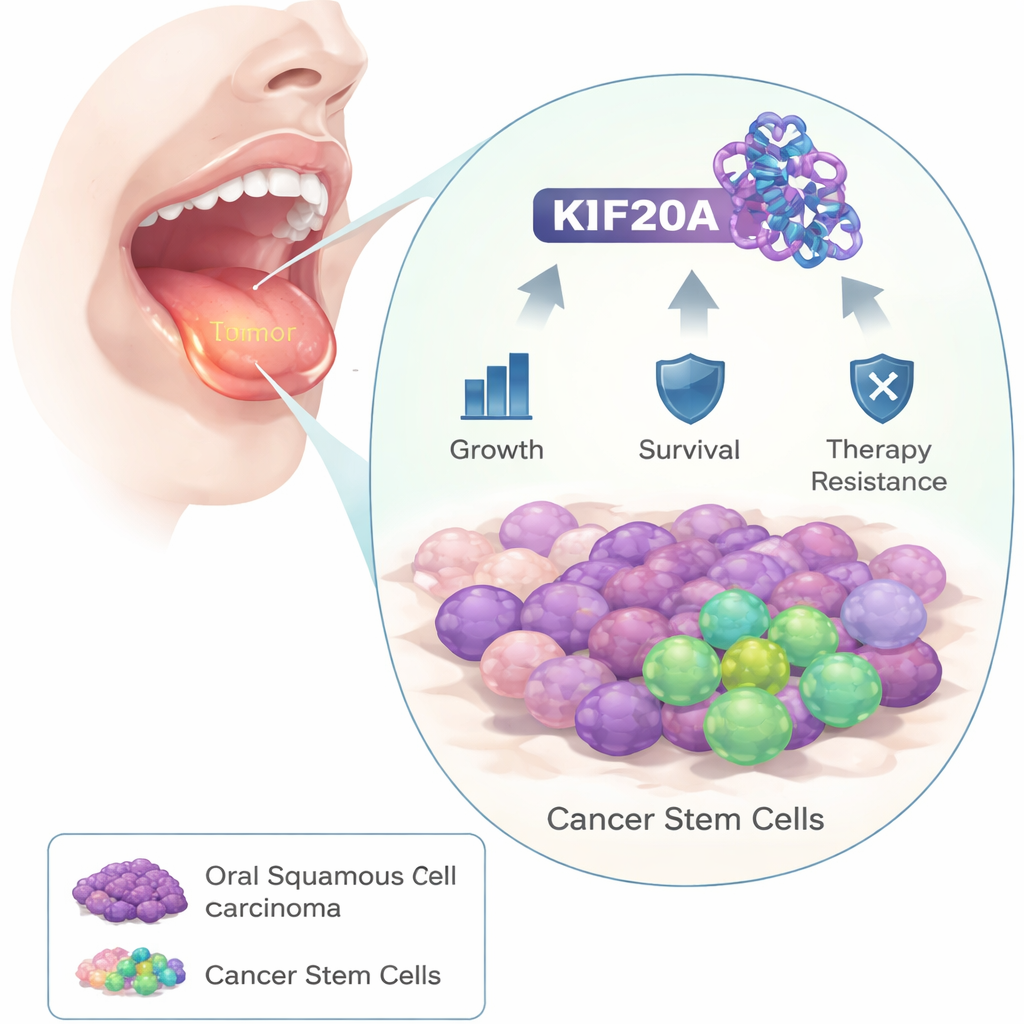
KIF20A如何保护一个关键的RNA调节蛋白
为弄清KIF20A的具体功能,团队使用蛋白质互作图谱方法在癌细胞内寻找其伙伴蛋白。一个突出的伙伴是DHX9,这是一种参与RNA管理并影响某些RNA稳定性的蛋白。研究人员发现,KIF20A与DHX9结合并阻止另一种E3连接酶TRIM21对其进行标记——TRIM21通常通过将“泛素”链加到DHX9上,将其送去细胞的蛋白降解通路。通过阻断这一标记,KIF20A减缓了DHX9的降解并增加了其水平,尤其是在细胞质中,使其能作用于特定的RNA靶点。
从RNA稳定性到癌症干性与铁死亡耐受
DHX9更稳定时,另一个关键因子浮出水面:SOX2,这是一种帮助细胞保持干性并抵抗治疗的主控基因。研究显示DHX9保护SOX2的mRNA不被降解,从而产生更多SOX2蛋白。在口腔癌细胞中,KIF20A升高导致DHX9和SOX2增多,培养中肿瘤球形成增加,表达干细胞标志物的细胞比例上升——这些都是“癌症干性”增强的迹象。KIF20A还使细胞对铁死亡(一种与铁和脂质代谢相关的细胞死亡类型,目前被探索用于杀死耐药癌细胞)更不敏感。当关闭KIF20A时,小鼠模型中的肿瘤更容易缩小,铁死亡标志上升,表明肿瘤失去了这种保护措施。
一个具有可药物化弱点的分子回路
综上,作者提出了一个KIF20A–DHX9–SOX2轴:KIF20A稳定DHX9,DHX9稳定SOX2 mRNA,而SOX2反过来维持癌症干细胞并阻断铁死亡。该回路还与PI3K–AKT通路相互作用,这是许多癌症中的主要生长与存活通路。 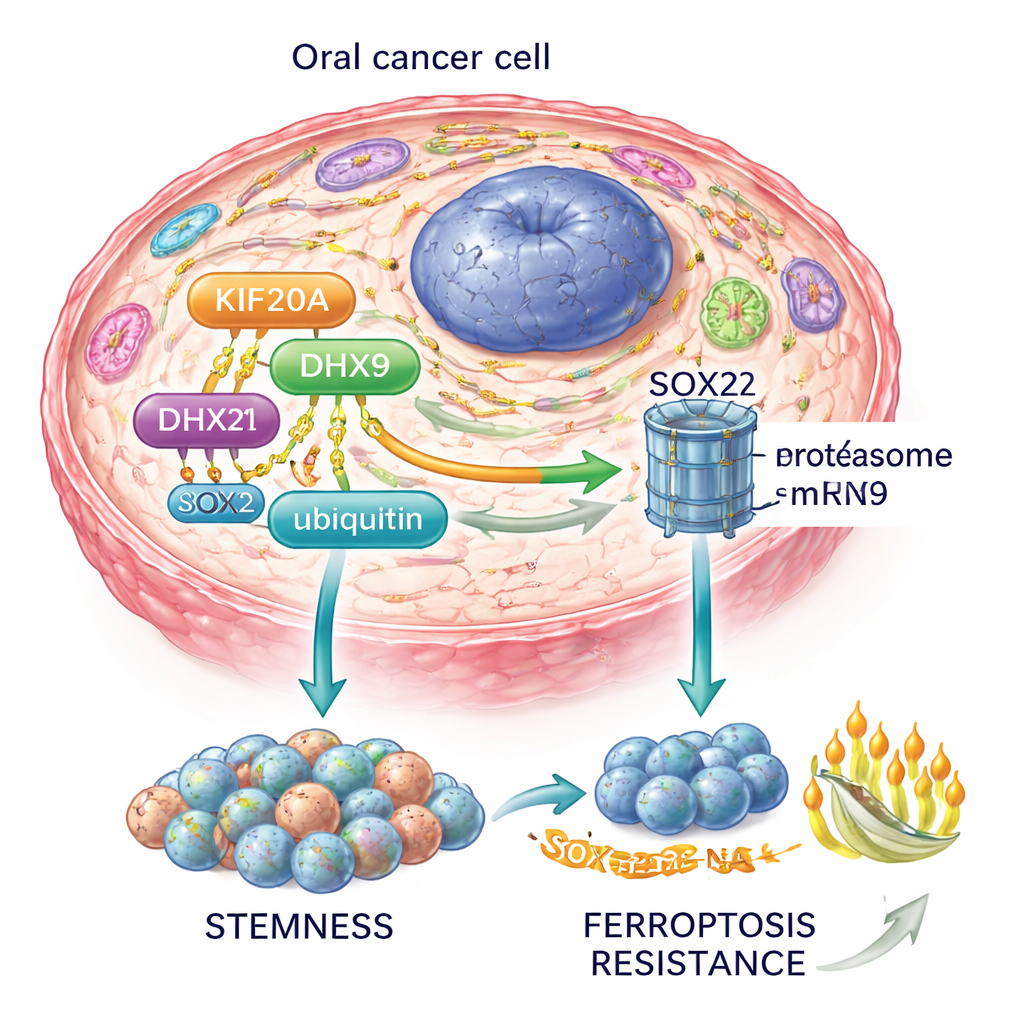
削弱耐药肿瘤的候选药物
为推进治疗转化,团队在大型药物—基因数据库中筛选出可逆转KIF20A相关基因模式的化合物,鉴定出ENMD-2076,这是一种口服多靶点激酶抑制剂,已在其他癌种中试验。在KIF20A高表达的口腔癌细胞中,ENMD-2076降低了KIF20A、DHX9和SOX2的水平,抑制了与干性相关的信号并减缓细胞生长。与标准化疗药顺铂联合使用时,ENMD-2076在细胞培养和小鼠肿瘤模型中产生了比单药更强的抗癌效应,且未观察到明显的额外毒性。
对未来治疗的意义
对非专业读者来说,结论是:这项研究揭示了如何通过一个过度活跃的蛋白KIF20A,帮助口腔肿瘤维持一小群“种子”细胞的存活并使其免受一种有前景的细胞死亡方式的侵害。通过描绘从KIF20A到DHX9再到SOX2的链条,研究者指出了新的药物靶点,并展示了一种已有的实验性药物ENMD-2076能够削弱该轴并在模型中增强顺铂疗效。虽然仍需更多研究以评估安全性并在患者中证实益处,但这些发现支持未来通过阻断该回路来帮助预防复发并克服口腔癌药物耐受性的设想。
引用: Zhang, Z., Li, Y., Hu, J. et al. KIF20A inhibits TRIM21-dependent ubiquitination of DHX9 to boost SOX2 stability, enhancing OSCC stemness and ferroptosis resistance. Cell Death Dis 17, 218 (2026). https://doi.org/10.1038/s41419-026-08467-w
关键词: 口腔鳞状细胞癌, 癌症干细胞, 铁死亡, KIF20A, SOX2