Clear Sky Science · zh
硒代蛋氨酸作为双重机制的铁死亡抑制剂:超越穿硫代谢的硒供应驱动GPX4生物合成与独立于GPX4活性的还原能力介导的活性氧清除
为何保护细胞免于“像生锈一样”的死亡很重要
我们体内的细胞可以通过多种方式死亡,其中一种新发现且引人关注的方式称为铁死亡——一种由铁驱动、对细胞膜造成“生锈式”损伤的过程。这一机制现已与多种疾病相关,涵盖从肾损伤到神经退行性疾病等。微量元素硒(很多人通过膳食补充剂了解它)被发现对阻止这种危险的细胞死亡形式至关重要。本研究探讨了一种常见的含硒氨基酸硒代蛋氨酸如何通过不止一种,而是两种不同的保护策略来抵御铁死亡。
在大规模药物筛选中发现的新防御者
为了寻找能阻断铁死亡的小分子,研究者对成千上万种来自FDA批准药物和天然产物的化合物进行了筛选。他们使用一种名为RSL3的化学物质在人体癌细胞系中诱导铁死亡,然后监测细胞死亡和细胞膜中被氧化损伤的脂质积累。在所有候选物中,硒代蛋氨酸表现出强有力的保护作用:它在不同细胞类型和两种主要的铁死亡模型中都能减少脂质损伤与细胞死亡——一种由直接抑制GPX4(使用RSL3)驱动,另一种由缺乏胱氨酸(抗氧化剂谷胱甘肽的构件)引起。这些结果将硒代蛋氨酸定位为一种广谱且稳健的铁死亡抑制剂。 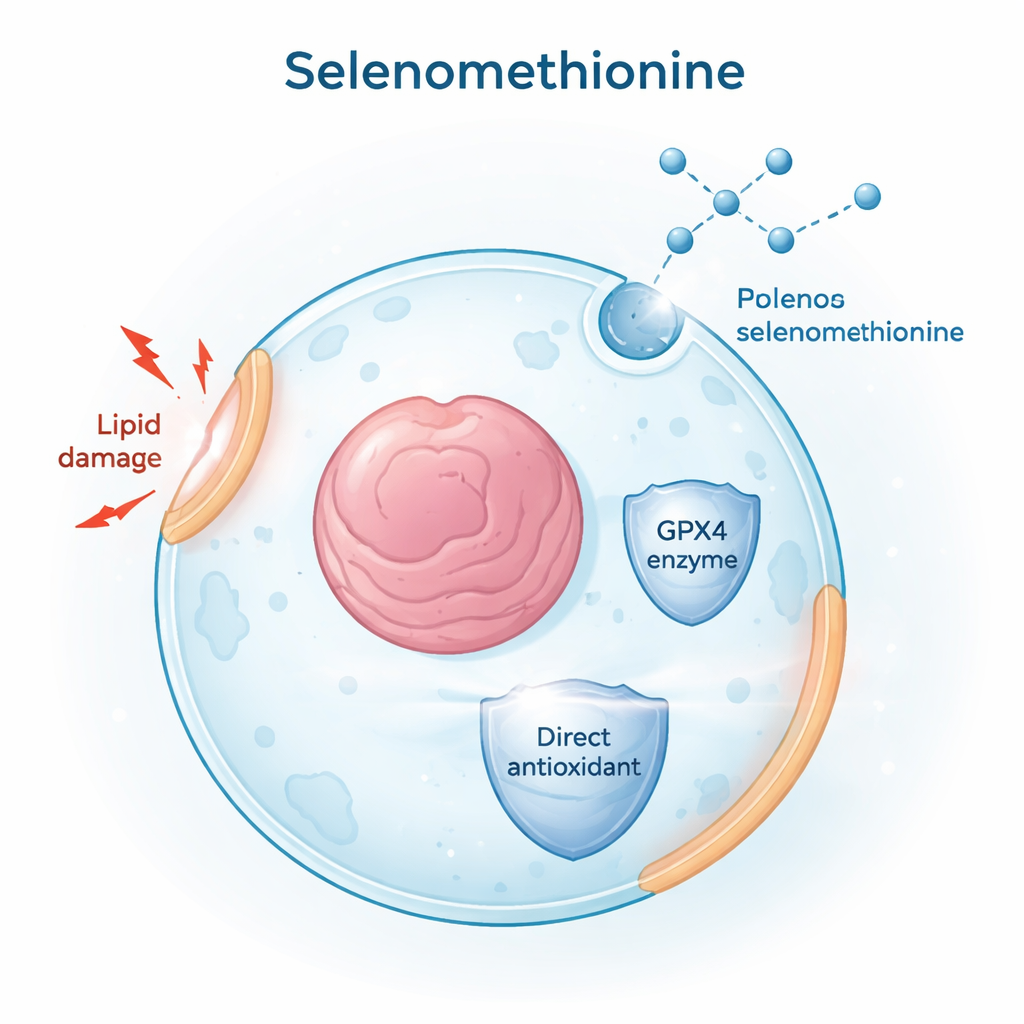
为关键保护酶提供硒供应
细胞中对抗铁死亡的核心防线之一是一种依赖硒才能发挥功能的酶GPX4。研究团队旨在确定硒代蛋氨酸是否仅仅为这一通路提供原料,还是还有额外作用。他们追踪了来自硒代蛋氨酸的硒如何被转换为可用于合成GPX4的形式,即便一种通常的途径——穿硫代谢途径——受损或被阻断。通过对这些硫—硒代谢通路中酶的基因敲低和化学抑制,他们发现硒代蛋氨酸仍能提升GPX4水平并保护细胞。这表明细胞可以利用多条代谢途径从硒代蛋氨酸中提取硒并维持GPX4的合成,即使在经典通路较弱的组织中也是如此。
不依赖常规酶的保护作用
令人惊讶的是,当研究者使用CRISPR基因编辑完全敲除细胞中的GPX4后,硒代蛋氨酸仍继续抵御铁死亡。它仍然能降低膜脂质损伤和细胞死亡,表明GPX4并非全部保护机制。后续实验暗示,这种保护的一部分涉及硒代蛋氨酸被掺入新合成的蛋白质中,但这仅是部分效应。作者随后将注意力转向硒代蛋氨酸本身的化学反应性。他们发现它可以直接中和活性氧(ROS),包括过氧化氢,并被转化为氧化的“亚砜”形式。质谱证实了该产物,并且给予细胞该亚砜形式也能降低铁死亡,暗示细胞能够在一种氧化还原循环中将其再还原回活性硒代蛋氨酸。
从细胞培养到在活体动物中保护肾脏
为了检验这些机制在整体有机体中是否重要,团队使用了顺铂诱导的急性肾损伤小鼠模型——这一状况已知涉及铁死亡。接受顺铂处理的小鼠出现体重下降、肾脏肿胀、肾功能受损以及铁死亡标志物升高。给予硒代蛋氨酸的动物中,这些问题多有改善:体重恢复,肾脏肿胀减轻,血液中的肾功能指标趋于正常,炎症信号下降,脂质损伤的化学标志物减少。肾组织中还显示出更高的GPX4水平和较少的结构性损伤。这些益处与已知的实验性铁死亡抑制剂ferrostatin-1所见的效果相当。 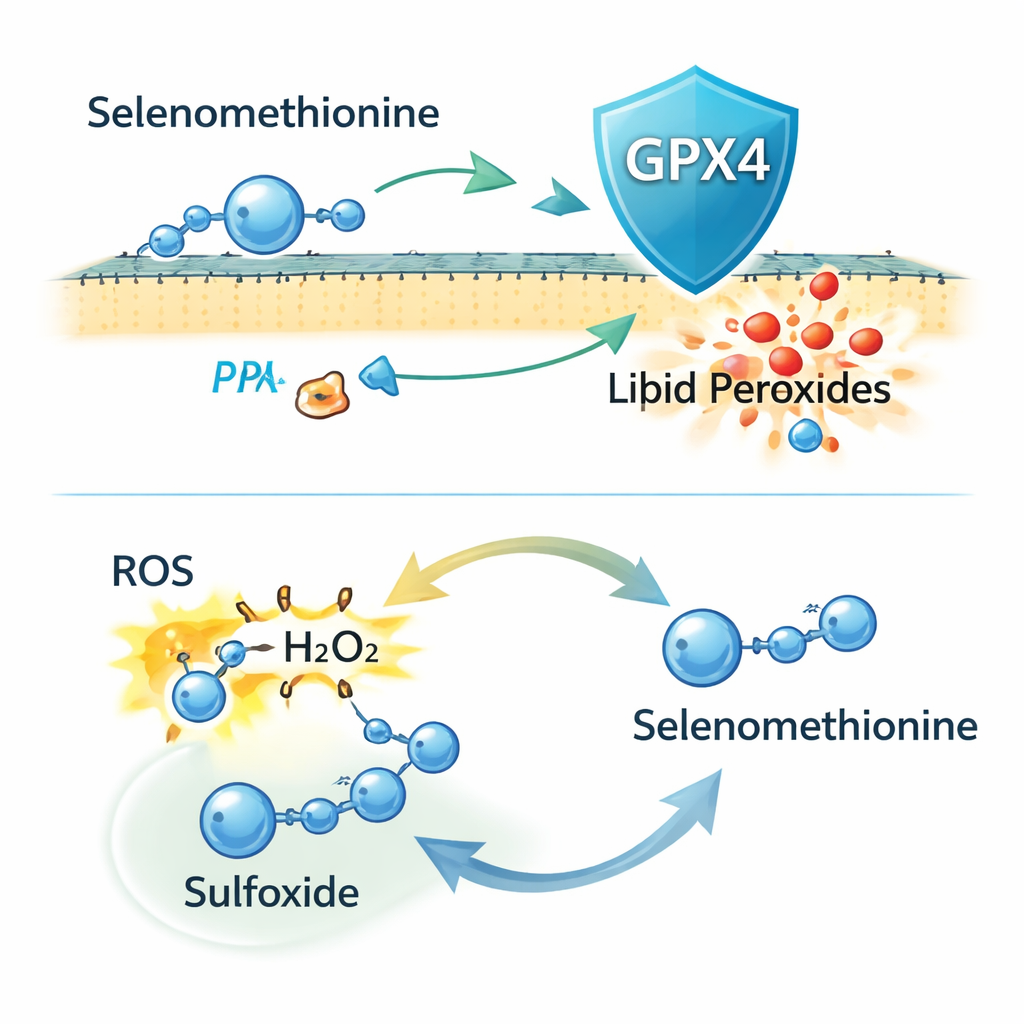
这对未来疗法意味着什么
通俗地说,这项工作表明硒代蛋氨酸像一种双用途灭火器,能对抗一种以铁为燃料的细胞膜“生锈”。一方面,它提供硒,使细胞能合成更多的GPX4这一内部“清道夫”,用于去除受损脂质;另一方面,硒代蛋氨酸自身能够吸收有害氧化物并在细胞内循环再生,提供独立于GPX4的备用保护。综合起来,这些特性使硒代蛋氨酸成为防治以铁死亡为中心的疾病(如药物诱导的肾损伤以及其他由失控氧化应激驱动的状况)的有希望的候选分子。
引用: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
关键词: 铁死亡, 硒, 硒代蛋氨酸, 氧化应激, 急性肾损伤