Clear Sky Science · zh
PDHA1 乙酰化信号抑制铜致死以减弱雄激素拮抗剂在前列腺癌中的疗效
这项研究为何重要
前列腺癌是男性中最常见的癌症之一,许多晚期病例通过阻断雄性激素信号的药物治疗。核心药物依那扎胺(enzalutamide)在初期常有效,但肿瘤往往随后产生耐药而失去疗效。本研究揭示了部分前列腺癌逃避依那扎胺作用的一个令人意外的机制,并表明阻断单一代谢通路即可使肿瘤重新变得敏感,从而为更持久的治疗打开了可能性。
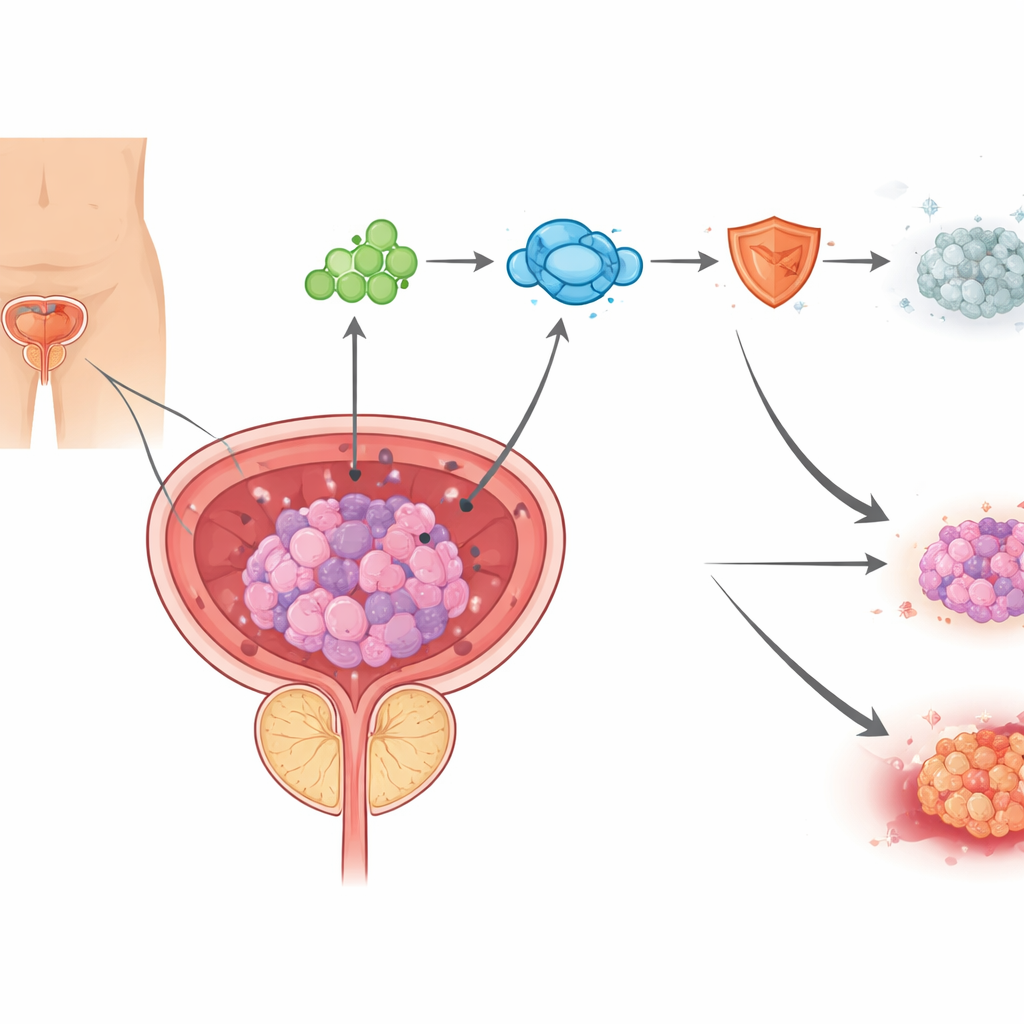
由铜驱动的一种新型细胞死亡
细胞可以通过多种途径死亡,现代癌症研究越来越多地尝试在肿瘤细胞中重新激活这些天然的死亡程序。作者关注一种新近描述的细胞死亡形式——铜致死(cuproptosis),当铜在线粒体内积累时会触发此类死亡。来自接受雄激素阻断治疗的前列腺癌患者样本中,研究组发现铜积累和线粒体损伤的迹象,以及作为铜致死特征的蛋白质改变。在细胞培养中,依那扎胺提高了铜水平并损害线粒体,而一种结合铜的化合物在很大程度上能挽救细胞,这表明依那扎胺部分通过推动细胞进入铜驱动的死亡来杀死前列腺癌细胞。
肿瘤如何削弱铜的毒性
然而并非所有癌细胞都会屈服。通过挖掘多个依那扎胺耐药前列腺肿瘤的数据集并聚焦与铜致死相关的基因,研究者锁定了一个突出蛋白:PDHA1,它是将糖类衍生燃料转化为乙酰辅酶A(细胞关键构件)的核心机器的一部分。耐药肿瘤中PDHA1水平更高,与更差的生存率和更具侵袭性的疾病相关,并且可被依那扎胺本身上调。在实验室实验中,下调PDHA1使癌细胞对依那扎胺和直接诱导铜致死的药物都更为敏感,而提高PDHA1则使其更难被杀死。在小鼠体内,降低PDHA1的肿瘤在依那扎胺治疗下明显缩小,证实该酶在生物体内帮助肿瘤抵抗治疗。
一种代谢与表观遗传的治疗屏障
研究团队随后解析了PDHA1如何构建这一屏障。由于PDHA1参与乙酰辅酶A的生成,他们检测了其是否会改变DNA的包装与读取方式。当PDHA1水平升高时,乙酰辅酶A含量和组蛋白上的“乙酰”化学标记增加,尤其是与基因活性相关的标记。一个重要受益者是SLC7A11,这是一种将半胱氨酸运入细胞以合成谷胱甘肽(主要抗氧化剂)的转运蛋白。PDHA1升高时,细胞产生更多谷胱甘肽;PDHA1降低时,半胱氨酸和谷胱甘肽下调。谷胱甘肽反过来结合并中和铜,减轻触发铜致死的压力。恢复谷胱甘肽或SLC7A11可以逆转PDHA1被抑制时出现的增强铜压力,表明PDHA1–乙酰辅酶A–组蛋白–SLC7A11–谷胱甘肽这一链条使癌细胞清除铜并规避死亡。
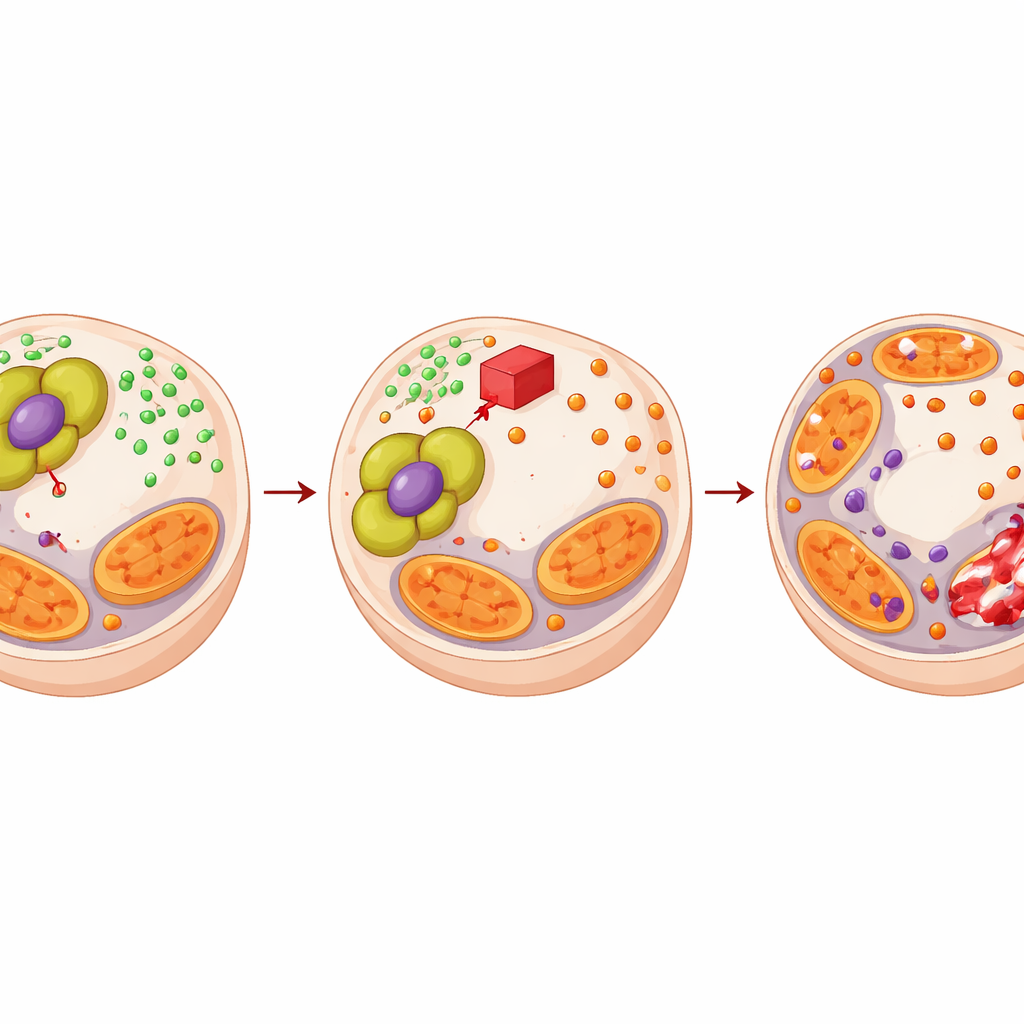
将脆弱点转为治疗策略
既然PDHA1通过强化铜缓冲系统帮助肿瘤抵抗依那扎胺,作者便探讨针对PDHA1的药物是否能扭转局面。他们使用了CPI‑613,这是一种能干扰同一代谢复合体的化合物。CPI‑613单用可在前列腺癌细胞中增加铜压力并损伤线粒体蛋白,但对正常前列腺细胞影响较小。与依那扎胺联合使用时,CPI‑613较单药或任何单独治疗显著抑制癌细胞生长,数学分析证实了真实的协同效应。在小鼠肿瘤模型和来源于患者的肿瘤移植中,这对药物组合产生了更小的肿瘤、更多坏死组织、更少分裂细胞以及更强的铜驱动细胞死亡信号。
对患者意味着什么
综合来看,这些发现表明部分前列腺癌通过重编程代谢以产生更多乙酰辅酶A、改写基因活性并提升谷胱甘肽来逃避依那扎胺,谷胱甘肽吸收有毒铜从而阻断铜致死。通过抑制PDHA1,这一保护性回路可以被拆解,使铜驱动的细胞死亡得以发生并恢复激素阻断疗法的效果。尽管仍需临床试验验证,该研究指向了一个具体且可测试的策略:将依那扎胺与像CPI‑613这样的PDHA1靶向药物联合使用,以克服晚期、难治性前列腺癌的耐药性。
引用: Zhuang, R., Zhou, Q., Cheng, B. et al. PDHA1–acetylation signaling suppresses cuproptosis to attenuate anti-androgen effect in prostate cancer. Cell Death Dis 17, 243 (2026). https://doi.org/10.1038/s41419-026-08462-1
关键词: 前列腺癌, 药物耐药, 铜诱导细胞死亡, 癌症代谢, 表观遗传调控