Clear Sky Science · zh
内皮细胞 IRE1 信号维持血–脑屏障完整性并在创伤性脑损伤后限制神经炎症
为何保护大脑内壁至关重要
头部受到撞击后,即时的损伤只是部分情形。在随后数小时到数天内,大脑会发动强烈的应激和免疫反应,可能在暗中扩大损伤。本研究考察了一种存在于脑血管内皮细胞中的微小应激感知系统,如何在创伤性脑损伤后帮助保持大脑内壁——血–脑屏障——的密闭与平稳。理解这一隐蔽的防御机制,或能为减轻头部外伤后持久残疾指明新的治疗方向。
承受应激的大脑守门人
大脑依赖由内皮细胞形成的专业屏障,这些细胞衬里血管内腔,严格控制血液进入脑组织的物质。创伤性脑损伤(TBI)会破坏血–脑屏障,使炎性分子和免疫细胞涌入并加剧损害。内皮细胞内存在一套质量控制系统,称为未折叠蛋白反应(UPR),它帮助细胞在内质网这一结构中应对压力。其中的关键成分 IRE1,像一个在细胞受压时的传感器和调控器。研究者提出问题:这种内皮应激感受器在 TBI 后是帮助防御屏障,还是使情况恶化?
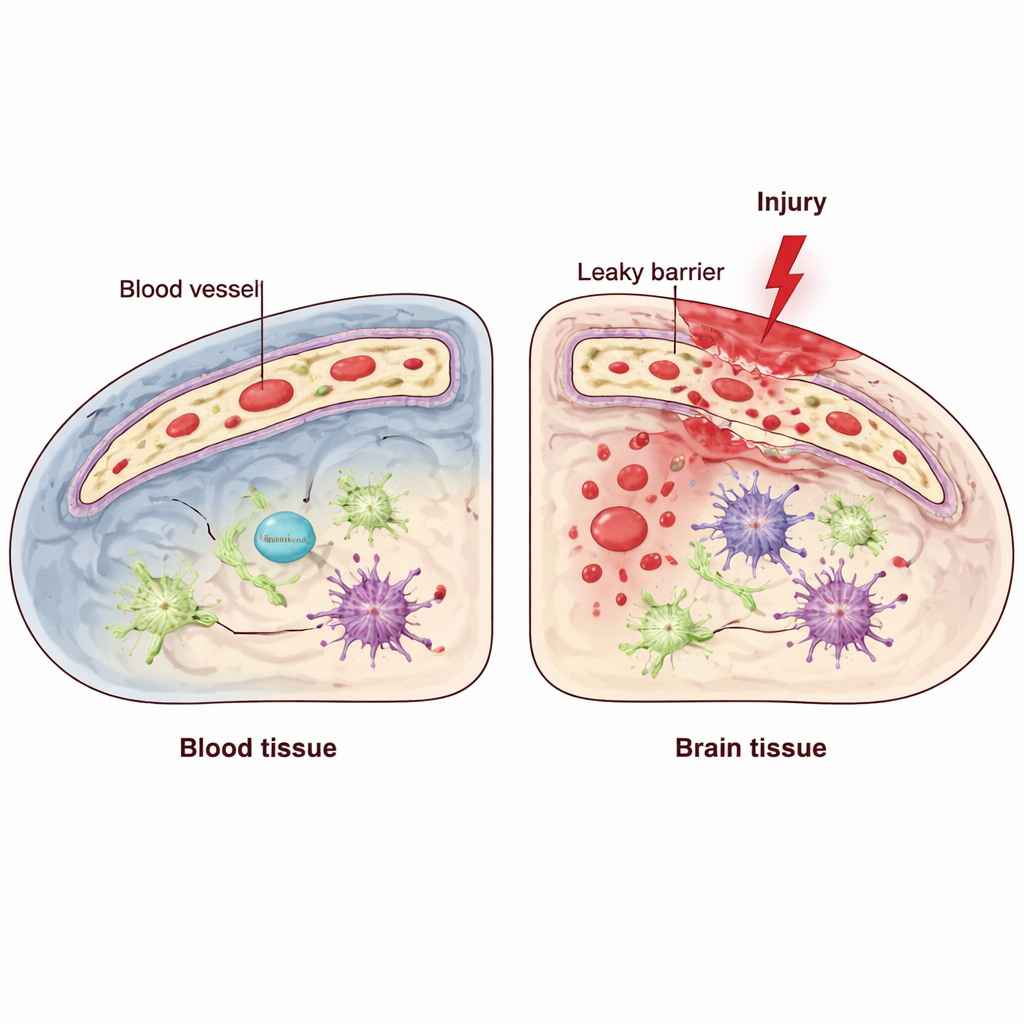
在血管细胞中关闭一种细胞传感器
为了解答这一问题,团队使用了基因工程小鼠,使 IRE1 能够被选择性地在内皮细胞中关闭。他们随后在皮层的运动区制造受控损伤,以模拟人类 TBI 的部分特点,并将这些小鼠与正常同窝小鼠进行比较。研究者通过衡量平衡和精确着爪等任务测试运动功能,并用高分辨率显微镜和分子技术检查脑组织。在正常小鼠中,损伤后不久血管细胞中的 IRE1 活性在损伤附近上升,表明内皮细胞能迅速感知并响应应激。当 IRE1 在这些细胞中特异性缺失时,动物在运动测试中的表现更差,说明功能恢复更差。
血管渗漏、更多免疫细胞与神经元死亡
研究者接着评估血–脑屏障的完整性。通常,大型血浆蛋白如抗体会留在血管内。TBI 后,在病灶附近出现一定渗漏是可以预期的,但缺乏内皮 IRE1 的小鼠显示这些蛋白质向脑内更广泛地渗出。显微镜观察显示,一种关键的连接分子 VE-cadherin(帮助内皮细胞相互密封)在损伤区域减少,即便血管总数看起来相似。这种渗漏伴随免疫细胞涌入病灶周围及炎性信号水平升高。在这些区域,神经元更易出现退化和程序性细胞死亡的迹象,损伤核心周围的受损组织范围明显增大。
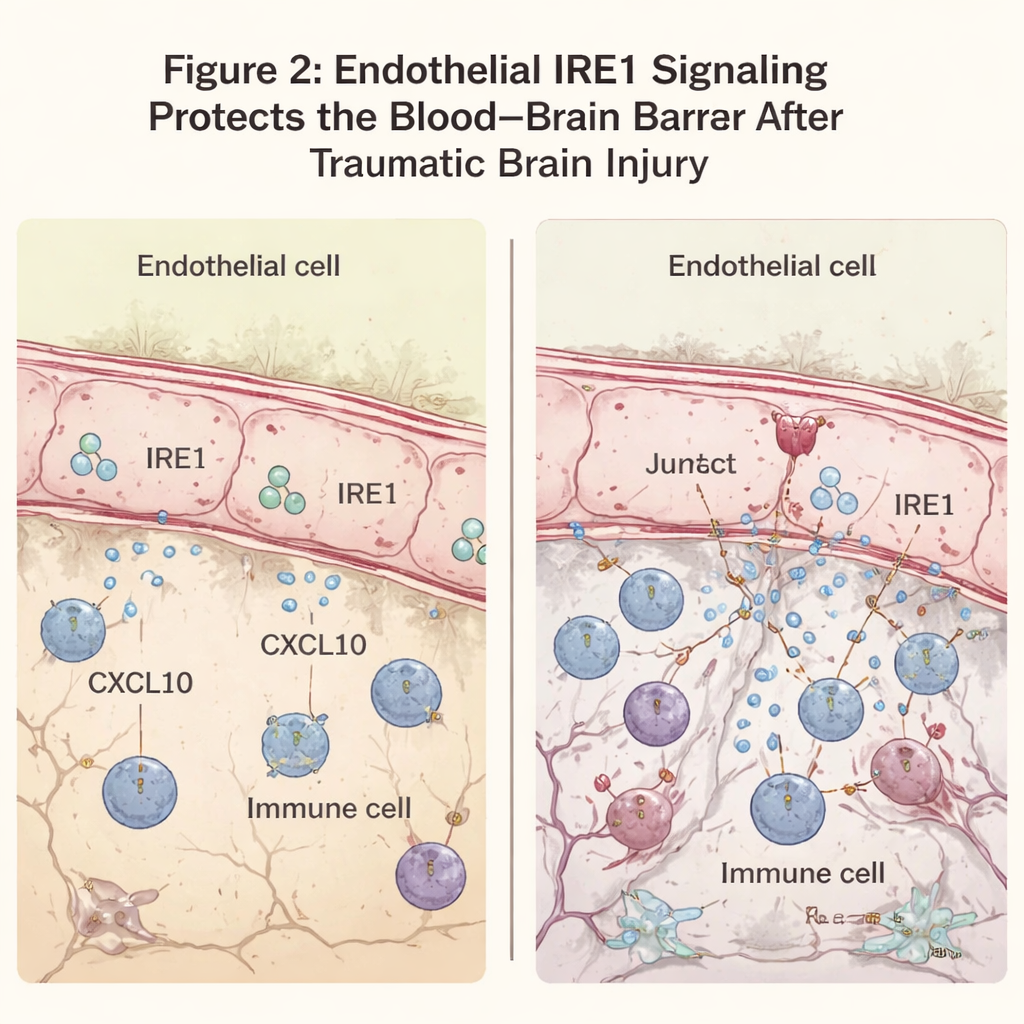
一种抗应激药物平息信号风暴
为探明分子机制,团队分析了损伤后被激活的基因。在缺乏内皮 IRE1 的小鼠中,与抗病毒和炎性反应相关的基因显著上调。其中尤为突出的是趋化因子 CXCL10,这类分子像信号焰火,会吸引免疫细胞并进一步削弱屏障。CXCL10 在 IRE1 缺失时在病灶附近的内皮细胞中尤其升高。在体外培养的脑内皮细胞暴露于炎性刺激时,使用一种名为 TUDCA 的药物降低内质网应激,可同时减少 IRE1 活性与 CXCL10 的产生。将 TUDCA 给予受伤小鼠后,受损皮层中的 CXCL10 和免疫细胞标志物下降,运动表现也有所改善,提示抑制该应激通路可减轻继发性损伤。
对头部受伤患者意味着什么
简单来说,这项工作表明,位于脑血管内皮细胞中的应激传感器 IRE1 在创伤性脑损伤后充当守护者。当它存在并正常工作时,有助于保持血–脑屏障的紧密,减少召唤免疫细胞的化学信号的释放,并限制围绕病灶的炎症扩散与神经元丧失。相反,若其失能,屏障会变得更易渗漏,免疫细胞大量涌入,更多脑组织受到损害。由于血管细胞相对容易通过血流中的药物到达,针对它们的应激反应(如使用 TUDCA 或未来更精确的疗法)可能成为减少头部外伤长期危害的可行策略。
引用: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
关键词: 创伤性脑损伤, 血–脑屏障, 内皮细胞, 神经炎症, 细胞应激