Clear Sky Science · zh
CD36 增强三阴性乳腺癌细胞对棕榈酸诱导的铁死亡的敏感性
肿瘤周围的脂肪为何既是朋友又是敌人
乳腺肿瘤生长在天然富含脂肪的组织中,癌细胞已知会“吃掉”附近的脂肪酸。这项研究探讨了一个令人意外的转折:在特定条件下,体内最常见的脂肪之一——棕榈酸,实际上可以通过触发一种特定的细胞死亡方式来帮助杀死一种特别具侵袭性的乳腺癌。理解这一过程有望为目前缺乏治疗选择的患者指明新的治疗方向。
显微镜下难以治疗的乳腺癌
三阴性乳腺癌(TNBC)缺乏许多现代药物所针对的激素和生长因子受体,使其成为最难治疗的乳腺癌类型之一。这些肿瘤与脂肪细胞紧密相邻,脂肪细胞释放大量脂肪酸,其中包括饱和脂肪棕榈酸。研究人员想弄清楚棕榈酸是否仅仅是肿瘤生长的燃料,还是也可能创造一种可被利用来杀死癌细胞的弱点。
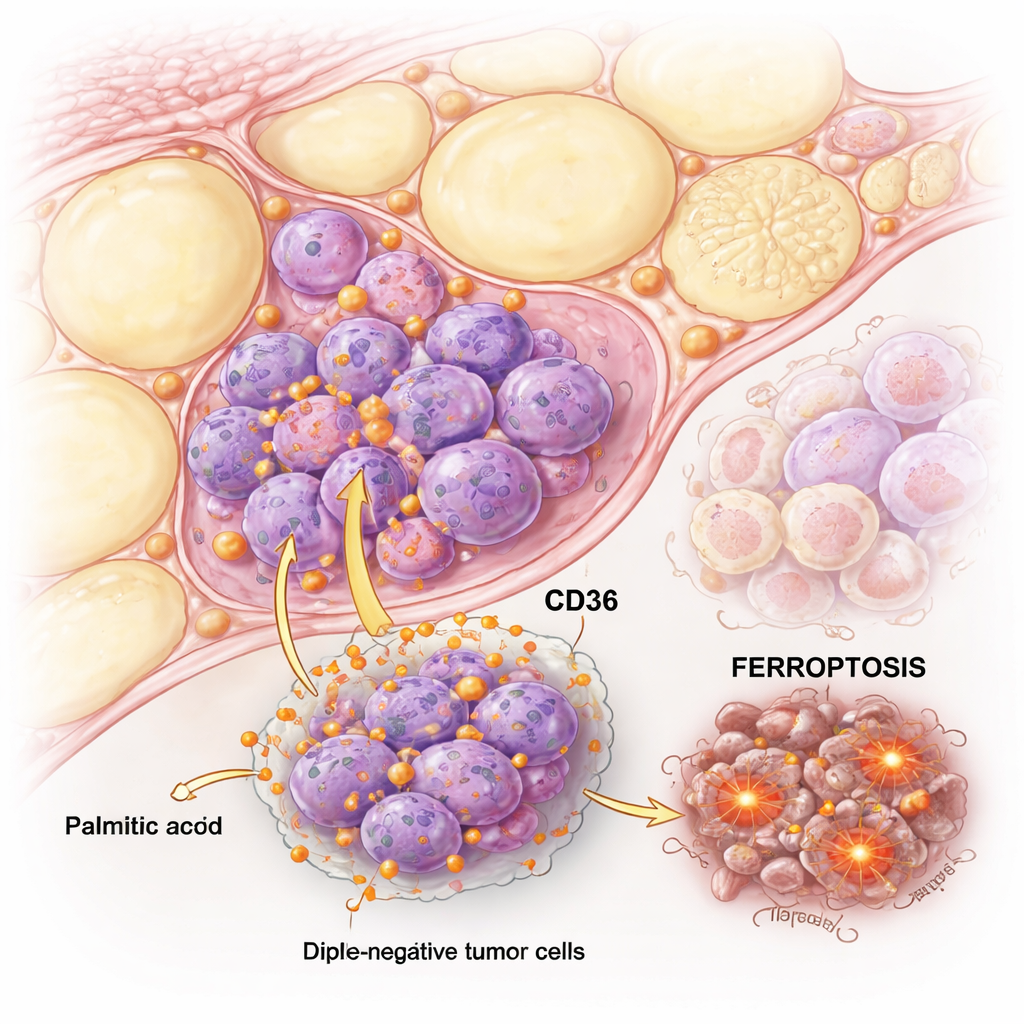
当棕榈酸将癌细胞推向崩溃
研究团队将 TNBC 细胞与对激素敏感的“腔内型”(luminal)乳腺癌细胞进行比较,并给予逐渐增加的棕榈酸剂量。两类细胞在高剂量下都会受到伤害,但 TNBC 细胞的敏感性远高于腔内细胞。详细检测显示,在腔内细胞中,棕榈酸主要引发经典的细胞凋亡——一种相对整洁的细胞死亡方式。然而在 TNBC 细胞中,棕榈酸既触发了凋亡,又引发了一种较不熟悉的途径——铁死亡,这种死亡依赖于铁和细胞膜脂质的破坏。
名为 CD36 的脂肪酸“门道”
为了解为何 TNBC 细胞反应截然不同,研究人员把注意力集中在 CD36 上——一种位于细胞表面的蛋白,像门道一样允许长链脂肪酸进入。TNBC 细胞天然携带的 CD36 明显多于腔内细胞,且暴露于棕榈酸会进一步提升 CD36 水平。这意味着 TNBC 细胞摄取更多棕榈酸,累积更多受损脂质,线粒体产生更多活性氧,细胞内游离铁也增多——这些都是铁死亡的关键信号。当用药物阻断 CD36 或用遗传手段降低其表达时,棕榈酸诱导的铁死亡显著下降。
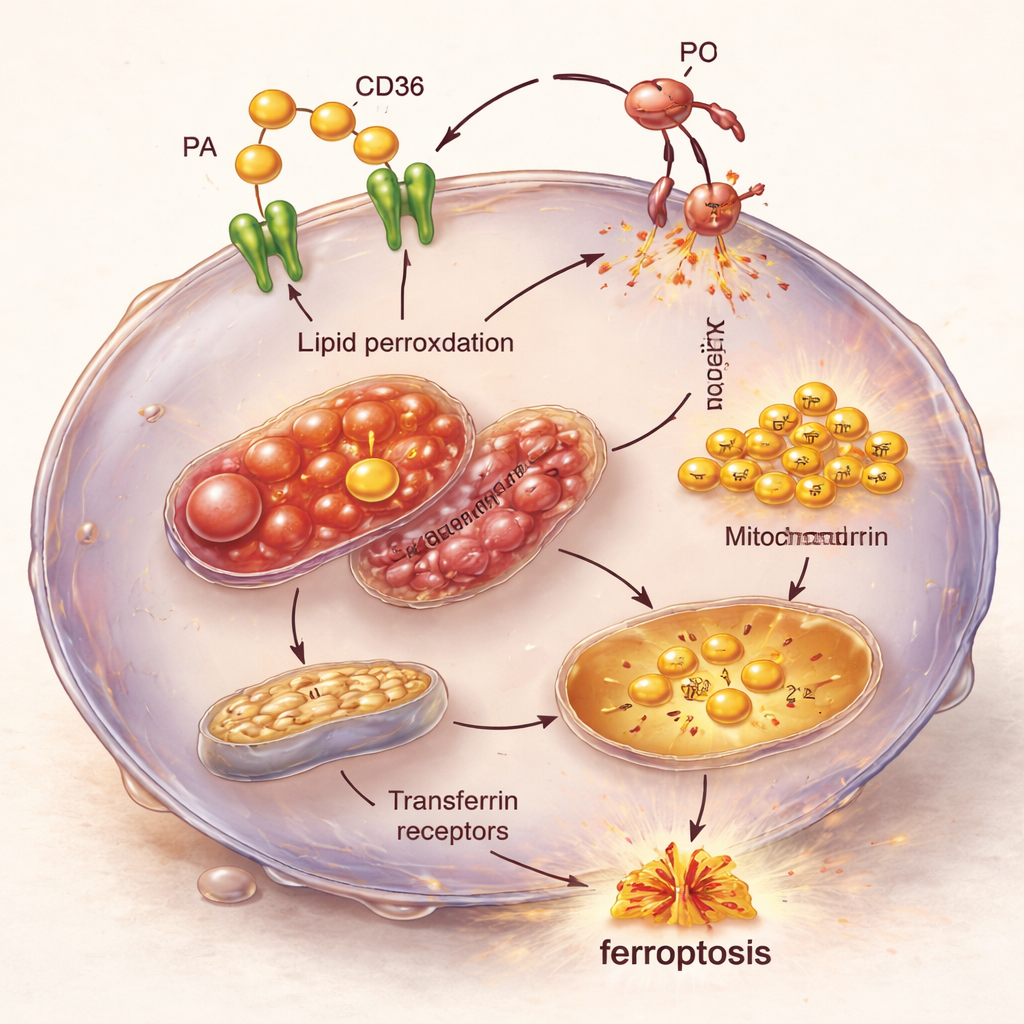
聚焦细胞内部的连锁反应
显微镜观察和基因活性分析揭示了这一脆弱性的内部连锁反应。充斥棕榈酸且 CD36 表达升高的 TNBC 细胞显示出肿胀、结构受损的线粒体,并且通过转铁蛋白受体带入的铁水平上升。与此同时,促进铁死亡的基因被激活,而通常保护细胞免受这类死亡的基因则被下调。结果就是一场完美风暴:过量脂肪涌入、更多可用于驱动化学反应的铁、以及抵御脂质损伤的防御被削弱,共同将 TNBC 细胞推向铁死亡。
哪些患者可能受益最大?
癌症并非单一,即便在 TNBC 内部也存在异质性。利用在小鼠体内培养的肿瘤样本和大型患者数据库,作者发现 CD36 在一种名为腔内雄激素受体(LAR)的 TNBC 亚型中特别高,这一亚型此前已被注意到对铁死亡较敏感。其他具有高铁摄取特征的 TNBC 亚型也倾向于显示较高的 CD36 水平。这一模式表明,CD36 可作为标志物,用于识别那些肿瘤天生更易被基于铁死亡的疗法触发的患者。
将常见脂肪转为治疗盟友
简而言之,这项工作表明,一种常见的膳食及体内脂肪——棕榈酸,在癌细胞表达高水平脂肪转运蛋白 CD36 时,能够帮助杀死某些三阴性乳腺癌细胞。通过促成脂肪过载、铁积累和细胞膜损伤,CD36 使这些癌细胞更易发生不可逃避的铁死亡。如果未来的治疗能够安全地增强这一路径——或将其与进一步削弱细胞防御的药物联合使用——临床医生或许能将这一代谢弱点转化为攻击某些最具侵袭性的乳腺肿瘤的一种更精准的新策略。
引用: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
关键词: 三阴性乳腺癌, 铁死亡, CD36, 棕榈酸, 肿瘤代谢