Clear Sky Science · zh
USP30介导的己糖激酶2去泛素化控制葡萄糖的代谢命运及肿瘤进展
癌细胞如何改写它们对糖的利用
癌细胞以“嗜糖”著称:它们以不同寻常的方式燃烧糖分以支持快速生长。本研究发现了一个新的开关——一种称为USP30的蛋白,帮助肿瘤细胞决定如何使用葡萄糖。通过微调另一个蛋白己糖激酶2(HK2),USP30可以促使癌细胞更多地消耗糖并更快生长,这为未来抗癌药物提供了新的靶点。 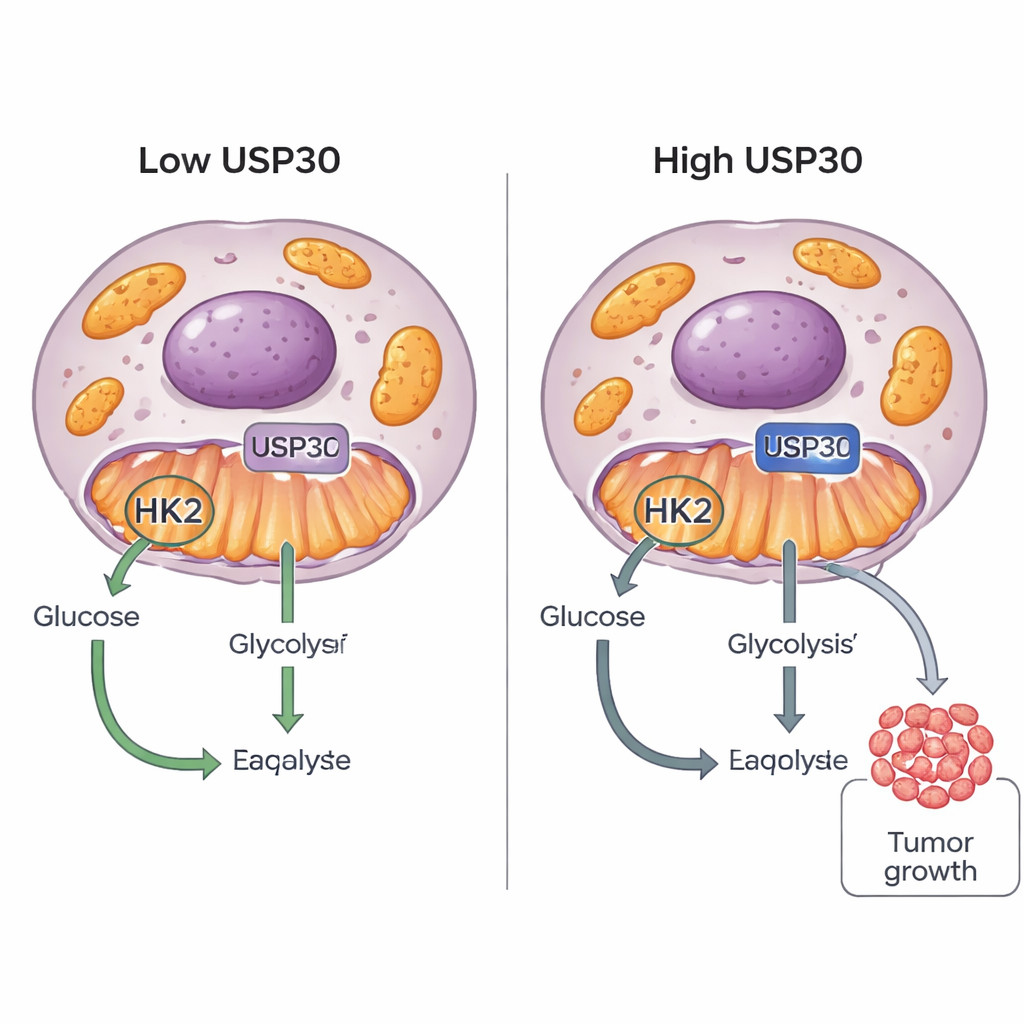
肿瘤内的嗜糖生活方式
大多数健康细胞以高效方式从营养物质中提取能量,但许多癌细胞偏好一种快速但粗糙的路径,称为有氧糖酵解,也就是瓦尔堡效应。它们摄取大量葡萄糖并迅速将其转化为乳酸,即便氧气充足。这种策略不仅产生能量:还为 DNA、脂质和蛋白质提供构建材料,帮助肿瘤抵抗压力,甚至削弱免疫攻击。在这一路径的门口坐落着己糖激酶,这种酶为进入的葡萄糖添加磷酸基团,使其进入后续分解和支持生长的代谢反应。
一个线粒体酶进入聚光灯
USP30是一种位于线粒体外表面的酶,线粒体是细胞的能量工厂。它属于“去泛素化酶”家族,能从其他蛋白上移除称为泛素的小标签,常常改变这些蛋白的稳定性、定位或活性。USP30此前已知在神经细胞和线粒体质控中有作用,但其对癌症的影响尚不清楚。通过挖掘大型癌症基因数据库,研究人员注意到,USP30水平较高的肿瘤倾向于表现出更强的葡萄糖燃烧特征和较弱的脂质氧化特征,这提示USP30可能在帮助癌症向糖代谢倾斜中发挥作用。
把USP30与细胞的“糖门”连接起来
为探讨这一联系,研究团队在若干癌细胞系中降低或敲除USP30并测量它们的能量代谢。使用能实时跟踪酸产生和氧气利用的仪器,他们发现失去USP30会显著降低糖酵解和线粒体呼吸。乳酸生成和葡萄糖消耗均下降,表明细胞的糖代谢发动机放慢。随后的一系列质谱实验显示,USP30与多种与葡萄糖代谢相关的酶发生物理相互作用,尤其是己糖激酶家族的HK1和HK2。后续测试表明,这种相互作用依赖于USP30的催化活性,并且是直接发生的,而非仅通过间接伙伴介导。
对己糖激酶2的精确分子操控
深入研究表明,USP30从HK1和HK2上去除的是特定类型的泛素链——所谓非典型连接链。对于HK2,这种修饰发生在单个关键氨基酸赖氨酸144(K144)上。当K144被突变以无法再携带泛素时,HK2变得更稳定,与线粒体上的通道蛋白VDAC1结合更紧密,且酶活性更高。工程化携带该K144突变的细胞将更多HK2定位到线粒体,燃烧更多葡萄糖,释放更多乳酸,并在培养皿中表现出更快的生长和迁移。在小鼠中,由携带K144突变HK2的细胞形成的肿瘤比携带正常HK2的肿瘤生长更大、更快,凸显了这一微小分子开关的强大效应。 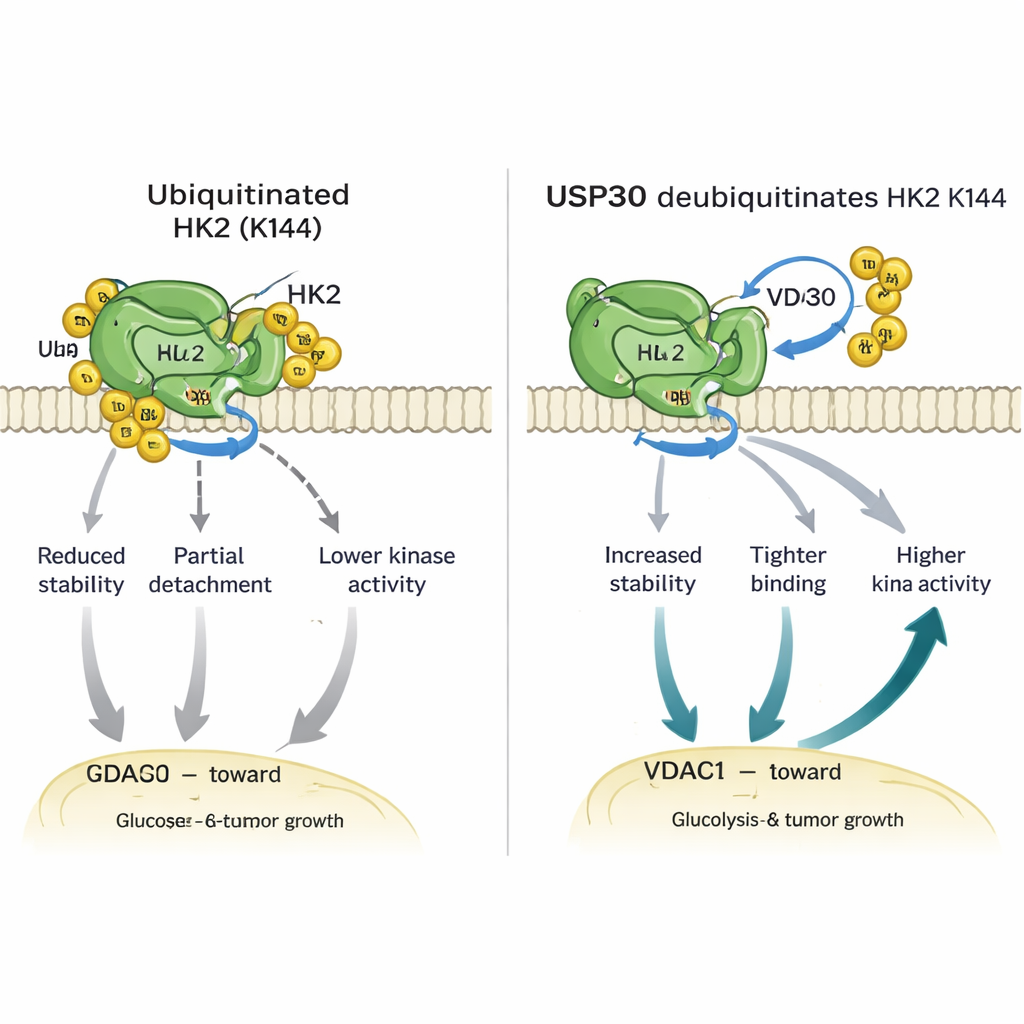
将代谢开关转化为生长优势
这些结果勾勒出一条明确的事件链:USP30与HK2结合,从K144处去除泛素标签,从而保持HK2在线粒体上的活性和锚定。这增强了糖酵解,为肿瘤细胞的分裂和迁移提供燃料,最终加速肿瘤生长。当USP30缺失或失活时,HK2变得不稳定且效能下降,癌细胞因此丧失部分代谢优势。从外行角度看,USP30就像一名修理工,保持癌细胞的“糖发动机”调校并固定在适当位置——移走这名修理工,发动机就会熄火。
这对未来癌症治疗意味着什么
对非专业读者来说,关键结论是:癌细胞依赖对其糖代谢进行精细调控,而USP30是这一控制面板上新发现的旋钮。通过稳定HK2在一个特定位点,USP30帮助肿瘤维持嗜糖代谢并更具侵袭性。阻断USP30的药物,或破坏其在赖氨酸144处对HK2的结合,可能通过削弱肿瘤的“糖发动机”来抑制肿瘤,而不一定对正常细胞造成同等程度的伤害。因此这项工作为理解癌症如何重构代谢提供了重要拼块,并指示了一个有前景的靶向治疗新方向。
引用: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
关键词: 癌症代谢, 糖酵解, 己糖激酶2, USP30, 瓦尔堡效应