Clear Sky Science · zh
卵母细胞特异性敲除eIF2亚基导致小鼠早期生长期滤泡内卵母细胞通过线粒体功能障碍和DNA损伤发生凋亡
为何卵细胞的存续至关重要
女性出生时便携带了终生的卵细胞,这些卵细胞储存在卵巢内称为滤泡的小结构中。当这些滤泡过快丧失时,女性可能出现卵巢早衰(POI),导致过早不孕并在年轻时出现类似更年期的症状。本项小鼠研究提出了一个基础而关键的问题:当合成新蛋白的一个关键步骤出现故障时,卵细胞内部会发生什么,这又如何导致生育能力的早期丧失?
细胞启动蛋白合成的开关
为了保持健康,卵细胞必须在适当时间合成合适的蛋白。该过程的核心是一台由三部分组成的分子机器eIF2,它帮助将遗传信息启动为蛋白质合成。研究者选择性地在小鼠早期生长期的卵母细胞中关闭了eIF2的两个亚基,分别是eIF2α和eIF2β。任一亚基缺失时,雌鼠均完全不育。其卵巢体积缩小,从早期滤泡到成熟排卵滤泡的正常进展明显受阻,各个后期阶段的滤泡数量显著减少。随着时间推移,基本上所有滤泡都被耗竭,呈现出严重的早发型POI样病程。
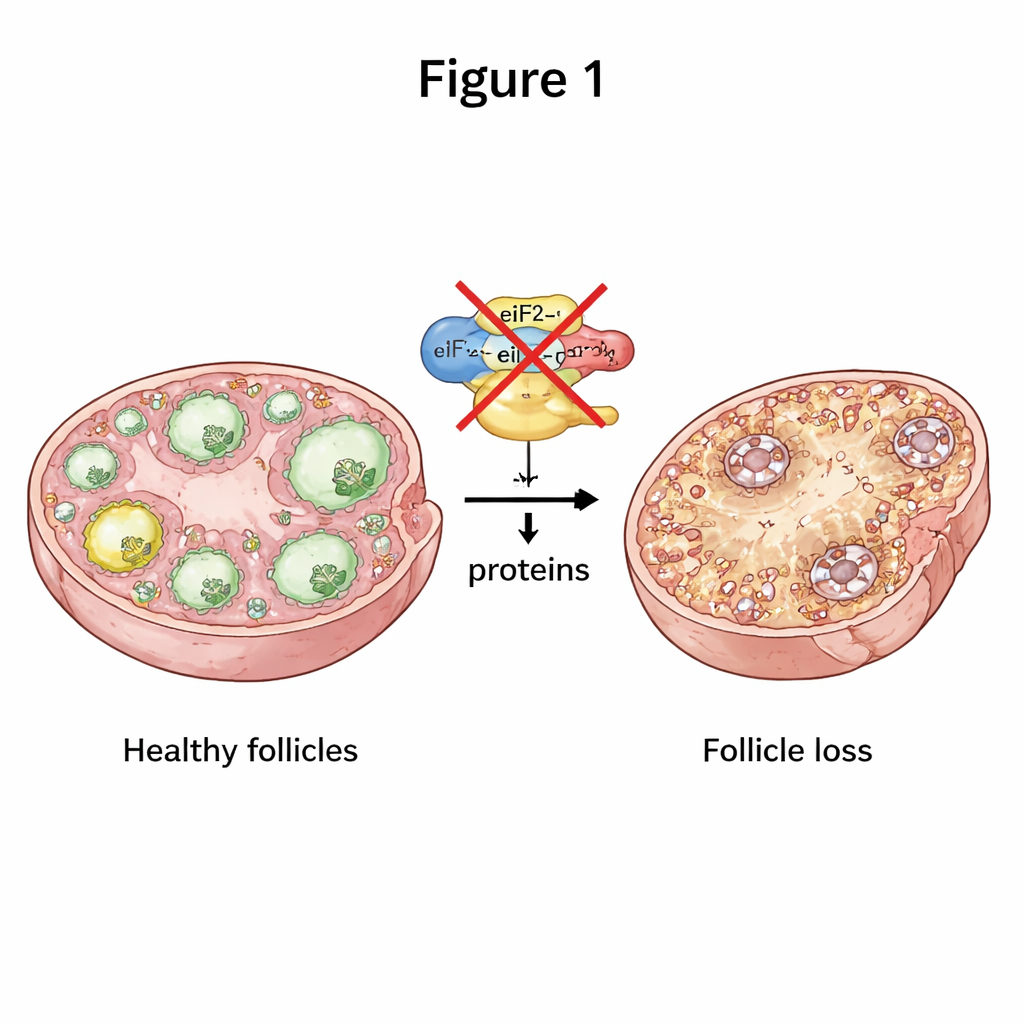
卵巢内通讯中断时的后果
滤泡并非单独存在的卵细胞;它们是卵细胞与周围“辅助”细胞——颗粒细胞之间的紧密协作体。研究团队发现,缺失eIF2β的卵母细胞中,多种通常支持颗粒细胞生长和营养输送的关键信号蛋白表达显著降低。卵细胞与颗粒细胞之间的物理桥接结构紊乱并变短,电子显微镜下卵细胞表面的微绒毛显得发育不良并受损。这些滤泡中的颗粒细胞分裂减少、死亡增加。双向通讯的这一崩溃导致滤泡无法正常发育,推动卵巢走向滤泡耗竭。
卵细胞“电池”的能量失效
线粒体常被称为细胞的发电厂,在卵细胞中尤为重要,因为它们为生长及随后胚胎发育提供能量。在缺乏eIF2β的卵母细胞中,总体新蛋白合成速率下降,许多与线粒体相关的蛋白表达减少。线粒体变得异常延长、在细胞表面附近聚集,显示出膜电位减弱、能量(ATP)水平降低以及线粒体DNA拷贝数减少。同时,细胞内积累了高水平的活性氧(ROS),这些具有攻击性的氧基分子会损伤细胞组分。综合这些变化表明线粒体动力学与功能发生了严重崩溃。
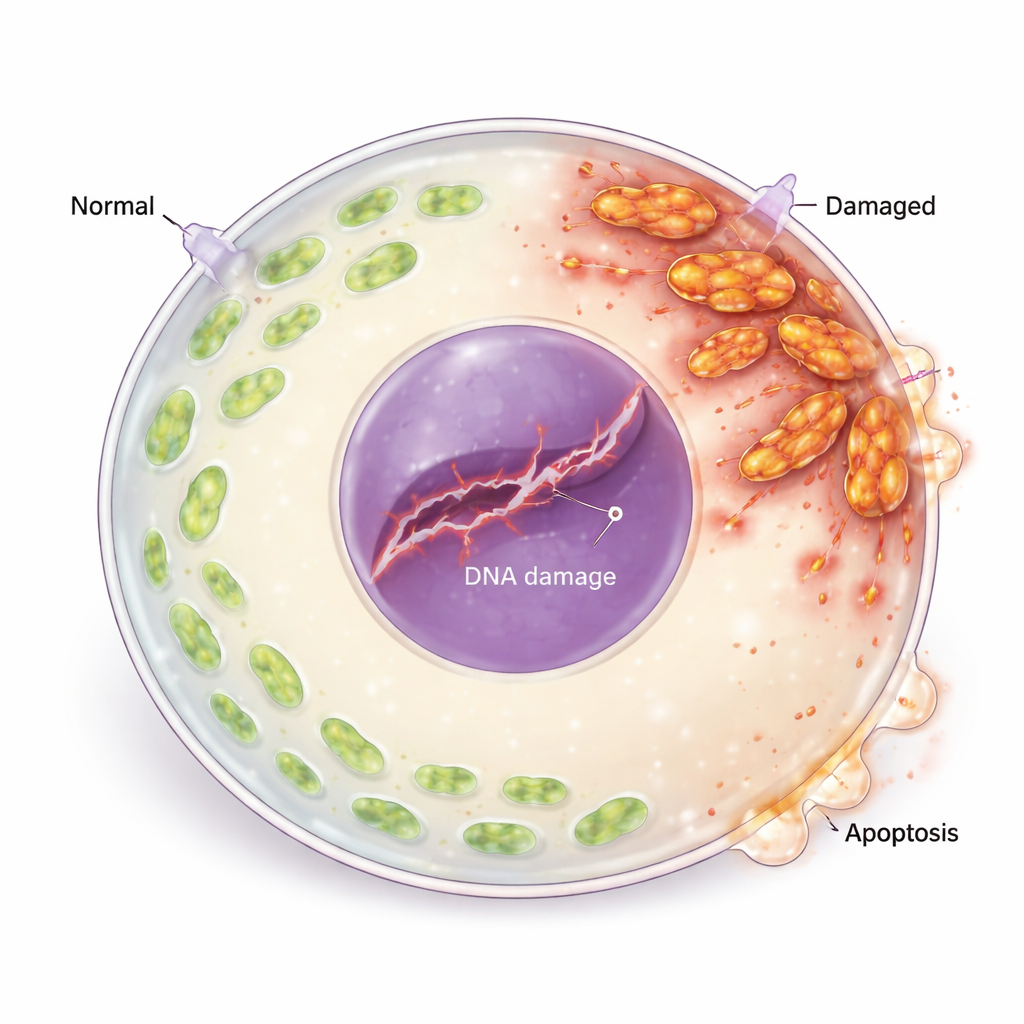
从氧化应激到DNA损伤与细胞死亡
过量的活性氧不仅损害线粒体,也伤及卵细胞的遗传物质。研究者观察到断裂DNA链的标志物增加以及细胞DNA损伤反应机制的激活,包括感知和报告遗传损伤的蛋白。一种关键修复蛋白表达下降,提示损伤未能被高效修复。下游的生死调控平衡发生转向:促死蛋白上升而抗死保护蛋白下降,卵细胞出现明显的程序性细胞死亡(凋亡)特征。当研究组用抗氧化剂(N-乙酰半胱氨酸)处理卵母细胞时,ROS水平下降,DNA损伤与凋亡标志物减少,卵细胞成熟有所改善,直接将氧化应激与卵细胞丧失联系起来。
对早发性卵巢衰竭的意义
通过追踪从单一分子复合体(eIF2)到错误的蛋白质合成、线粒体崩溃、氧化应激、DNA损伤,最终导致卵细胞死亡的事件链,本研究描绘了一条可能毁灭卵巢储备的详细途径。该研究强化了这样一个观点:翻译启动因子的突变(已在一些POI患者中发现)可以通过此途径直接损害卵细胞。研究还指向潜在的干预手段:抗氧化剂、应激反应调节剂或保护早期滤泡的治疗(例如抗缪勒管激素,在这些小鼠中对休眠滤泡有部分保护作用)可能有一天帮助那些卵巢易受类似损伤的患者维持生育力。
引用: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
关键词: 卵巢早衰, 卵母细胞凋亡, 线粒体功能障碍, 蛋白质翻译, 活性氧