Clear Sky Science · zh
转谷氨酰胺酶2通过直接使GSK3β失活加剧卵巢癌的存活
这项研究为何对女性健康重要
卵巢癌是女性中致死率最高的癌症之一,因为它通常在晚期才被发现,且即使经过强力化疗也常常复发。这项研究揭示了一种鲜为人知的蛋白——转谷氨酰胺酶2(TGase 2)——如何帮助卵巢癌细胞在治疗中生存并在体内扩散。通过暴露这一隐藏的癌症帮手,研究为提高现有药物效果、减缓或阻止致命性转移提供了新的思路。
侵袭性肿瘤内的隐秘驱动因子
临床长期观察到许多卵巢癌对化疗产生耐药并在腹腔广泛扩散。上皮—间质转化(EMT)是其中一个主要原因;在此过程中,癌细胞放松彼此的连接,变得更具移动性,更像侵袭性的“游走者”而非有组织的组织细胞。作者证实,TGase 2在正常卵巢组织中含量极低,而在卵巢肿瘤中明显升高,并且与这种转变密切相关。在大量人体组织样本中,TGase 2水平从早期肿瘤到晚期及转移性疾病逐步升高,其丰度与多种调控细胞迁移、生长和血管生成的EMT相关基因的活性紧密匹配。 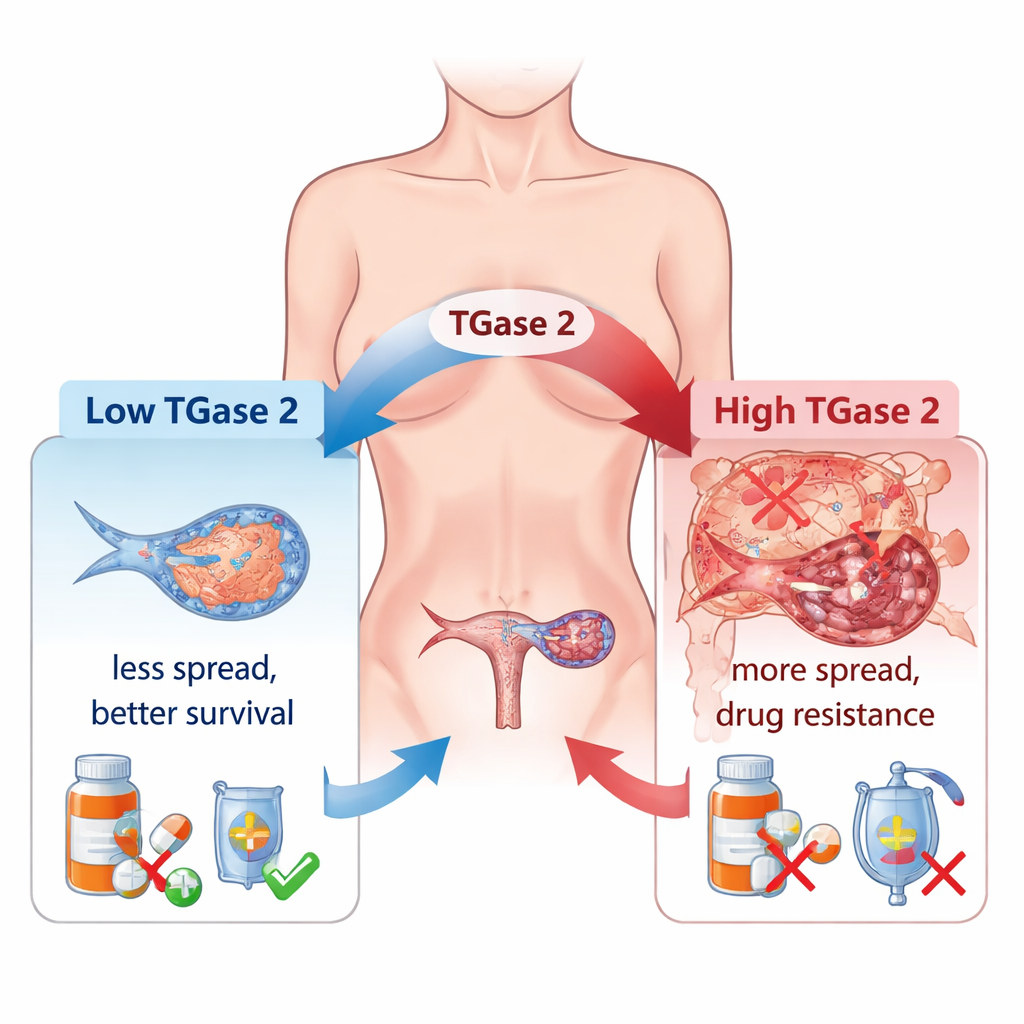
TGase 2如何扳动关键的安全开关
为弄清TGase 2在癌细胞内部的实际作用,研究人员将注意力集中在其与另一种蛋白GSK3β的关系上。在健康状态下,GSK3β像一只控制侵袭的刹车:它让一种称为β-连环蛋白(β-catenin)的信号分子保持低水平,从而抑制驱动EMT的基因。研究团队发现,TGase 2能与GSK3β直接结合,既削弱其活性,又促进通过细胞自噬通路将其送往降解。当TGase 2丰富时,卵巢癌细胞迁移能力增强,且经典的EMT标志物如纤维连接蛋白、波形蛋白和β-连环蛋白水平均升高。当研究者用遗传手段降低TGase 2时,这些侵袭性特征减弱,β-连环蛋白信号被抑制,表明TGase 2破坏了抵御转移的关键安全开关。
从细胞到活体动物的验证
研究团队接着探讨抑制TGase 2是否能在动物体内减缓癌症。他们构建了缺失TGase 2基因的卵巢癌细胞并将其移植到小鼠体内。与接受正常癌细胞的小鼠相比,注入缺失TGase 2细胞的小鼠肿瘤负担较小且生存时间更长。在另一个模拟癌细胞经血液扩散的模型中,注射TGase 2缺失细胞的小鼠在肺部形成的转移灶明显更少且更小。重要的是,这些转移灶显示出更高的GSK3β水平,符合去除TGase 2可恢复对侵袭的天然刹车、帮助控制疾病的观点。
把实验室线索转化为药物策略
由于在患者体内删除基因不可行,作者测试了一种名为链霉硝霉素(streptonigrin)的低分子化合物,已知其可与TGase 2用于与其他蛋白相互作用的同一端相结合。他们发现链霉硝霉素可以干扰细胞内TGase 2与GSK3β的相互作用,减少两者的共定位并限制癌细胞迁移。在卵巢癌小鼠模型中,经口给药的链霉硝霉素减缓了肿瘤生长、缩小了转移病灶并延长了生存期。最显著的是,当链霉硝霉素与顺铂或紫杉醇等标准化疗药物联合使用时,小鼠的生存期比单用化疗延长了数周。单独化疗往往会升高TGase 2水平并降低GSK3β,间接推动细胞走向EMT,但加入TGase 2抑制剂可以逆转这一趋势并抑制细胞新获得的迁移性。 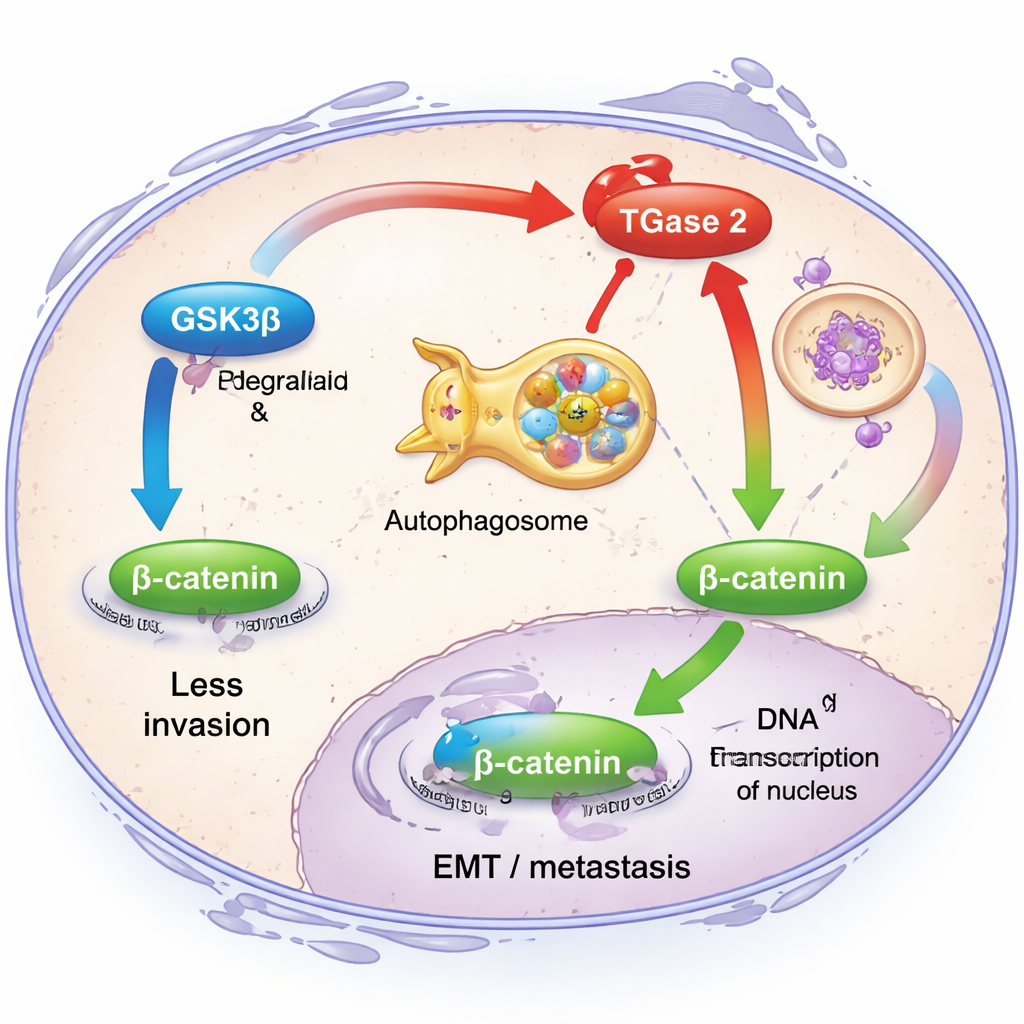
这对未来治疗意味着什么
对非专业读者而言,核心信息是:卵巢癌细胞利用TGase 2关闭内在的反转移刹车,从而在化疗冲击下存活。通过直接使GSK3β失活并稳定β-连环蛋白,TGase 2帮助肿瘤变得更具侵袭性和耐药性。这项工作表明,针对TGase 2 N端区域的药物——例如链霉硝霉素或未来以其为模型研发的更安全化合物——可能增强现有化疗效果、降低复发风险并改善生存。简单来说,靶向TGase 2有望关闭癌细胞的“逃逸通道”,使卵巢肿瘤对治疗更敏感、扩散能力更弱。
引用: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
关键词: 卵巢癌, 药物耐受性, 转移, 上皮—间质转化, 靶向治疗