Clear Sky Science · zh
抑制自体抗原诱导的B细胞受体(BCR)内吞作为弥漫性大B细胞淋巴瘤(DLBCL)的一种治疗策略
这对患者意味着什么
弥漫性大B细胞淋巴瘤(DLBCL)是成人中最常见的快速增长性血液癌症,许多患者在标准化疗‑免疫治疗后仍会复发。这项研究揭示了这类肿瘤中一个出人意料的薄弱点:它们对一种位于细胞表面的“天线”——B细胞受体(BCR)的依赖性。研究表明,阻断该天线被拉入细胞的过程可以削弱癌细胞的生存能力,这为将长期使用的抗恶心和抗精神病药物重新定位为抗淋巴瘤辅助药物打开了大门。
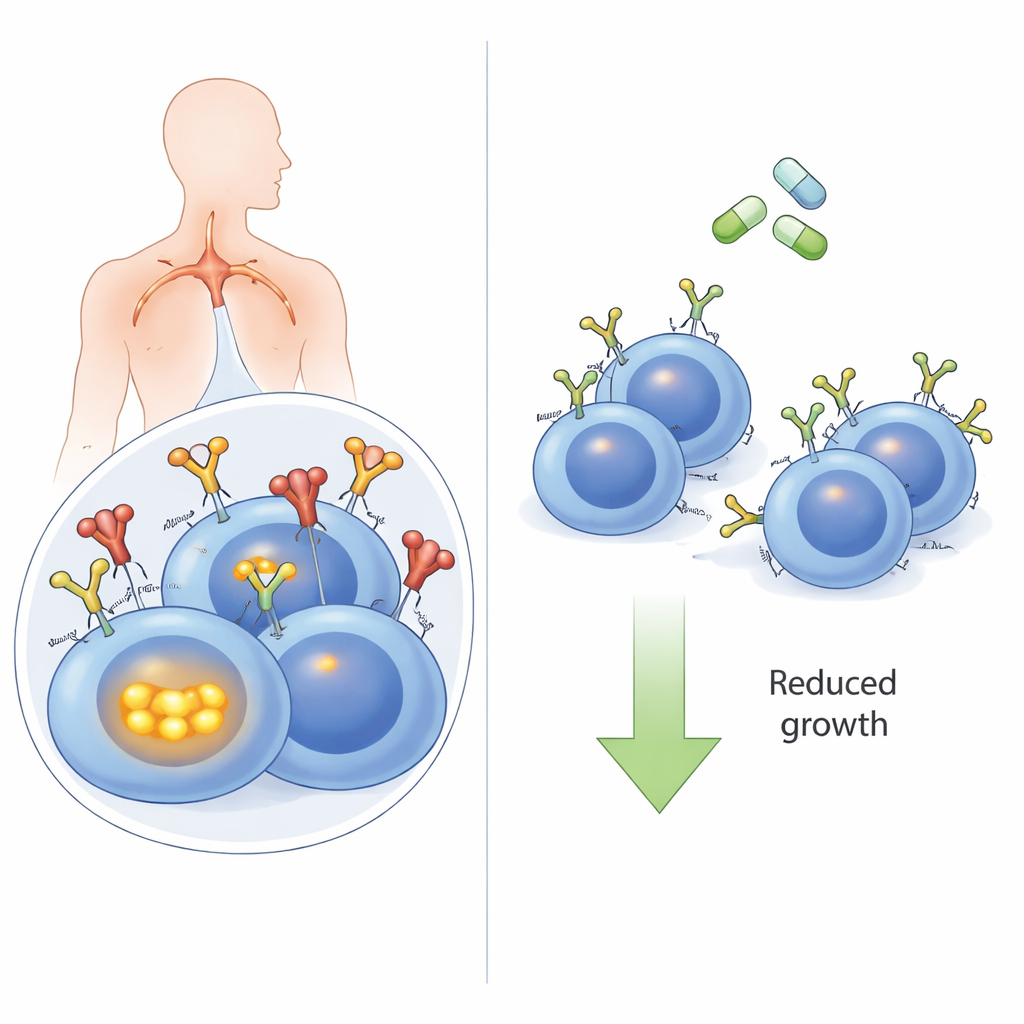
癌细胞的天线
B细胞是一种白细胞,它们通过表面的B细胞受体识别威胁。在许多DLBCL中,尤其是高风险的“活化B细胞”(ABC)亚型,这种受体被劫持以持续发出“保持存活并生长”的信号。通常,这些BCR识别的是机体自身的分子(自体抗原),类似于卡住的门铃。当自体抗原结合时,BCR不仅在表面发出信号:它还被拉入细胞,并与含有TLR9和MYD88等传感器的内部蛋白簇聚集。该超级复合体随后激活NFκB——一个强有力的促进生长的信号通路。直到现在,还不清楚受体的这一内向转运是否对驱动癌变的信号真正必需。
改造天线以检验其极限
为了解答这个问题,研究者使用CRISPR基因编辑精确改变了淋巴瘤细胞系中BCR的“末端”。他们用识别卵白蛋白(一种作为实验工具的无害蛋白)的序列替换了天然的自反应识别区。这些改造后的受体不再捕捉其常见的自体抗原,但仍可通过外加卵白蛋白以受控方式被激活。在通常依赖自体抗原结合的ABC型淋巴瘤细胞中,这一替换显著降低了多种关键信号酶的活性并抑制了NFκB响应基因。尽管这些细胞表面实际上有更多BCR,但它们生长变慢,表明持续的自体抗原参与及随后的内部信号传递对其存活至关重要。
将受体拉入细胞:关键一步
团队随后直接观察BCR在遇到抗原后的去向。在他们构建的模型中,无论是基于抗体的触发还是卵白蛋白,都在数分钟内使受体从细胞表面消失,证实了快速的内吞。这种内吞不仅发生在抗原在细胞外游离时,也发生在抗原被人为展示在同一细胞膜上,模仿某些真实肿瘤情形。通过遗传手段阻断这一内向运输——使用一种对网格蛋白介导的内吞必需蛋白dynamin‑2的显性抑制型——可使BCR留在表面、缩小细胞内的BCR–TLR9–NFκB复合体、降低NFκB靶基因表达并减慢细胞生长。有趣的是,当内吞被阻断时,表面一些“背景”BCR信号增加,提示癌细胞可能会通过增强一种较弱的、持续性的信号模式来尝试补偿。
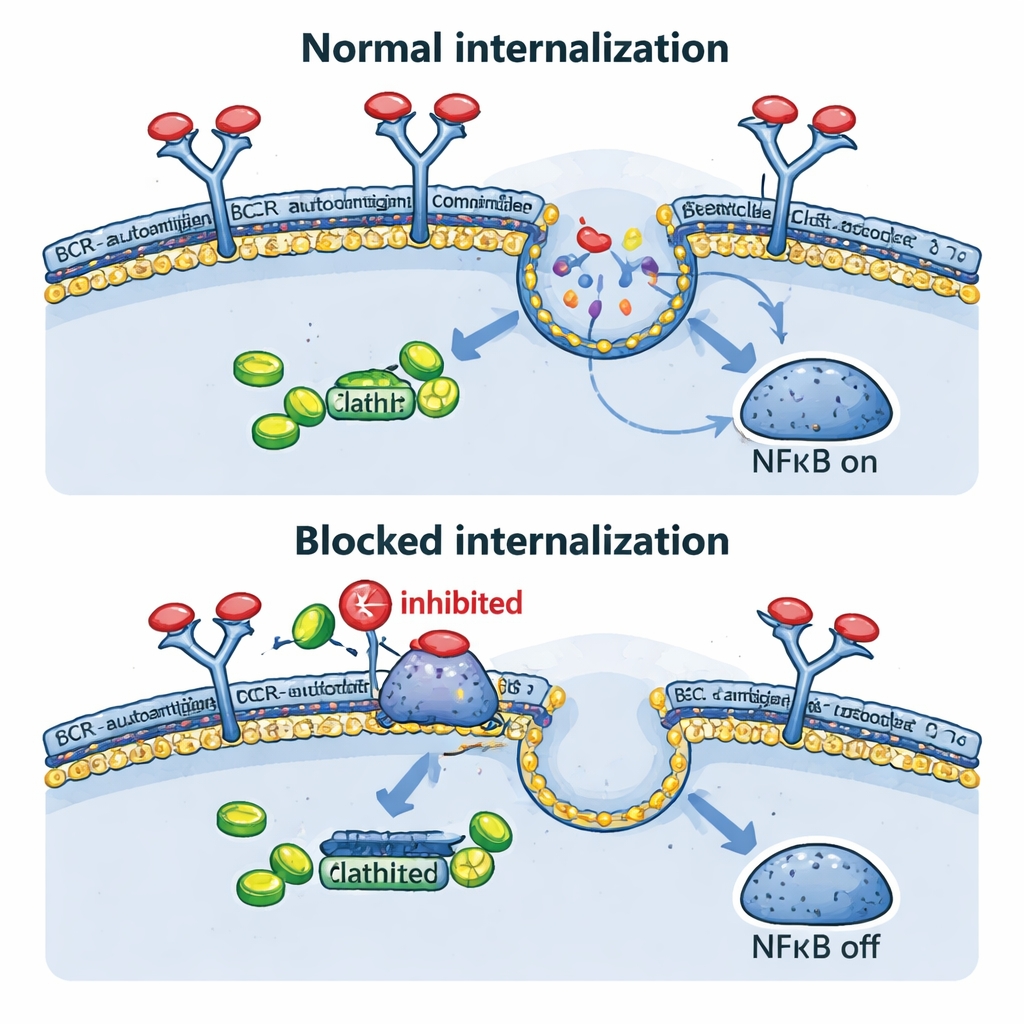
老药新用途
由于研发新药既慢又昂贵,作者接着探讨现有能阻断内吞的药物是否能模拟基因学实验的效果。苯噻嗪类是一类已知可抑制dynamin‑2和网格蛋白依赖受体摄取的抗精神病和抗恶心药物。在淋巴瘤细胞中,像盐酸普鲁氯丙嗪(prochlorperazine)和氯丙嗪(chlorpromazine)等化合物提高了表面BCR水平并强烈减少了抗原驱动的内吞。这导致NFκB驱动的基因活性下降并降低了ABC型DLBCL细胞的存活,尤其是那些具有完整BCR组分的细胞。在携带人类淋巴瘤移植的小鼠模型中,临床可达剂量的普鲁氯丙嗪显著减缓了肿瘤生长。此外,将苯噻嗪类与阻断其他BCR相关酶(如SYK和PI3Kδ)的药物联合使用,比单独用任一药物产生了更强的抗癌效果。
这对治疗可能意味着什么
总体而言,这项研究表明,对于DLBCL的一个重要亚群,驱动癌症的信号并非仅来自细胞表面的受体;它们在很大程度上依赖于通过特定内吞途径将BCR–抗原复合体拉入细胞。中断这一步骤——无论是通过遗传手段还是通过苯噻嗪类药物——都能削弱NFκB信号并损害肿瘤细胞的存活,同时可能使细胞对现有BCR通路抑制剂更敏感。鉴于苯噻嗪类作为抗恶心药物已有明确的剂量和安全资料,这项工作为在显示自体抗原依赖性BCR活性的患者中,单用或联合用药进行临床试验提供了现实可行的蓝图。
引用: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
关键词: 弥漫性大B细胞淋巴瘤, B细胞受体, 内吞作用, 苯噻嗪类, NFkB 信号传导