Clear Sky Science · zh
对人源 iPSC 衍生感觉神经元暴露于紫杉醇的时序多组学分析揭示化疗诱发周围神经病变的机制
为何某些抗癌药物会损伤神经
化疗拯救了数以百万计的癌症患者,但许多人为此付出了隐形代价:手脚数月甚至数年的灼痛、刺痛和麻木。本研究提出了一个简单却重要的问题:广泛使用的抗癌药紫杉醇究竟对人体感觉神经细胞做了什么?理解这些变化能否为更好地预防和治疗这种神经损伤指明方向?
从患者细胞到体外培养的痛觉神经元
研究人员没有依赖动物实验,而是取自五位人类供体的细胞,包括曾接受紫杉醇治疗的乳腺癌患者。他们将这些细胞重编程为诱导多能干细胞(iPSC),再引导分化为感觉神经元——即将来自皮肤的触觉和痛觉信号传到脊髓的那类神经细胞。实验室培养的这些神经元生长出长而纤细的神经纤维,并表现出与体内痛觉神经相似的电活动。研究团队随后以患者体内可见的药物浓度范围暴露这些细胞于递增剂量的紫杉醇,并在数日内跟踪细胞健康状况。低浓度时神经元能够应对,但在临床相关剂量(100 nM)下,其存活率在约两天后开始下降,标志着有毒性神经损伤的出现。
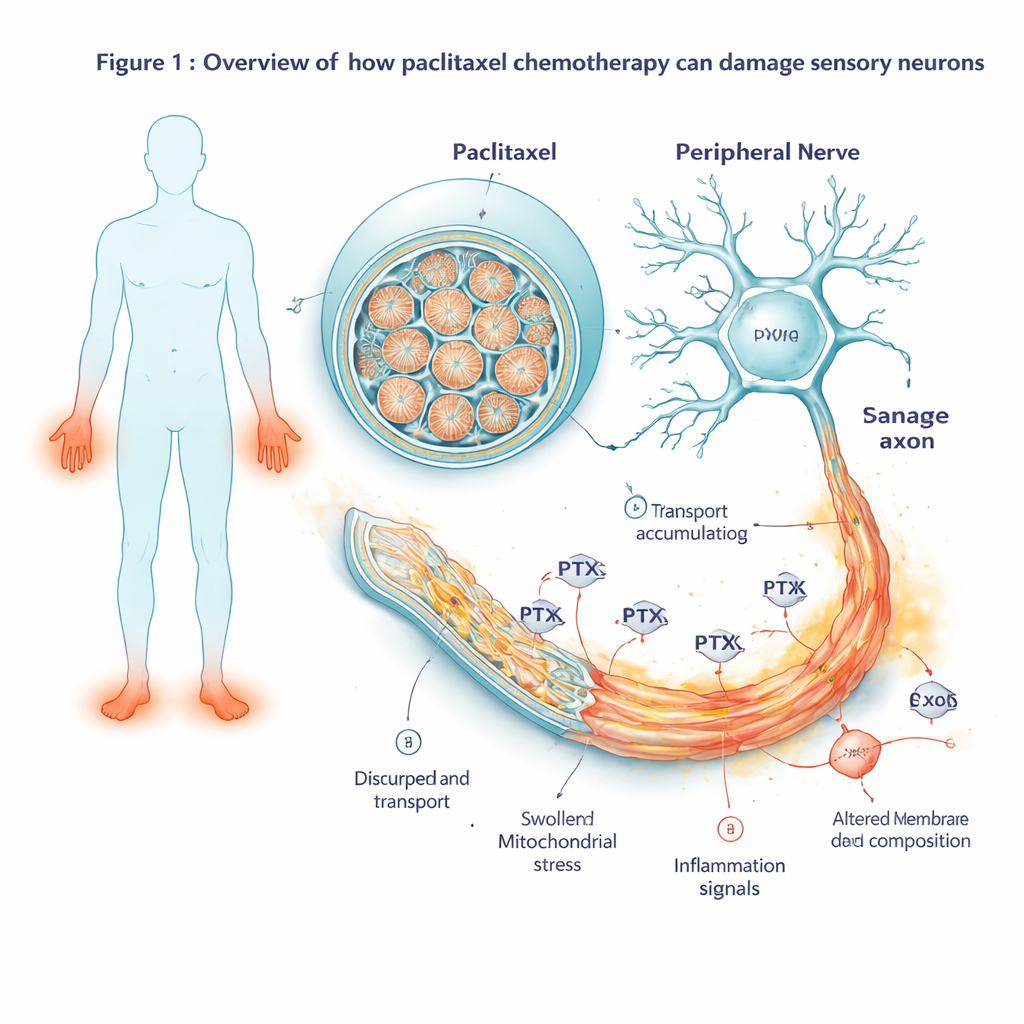
观察基因活性随时间的变化
为了在细胞出现可见退化之前了解其反应,科学家在从药物暴露后两小时到洗药后数天的多个时间点测量哪些基因被开启或关闭。早期他们观察到以基因 JUN 为核心的经典细胞应激程序被激活。随着暴露持续,这一应激信号扩展为全面的自毁级联反应:促使细胞进入程序性死亡的基因被强烈上调,而保护性因子则被压制。同时,与炎症和疼痛信号相关的基因变得更为活跃。神经元开始产生更多的炎性介质、与疼痛相关的肽类及使细胞对有害刺激更敏感的受体,这些变化与疼痛性神经疾病中的表现相呼应。
深入解析神经元内的蛋白质与脂类
鉴于基因仅是蓝图,团队还检测了神经元中实际存在的蛋白质及其脂质(脂肪)组成。紫杉醇暴露 48 小时后,许多在 RNA 水平检测到的应激和炎症信号也在蛋白水平上明显增加,证实神经元正在执行这些有害程序。醒目的是,与轴突运输相关的蛋白——负责沿长神经纤维运输货物的分子马达和骨架支撑——明显减少,其中包括动力蛋白家族和维持微管稳定的调控蛋白。在脂类层面,神经元关键的胆固醇与膜脂构件下降,同时储存性脂肪三酰甘油增加。总体来看,这些变化表明紫杉醇不仅触发细胞死亡途径,还削弱了神经纤维的物理结构与能量平衡。
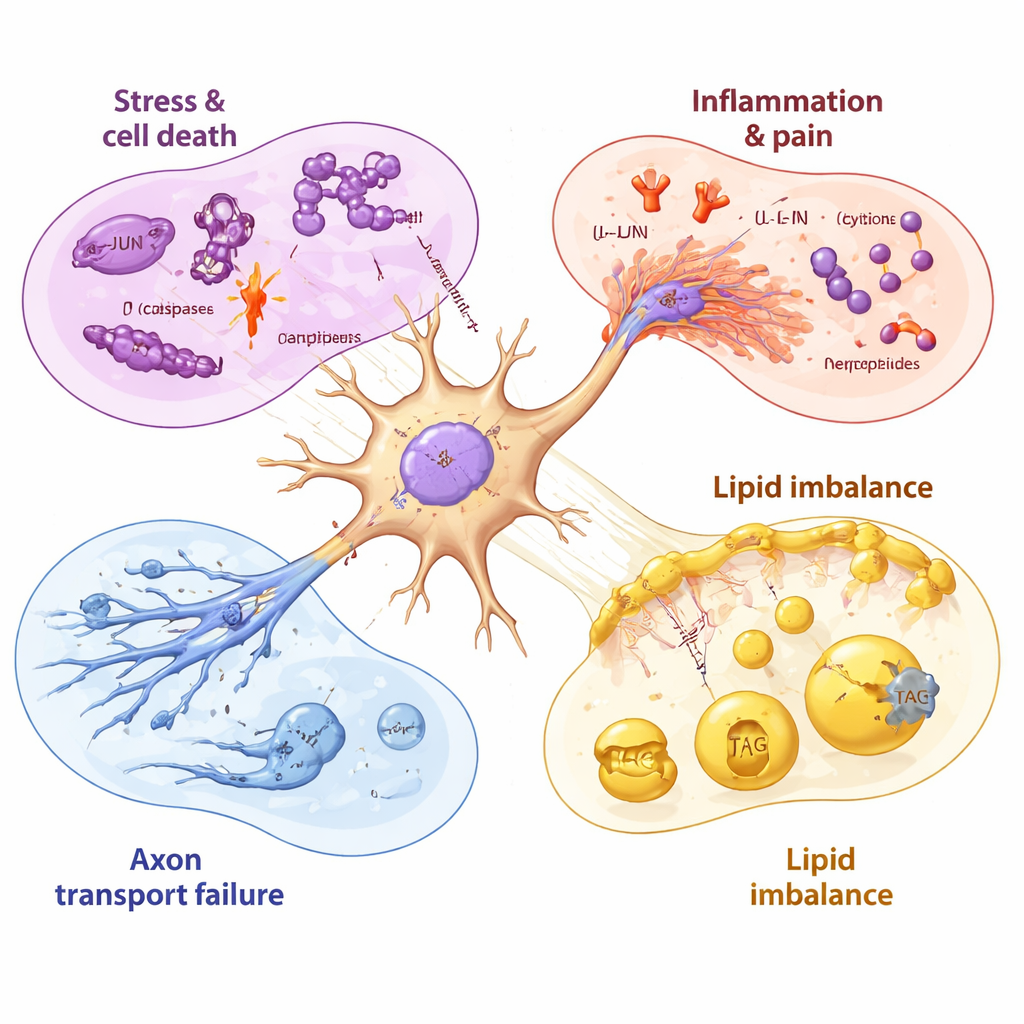
神经损伤与不完全恢复的时间线
通过在药物暴露前、暴露中与暴露后取样,研究者能够将这些事件按时间排列。与线粒体(能量相关)功能有关的基因在数小时内受到干扰,随后激活应激基因 JUN,接着在细胞活力开始下降时细胞死亡和炎症程序更强烈地被激活。即便在紫杉醇被移除后,许多有害信号仍在数天内保持升高,而合成健康膜脂所需的基因持续下降。一些晚期上调的分子,例如可将紫杉醇泵出细胞的药物外排泵和某些生长因子,暗示神经元正在尝试自我保护和修复——但这些反应相较于早期迅速推进的损伤倾向显得较慢且不完全。
对遭受神经疼痛患者的意义
对非专业读者而言,本研究传达的信息是:紫杉醇通过一系列联合作用损害感觉神经——它冲击能量系统、翻转基因开关以促使细胞死亡、激发炎症与疼痛信号、破坏神经纤维内部的“运输高速公路”,并改变维持神经膜稳定的脂类。通过对人源神经元进行精细的时序多组学描绘,研究凸显了具体且可药物干预的靶点——例如特定的应激调控因子、炎症受体和合成脂类的酶——这些靶点可能被抑制或支持以保护神经而不削弱抗癌治疗。尽管新的疗法仍需进一步检验,这项工作为预防或缓解化疗诱发的神经损伤提供了更清晰的路线图,有望改善癌症幸存者的生活质量。
引用: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
关键词: 化疗诱发周围神经病变, 紫杉醇, 感觉神经元, 神经炎症, 轴突退化