Clear Sky Science · zh
角质形成细胞中 MIF–p38–GSDMD 炎症回路是紫外B 诱导的皮肤型狼疮的基础
为什么阳光对狼疮患者可能成为严重问题
对大多数人来说,阳光顶多会让皮肤晒黑或晒伤。但对于许多狼疮患者,几分钟的紫外B(UVB)照射就能诱发疼痛且持续时间长的皮疹,甚至加重全身性疾病。该研究揭示了存在于皮肤细胞中的一个隐蔽“反馈回路”,有助于解释皮肤为何对光如此敏感——并指出了可能在局部平息反应的新方法,这些方法不会抑制整个免疫系统。
意想不到的皮肤细胞“始作俑者”
临床上已知皮肤型红斑狼疮(CLE)涉及慢性炎症和瘢痕形成,但研究往往集中在入侵的免疫细胞上。作者使用单细胞 RNA 测序,转而聚焦皮肤自身的构建细胞——表层的角质形成细胞和下层的成纤维细胞。他们发现狼疮患者中,特定亚群的角质形成细胞数量增加并表现出强烈的“干扰素签名”,即一组抗病毒警报基因持续开启。在这些异常角质形成细胞中,有一种信使蛋白格外突出:巨噬细胞迁移抑制因子(MIF),其产生水平远高于更常见的炎症分子如 TNF 或 IL‑6。
阳光释放的隐性信使
在角质形成细胞内发现高水平的 MIF 尚不能解释为何阳光如此危险。将培养的角质形成细胞暴露于 UVB 光后,研究团队发现细胞内的总 MIF 含量几乎未变——但该蛋白以剂量相关的方式被释放到周围液体中。UVB 剂量越大,MIF 泄漏越多,且与膜损伤标志物紧密相关。当将这种富含 MIF 的液体施加于新鲜的角质形成细胞和成纤维细胞时,会驱动典型的 CLE 风格改变:炎症性细胞因子增加,以及降解并重建皮肤支持基质的酶活性上升。通过基因工具沉默 MIF 或用小分子药物阻断它,可显著减少这些有害反应,表明角质形成细胞来源的 MIF 并非旁观者,而是放大 UVB 损伤的关键因子。 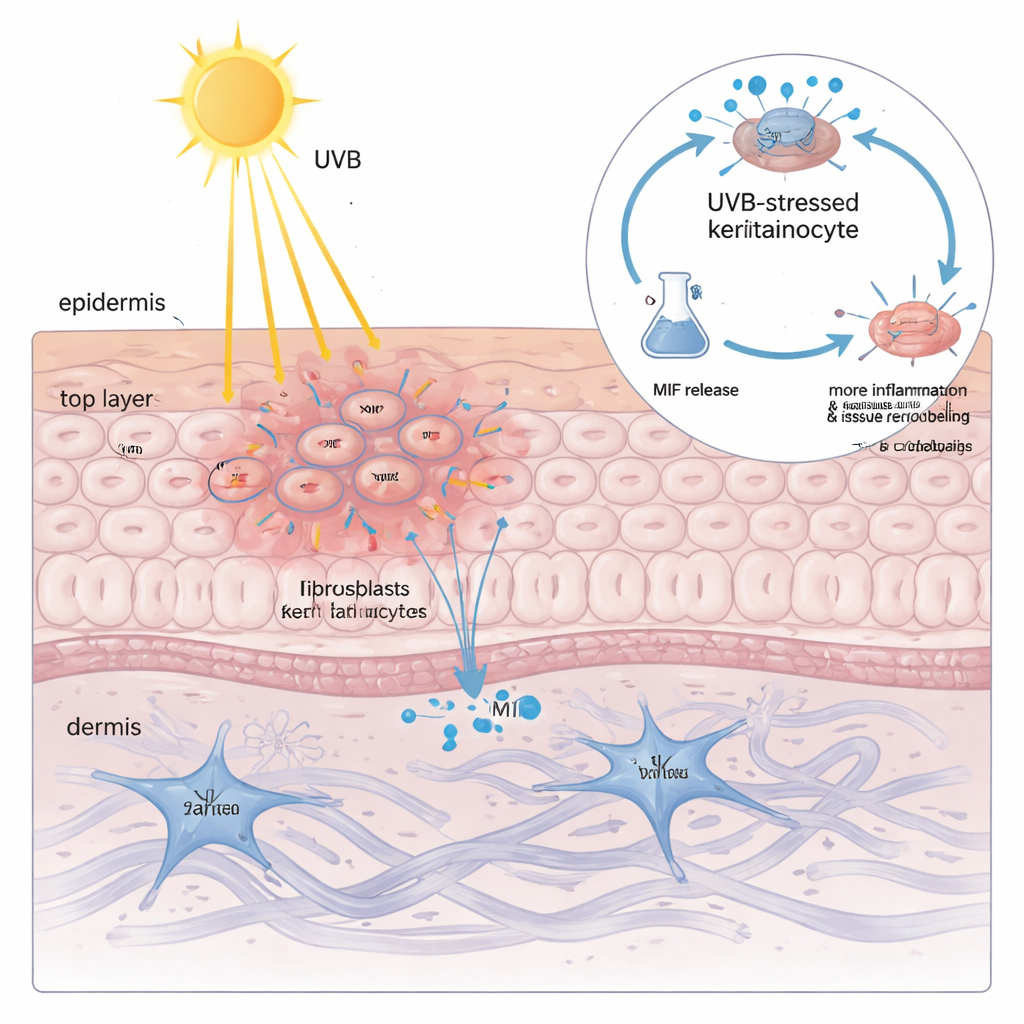
角质形成细胞内的自我维持炎症回路
为了解 UVB 如何促使角质形成细胞释放 MIF,研究者构建了一个“类狼疮”角质形成细胞模型:向细胞内加载自身的 DNA 和 RNA,模拟狼疮中处理不当的遗传碎片。在这一被预激的状态下,UVB 激活了一种所谓的核糖体毒性应激反应:来自核糖体的损伤信号开启了名为 ZAKα 的激酶,进而激活应激酶 p38。该通路提升了另一种蛋白——转录因子 C/EBPβ 的水平,C/EBPβ 结合并激活 NLRP3 基因的调控区。随后 NLRP3 促使形成孔道的蛋白 GSDMD 被切割,GSDMD 在细胞膜上打孔并引发一种称为焦亡(pyroptosis)的炎性细胞死亡。关键是,MIF 主要通过这些 GSDMD 孔道逸出——而非通过正常的分泌囊泡。一旦逸出,MIF 结合角质形成细胞表面的受体 CD74,再次激活 p38、NLRP3 与 GSDMD,从而闭合了一个恶性循环:UVB → p38 → NLRP3 → GSDMD 孔道 → MIF 释放 → 更多 p38 激活。
从分子发现到新的局部治疗
这一回路并非仅是体外实验的奇观。在易患狼疮的小鼠品系中,UVB 曝露导致严重的皮肤病变,表皮中 MIF、p38 激活、NLRP3 和被切割的 GSDMD 水平都很高。当研究者使用基因治疗病毒特异性沉默皮肤中的 Mif 基因时,UVB 诱导的皮疹明显减轻,角质形成细胞和成纤维细胞中的炎症与组织重塑标志也下降。为避免全身用药副作用,他们还设计了可溶解微针贴片,载入 MIF 抑制剂 ISO‑1。将这些微小针片短暂按压在皮肤上,能无痛地将药物传递到上层组织。接受处理的易患狼疮小鼠在 UVB 后的皮损数量和严重程度大幅减少,MIF–p38–GSDMD 回路的分子特征明显被抑制。 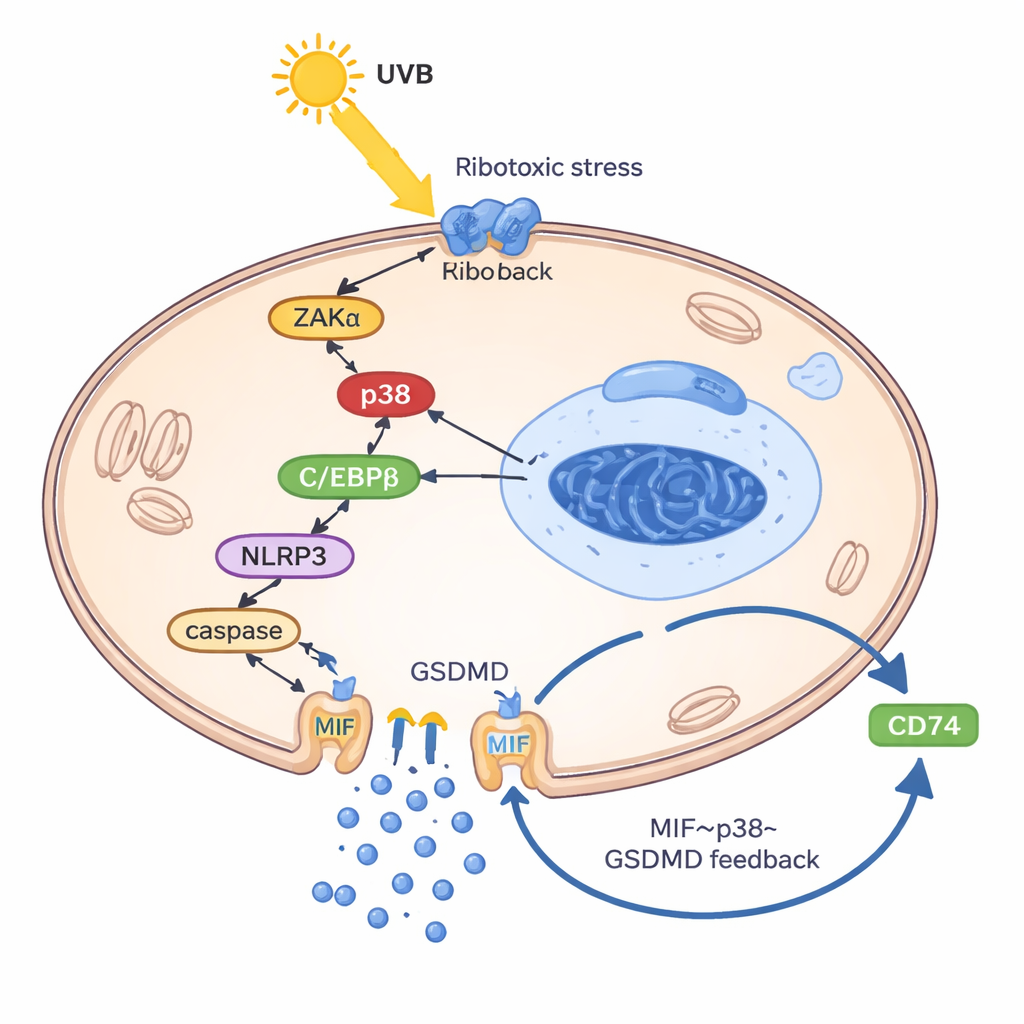
对狼疮患者意味着什么
简而言之,这项工作表明在狼疮中,某些皮肤细胞被“连线”成对 UVB 反应过度,通过自损的膜孔释放出一种强力“放大器”分子 MIF。该放大器随后反馈维持炎症机器的运转,即便初始光暴露已经结束。通过逐步描绘这一回路,研究提示在皮肤局部阻断 MIF——通过基因沉默或像微针贴片这样的智能给药系统——可能切断光敏感性发作的循环,而不会广泛抑制免疫系统。如果类似策略在人类中被证明安全且有效,可能为狼疮患者提供在光照下更舒适生活的新途径。
引用: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
关键词: 皮肤型狼疮, 光敏感, 角质形成细胞, 炎症回路, 微针疗法