Clear Sky Science · zh
SOX21通过抑制AP-1活性遏制胶质母细胞瘤生长
这项脑癌研究为何重要
胶质母细胞瘤是最致命的脑癌之一,原因在于一小部分顽固的“起始”细胞能够维持肿瘤生长并使其在治疗后复发。这项研究揭示了一种脑细胞中天然存在的蛋白SOX21如何通过关闭其DNA内的生长驱动程序来抑制这些危险细胞。了解这一内部的“关闭开关”可能为放慢胶质母细胞瘤进展并提高现有治疗效果提供新思路。
肿瘤内部的隐藏驱动因子
在胶质母细胞瘤中,并非所有细胞都相同。一小部分被称为胶质母细胞瘤前体细胞(GPCs)的细胞表现得像干细胞:它们自我更新、耐受治疗,并能在手术、放疗或化疗后重新播种肿瘤。这些细胞受转录因子网络控制——这些蛋白决定哪些基因处于活跃或沉默状态。一些已知因子,如SOX2和AP‑1家族成员,通常促进生长和存活。相反,SOX21与正常脑干细胞的分裂减少和成熟增加相关,早期研究也暗示它可能对脑肿瘤有保护作用。然而,尚不清楚在已确立的肿瘤中提高SOX21水平是否真的能放缓其生长,以及SOX21在癌细胞内部的具体作用机制。
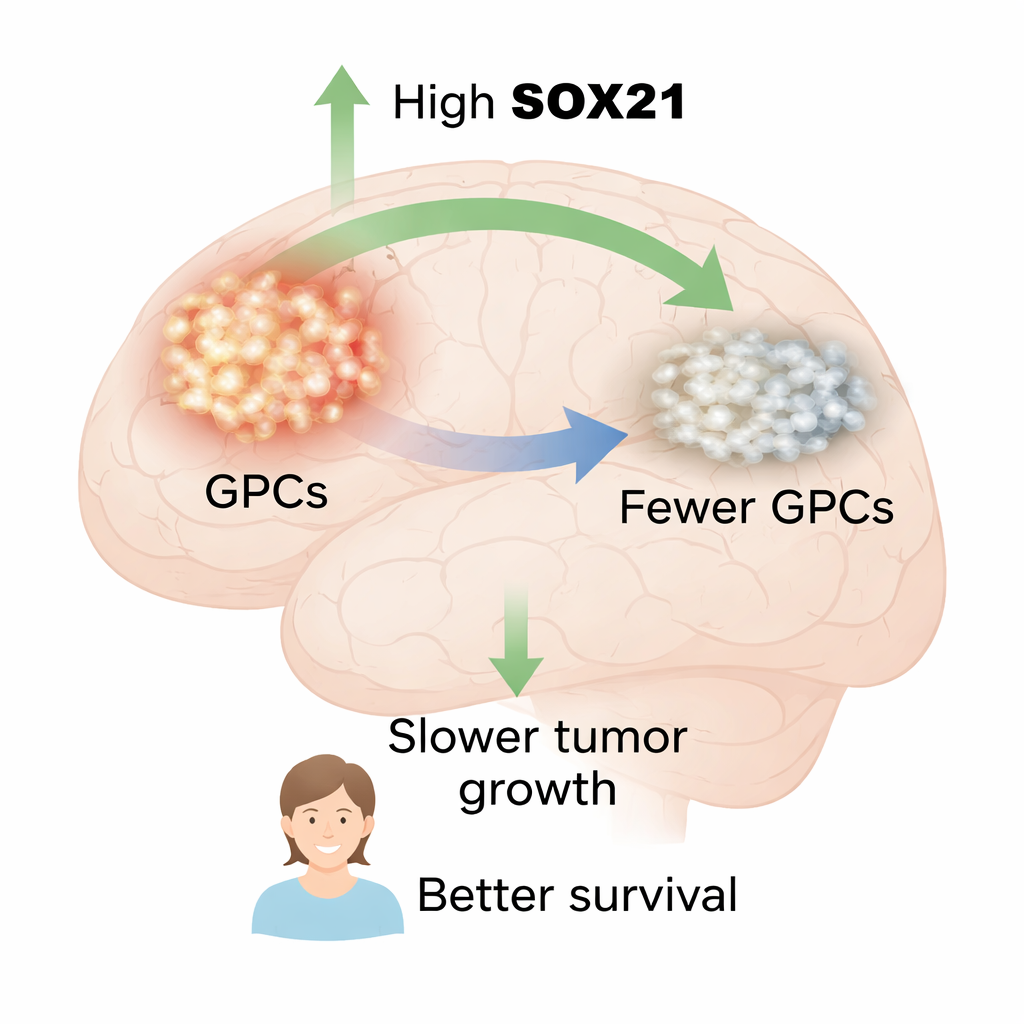
SOX21标志着更好的预后并削弱肿瘤细胞
研究人员首先检查了人类胶质母细胞瘤样本。他们发现SOX21蛋白主要存在于同时带有干样标志物(如SOX2和OLIG2)以及处于活跃分裂状态(由标志物KI67识别)的细胞中。这表明SOX21恰好位于肿瘤的GPC区。随后在大型公开患者肿瘤数据库中,他们比较了SOX21基因活性高与低的患者生存情况。在两个独立队列中,SOX21表达较高的患者生存期明显更长,将SOX21与更良好的病程联系起来。
激活SOX21可放慢生长并降低肿瘤形成能力
为检验因果关系,团队对取自患者肿瘤的GPC进行了工程改造,使其携带可用药物多西环素开启的可切换SOX21基因。当在培养皿中诱导SOX21时,这些细胞分裂减少,掺入的DNA合成标记减少(表明增殖减慢),并表现出更多程序性细胞死亡的特征。它们形成悬浮球体(干样自我更新的测量方法)的能力急剧下降,对标准胶质母细胞瘤药物替莫唑胺的敏感性增加。在小鼠实验中,人源GPC先被允许在脑内建立肿瘤,然后才开启SOX21。在这些条件下,SOX21——而非SOX2——减缓了肿瘤生长,降低了肿块内分裂和干样细胞的比例,并显著延长了动物的存活期。这表明提高SOX21可以作用于已存在的肿瘤,而不仅仅是预防其形成。
SOX21如何解除促癌程序的武装
深入分子机制,作者绘制了SOX21开启时发生变化的基因图谱以及SOX21在DNA上的结合位点。SOX21上调了与细胞周期阻滞和细胞死亡相关的基因,包括肿瘤抑制因子p21,并下调了先前与胶质瘤进展有关的基因,如CDK6、EFNB2、HDAC9以及SOX2本身。值得注意的是,SOX21强烈结合于也被c‑JUN占据的DNA区域——c‑JUN是AP‑1家族的关键成员,通常激活促生长基因。这些共有区域包含典型的AP‑1序列基序以及活性增强子(能增强基因表达的DNA片段)的化学标记。当SOX21水平上升时,这些增强子的可及性下降并失去活化标记,相关基因被抑制。阻断AP‑1的药物复制了SOX21引起的许多基因变化和生物学效应,而强制使细胞过度产生c‑JUN则可以将细胞从SOX21的抑制作用中拯救出来。
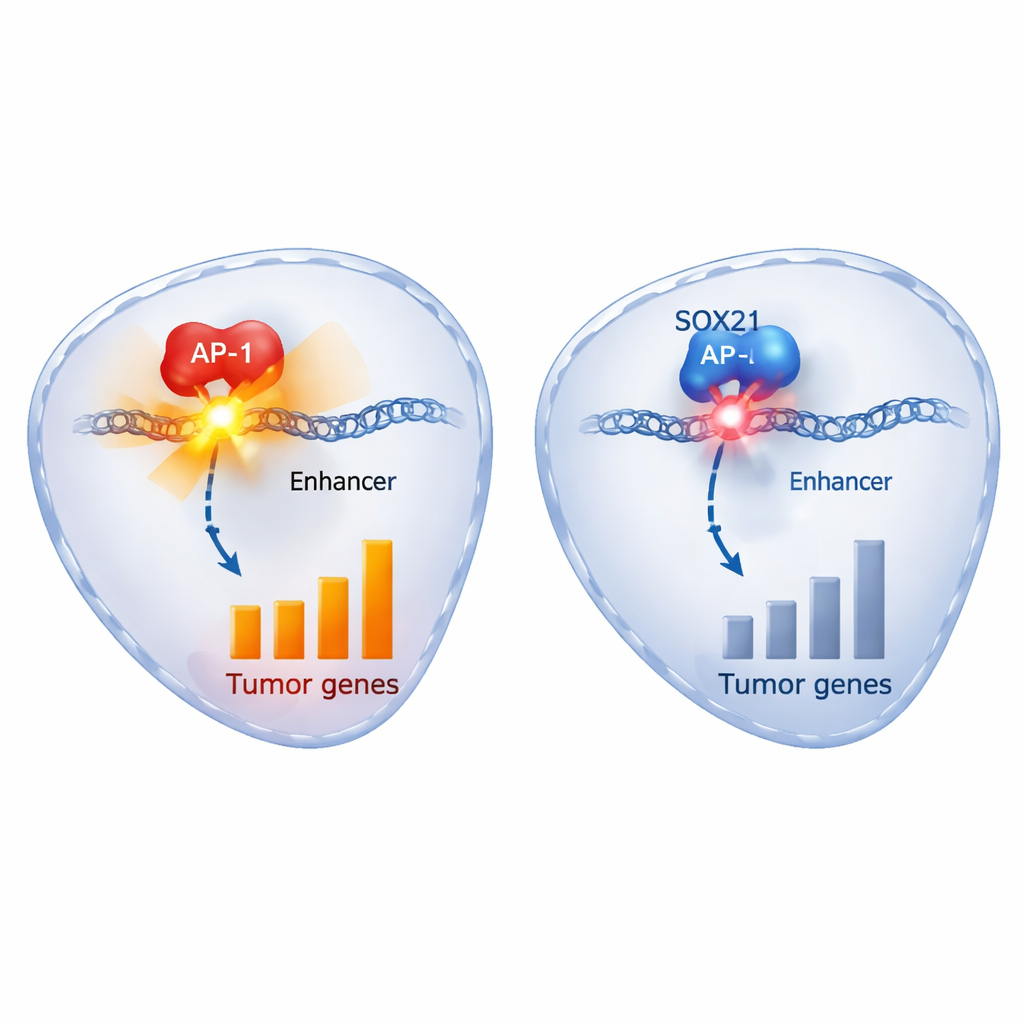
这对未来胶质母细胞瘤治疗的意义
简单来说,SOX21在胶质母细胞瘤最危险的细胞内充当制动器——它与AP‑1用于驱动肿瘤生长的同一DNA开关结合,然后使这些开关变暗。自然产生更多SOX21的患者往往预后更好,在动物模型中,在已确立的肿瘤中开启SOX21可以放慢肿瘤并增强其对化疗的反应。尽管目前还难以直接在患者体内传递或激活SOX21,但其所控制的通路——以及与AP‑1之间的竞争关系——为开发旨在削弱肿瘤干样核心、降低复发风险的新药提供了有希望的切入点。
引用: Rrapaj, E., Yuan, J., Kurtsdotter, I. et al. SOX21 suppresses glioblastoma growth by repressing AP-1 activity. Cell Death Dis 17, 191 (2026). https://doi.org/10.1038/s41419-026-08442-5
关键词: 胶质母细胞瘤, 癌症干细胞, SOX21, AP-1, 脑肿瘤治疗