Clear Sky Science · zh
厚朴酚通过靶向线粒体抑制肿瘤发生与转移
将一种树木化合物变成抗癌利器
许多抗癌药物来自植物,科学家们仍在揭示一些天然分子在细胞内的作用机制。本研究聚焦于厚朴皮中长期用于传统医药的厚朴酚,显示它可以直接作用于癌细胞内的微小能量工厂,从而减缓肿瘤生长并阻断扩散,同时在很大程度上不损害正常细胞。
细胞内部的发电站
每个细胞都依赖线粒体——常被称为细胞的“发电站”——来产生能量分子ATP。在癌症中,线粒体不仅生成燃料,还参与决定细胞的生存与死亡。一个位于线粒体内膜的大型分子机器ATP合酶负责合成ATP。癌细胞常过度表达一个伴侣蛋白IF1,IF1会附着在ATP合酶上,像安全锁一样帮助肿瘤抵抗一种称为线粒体通透性转换的自我毁灭过程以及随后发生的细胞死亡。
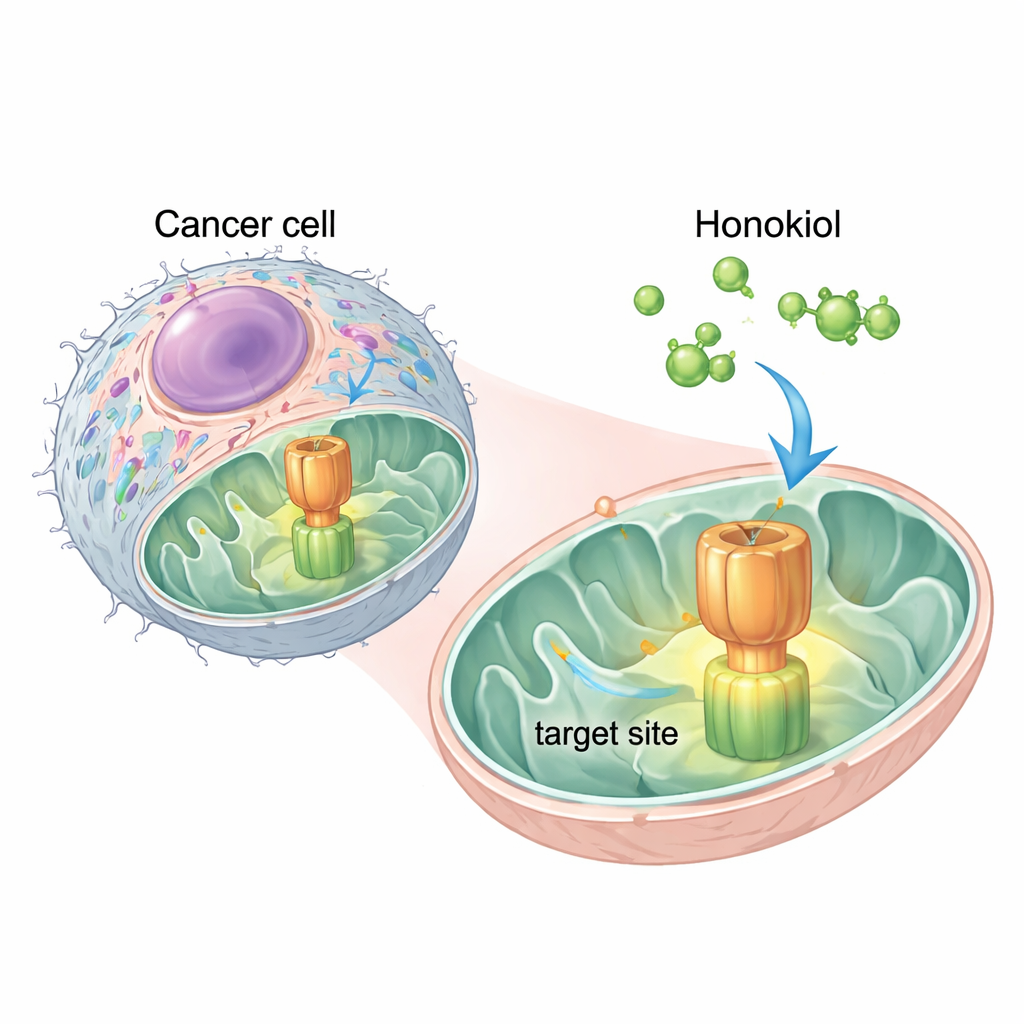
一种天然分子找到关键开关
研究人员使用计算机模拟来预测厚朴酚在ATP合酶上的结合位点。他们在其组成部分之一、称为OSCP的区域发现了两个有前景的“停靠”位点。最强的位点与IF1用来结合ATP合酶的同一片段重叠。这表明厚朴酚可能像一个分子楔子,插入OSCP并将IF1推开。在人类宫颈癌HeLa细胞的实验中证实了这一点:加入厚朴酚后,IF1与OSCP之间的物理接触减少,而酶的其他部分未被破坏,表明该效应具有特异性。
从细胞到活体动物:肿瘤更小、转移更少
为了评估这种分子推力在真实生物体内的影响,团队将带有荧光的人类癌细胞植入小型斑马鱼胚胎——这是一种用于追踪肿瘤生长与转移的成熟全动物模型。在注入含有大量IF1的正常HeLa细胞的鱼体内,厚朴酚处理显著缩小了肿瘤体积并减少扩散到远端区域的癌细胞数量,其表现类似于注入缺失保护性蛋白IF1的敲除细胞的鱼。有趣的是,即便在缺失IF1的情况下,厚朴酚仍降低了转移细胞数,提示存在第二种与IF1无关的限制癌细胞扩散的机制。
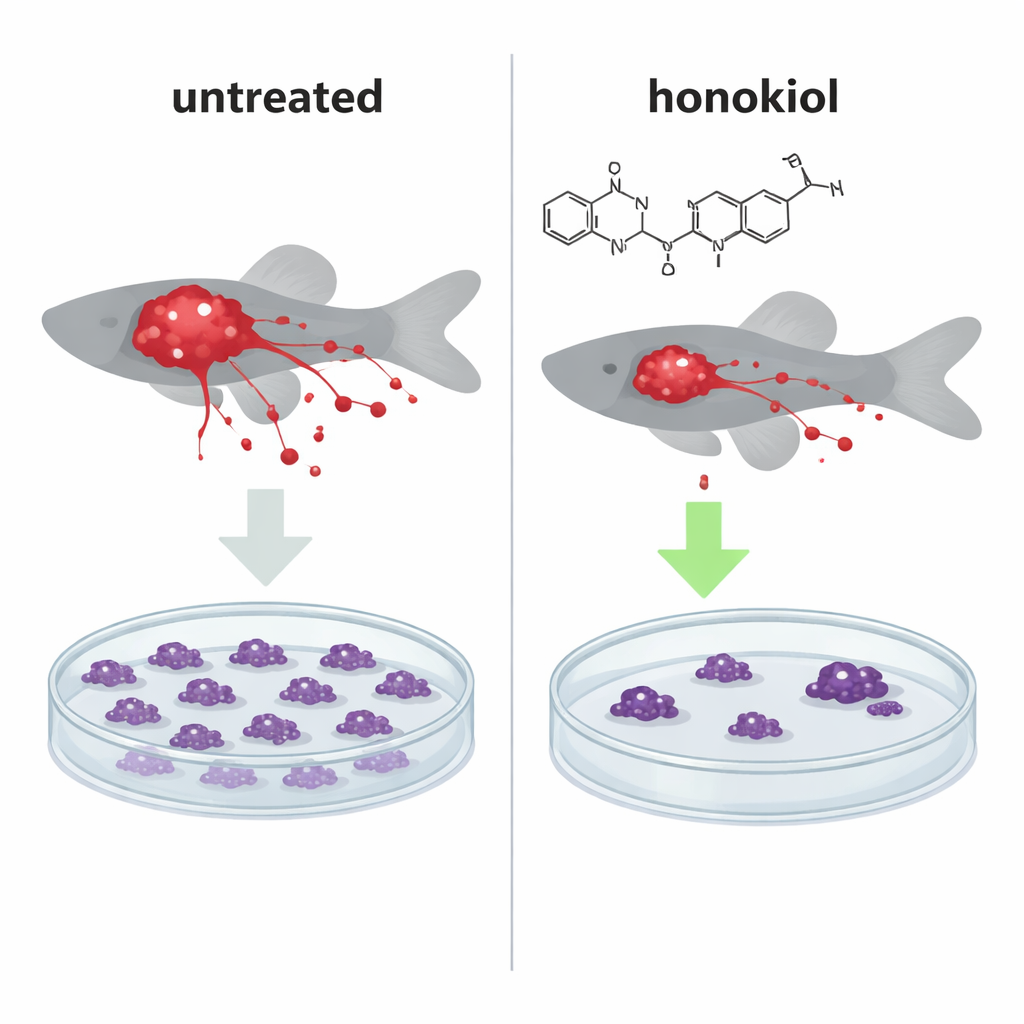
迫使失常的发电站触发自毁
在体外培养中,厚朴酚降低了癌细胞在软琼脂中形成大团簇的能力——这项测试模拟了实性肿瘤内部那种应激、低氧的环境。该现象并非由于正常细胞分裂或基础线粒体呼吸大幅减慢,而是指向线粒体在生死抉择方面的改变。钙处理测量显示,厚朴酚使线粒体在较低钙水平下就打开通透性转换孔,这是引发肿胀及释放促死因子的已知触发因素。在适度剂量下,这一效应依赖于IF1被置换;在较高剂量时,厚朴酚通过其第二个OSCP结合位点并伴随活性氧增多发挥作用,使即便缺失IF1的细胞也更易感受程序性细胞死亡。
阻止癌细胞四处迁移
当癌细胞脱落并迁移到新器官时,癌症才变得最为危险。在伤口样“划痕”实验中,厚朴酚明显减慢了癌细胞层的集体迁移,并降低了上皮‑间质转化的标志物,这一过程使肿瘤细胞具备移动和侵袭能力。电子显微镜的细致图像显示,迁移的细胞通常会增大并重塑线粒体,在内膜上增加皱褶以满足处于前沿的高能量需求。而在厚朴酚处理下,这些前沿线粒体反而肿胀并出现结构性损伤——通透性转换孔打开的特征——而非移动区域的线粒体受影响较小或数量反而增加,这取决于IF1的存在与否。
对未来癌症治疗的意义
简而言之,这项工作表明厚朴酚可以定位到线粒体产能机器ATP合酶的一个小型调控区域,并翻转癌细胞常保持上锁的内置安全开关。通过驱逐IF1并直接推动通透性转换孔朝打开状态移动,厚朴酚促使肿瘤细胞自我毁灭并降低其迁移和播散远端的能力。由于这些效应源自许多癌症共有的特征——而非单一的表面标志——针对ATP合酶OSCP区域的策略有望激发一类新疗法,利用癌细胞发电站的脆弱性,同时将对健康组织的损害降到最低。
引用: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
关键词: 厚朴酚, 线粒体, ATP合酶, 细胞凋亡, 转移