Clear Sky Science · zh
c-Myc/GRPEL1 通过 FASN 维持脂肪酸合成以支持 PDAC 细胞增殖
为什么癌细胞对脂肪的“渴求”很重要
胰腺癌是最致命的癌症之一,部分原因在于其细胞善于重编程自身代谢以求生存和增殖。本研究聚焦于这一故事中令人意外的一环:胰腺肿瘤细胞如何增强其内部的“脂肪工厂”以支持持续的生长,以及阻断这一过程如何可能为患者打开新的治疗途径。
一种具有代谢优势的顽固癌症
大多数胰腺癌属于胰腺导管腺癌(PDAC),通常发现较晚且对现有疗法反应不佳。PDAC 细胞生存在缺氧和营养匮乏的恶劣环境中,但它们通过重构对糖、脂肪及其它燃料的利用来繁荣。线粒体——细胞内的小型发电厂——在这一重编程中起着核心作用。为了维持这些发电厂的运转,细胞持续监控并修复成千上万的线粒体蛋白,这一过程称为线粒体蛋白质量控制。此前尚不清楚这种质量控制机制如何与胰腺肿瘤的能量供应方式相连。
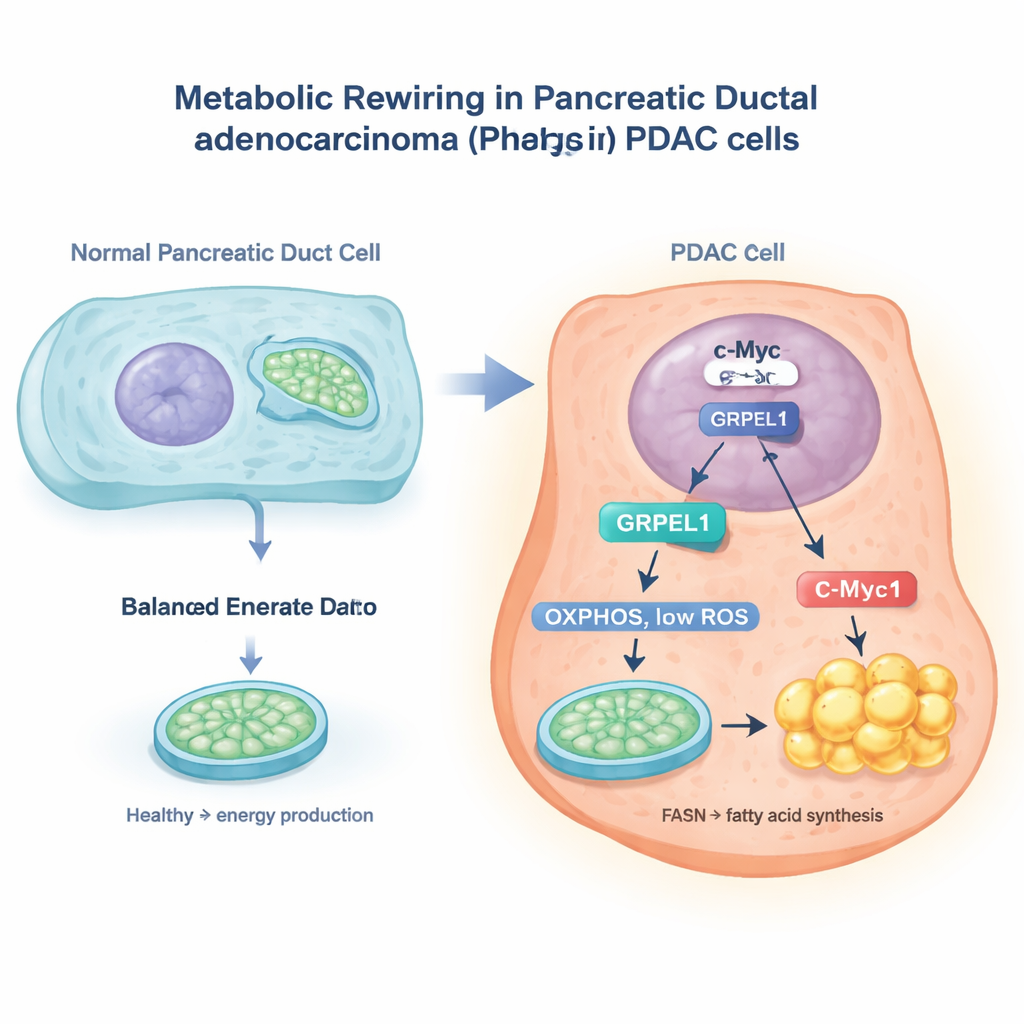
c-Myc 开关与线粒体助手
研究人员利用大型癌症数据库并在胰腺癌细胞中做实验,锁定了一个名为 GRPEL1 的蛋白,它参与线粒体蛋白的处理。研究发现,一种著名的癌基因 c-Myc 在细胞核内像分子开关一样激活 GRPEL1 基因。当 c-Myc 水平下降时,GRPEL1 水平也随之降低;当 c-Myc 增强时,GRPEL1 上升。患者肿瘤样本也显示 c-Myc 与 GRPEL1 往往共同升高,且两者都与较差的预后相关。在体外培养的 PDAC 细胞中,降低 GRPEL1 会减慢细胞分裂和集落生长,而额外补充 GRPEL1 则有助于细胞更快增殖,尤其是在 c-Myc 被抑制的情况下。
从线粒体到脂肪生产
深入研究发现,GRPEL1 的作用不仅限于维持线粒体蛋白的秩序。耗竭 GRPEL1 后,PDAC 细胞的线粒体能量生产效率下降,形态异常,并释放更多反应性氧物种(ROS)——一种有时被称为细胞“生锈”的化学活性副产物。这一 ROS 激增产生连锁反应:它降低了脂肪酸合成酶(FASN)的水平,FASN 是细胞内合成新脂肪的关键酶。FASN 水平下降后,细胞合成的脂肪减少,脂质储存降低,生长受阻。当研究者用抗氧化剂清除 ROS 时,FASN 水平恢复,表明 GRPEL1 与 FASN 之间的联系是由 ROS 驱动的。有趣的是,在该体系中,c-Myc 本身似乎并不直接激活 FASN 基因,而是通过影响 GRPEL1 和引起线粒体应激间接影响 FASN。
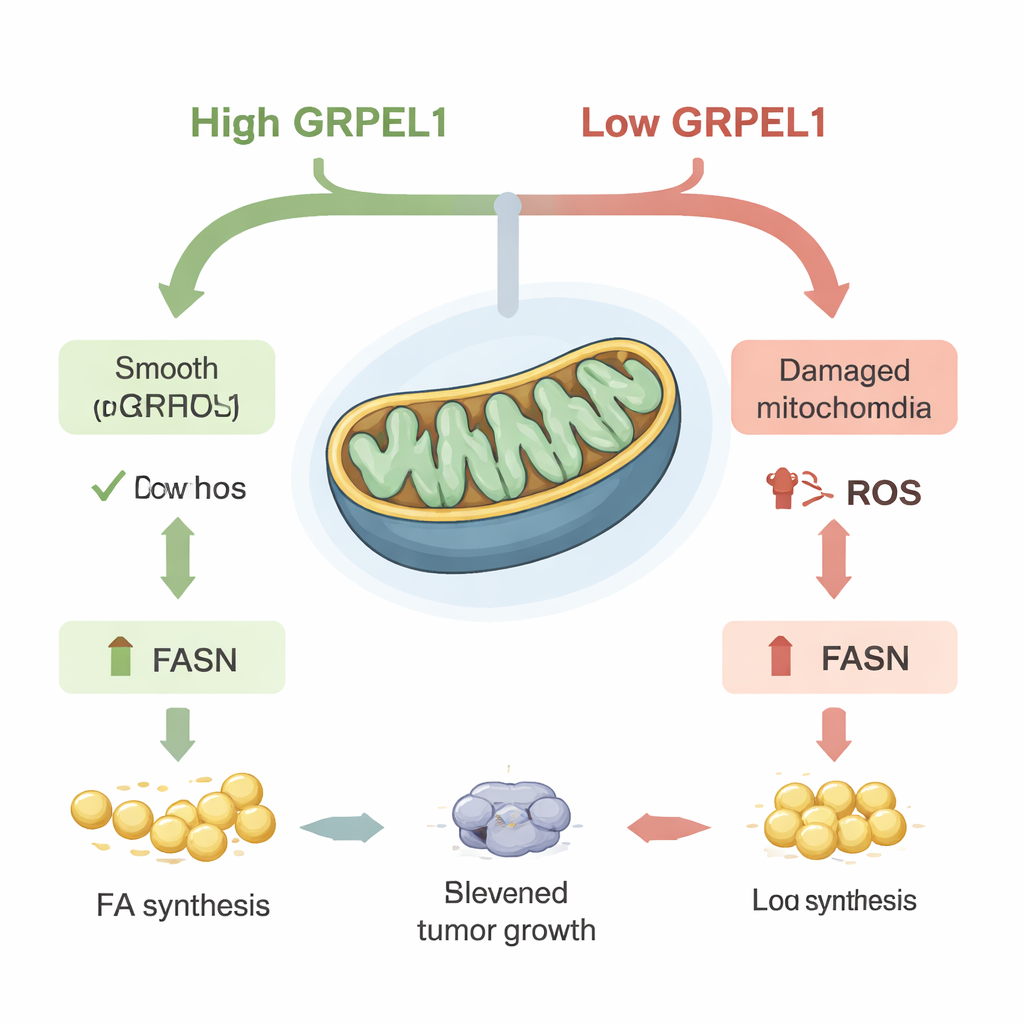
脂肪作为肿瘤生长的燃料
由于 FASN 位于脂肪合成的核心,科学家们探问在 GRPEL1 水平低时恢复 FASN 是否能挽救肿瘤细胞的生长。在细胞培养中,强制表达更多 FASN 部分逆转了因缺乏 GRPEL1 导致的生长和集落形成减慢。在小鼠模型中也观察到类似现象:由 GRPEL1 耗竭细胞形成的肿瘤生长较慢,但重新引入 FASN 能恢复肿瘤大小和脂肪含量。对代谢物和脂质的详细分析显示,当降低 GRPEL1 或 c-Myc 时,许多与脂肪相关的分子广泛下降。重要的是,外源补充游离脂肪酸或脂质混合物能在一定程度上恢复细胞系和来自患者的胰腺癌类器官(3D 培养的迷你肿瘤)的生长,提示主要问题是新合成脂肪的丧失。
将脆弱性转化为治疗策略
总体而言,该研究描绘了一个清晰的图景:在胰腺癌中,c-Myc 提升 GRPEL1,GRPEL1 帮助线粒体平稳运行并抑制 ROS。线粒体环境的这种稳定性使细胞能够维持高水平的 FASN,源源不断合成新的脂肪酸,这些脂肪酸作为膜构建材料、能量储备和生长信号。当阻断 GRPEL1 时,线粒体功能受损、ROS 上升、FASN 下降,癌细胞生长受挫——如果外源提供脂肪,这一影响可被部分弥补。对非专业读者而言,结论是胰腺肿瘤依赖一个由 c-Myc、GRPEL1 与 FASN 驱动的内部“脂肪工厂”回路。在该回路高度活跃的肿瘤中,针对脂肪酸合成轴的药物可能成为一种有前景的新策略,通过“饿死”癌细胞而对正常组织的影响较小。
引用: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
关键词: 胰腺癌, 肿瘤代谢, 脂肪酸合成, 线粒体, c-Myc