Clear Sky Science · zh
突变的 TDP-43 导致轴突运输和糖酵解受损:基于小鼠干细胞来源运动神经元的肌萎缩侧索硬化症(ALS)模型研究
这项研究对 ALS 患者有何意义
肌萎缩侧索硬化症(ALS)是一种致命疾病,会逐渐导致瘫痪,因为它杀死了控制肌肉的神经细胞。大多数患者会出现与一种名为 TDP-43 的蛋白相关的损伤,但科学家仍未完全弄清这种损伤究竟如何伤害运动神经元。本研究使用精心构建的小鼠干细胞模型,识别出由病变相关 TDP-43 导致的一些最早期问题,为未来可能的治疗方向提供线索。
在培养皿中构建运动神经元
为了在可控环境中研究 ALS,研究人员以小鼠胚胎干细胞为起点,将它们诱导分化为运动神经元——那些将信号从脊髓传到肌肉的长而像电缆的细胞。他们在这些细胞中插入了一个额外的人类 TDP-43 基因拷贝,既有正常型,也有携带称为 M337V 的特定 ALS 相关突变的型。一个荧光标签使研究团队能够在细胞内追踪该人类蛋白。培养第20天时,正常型和突变型细胞都已成熟为表达典型标志物、形成分支网络并建立类突触连接的运动神经元,近似模拟了神经系统中的真实神经元。 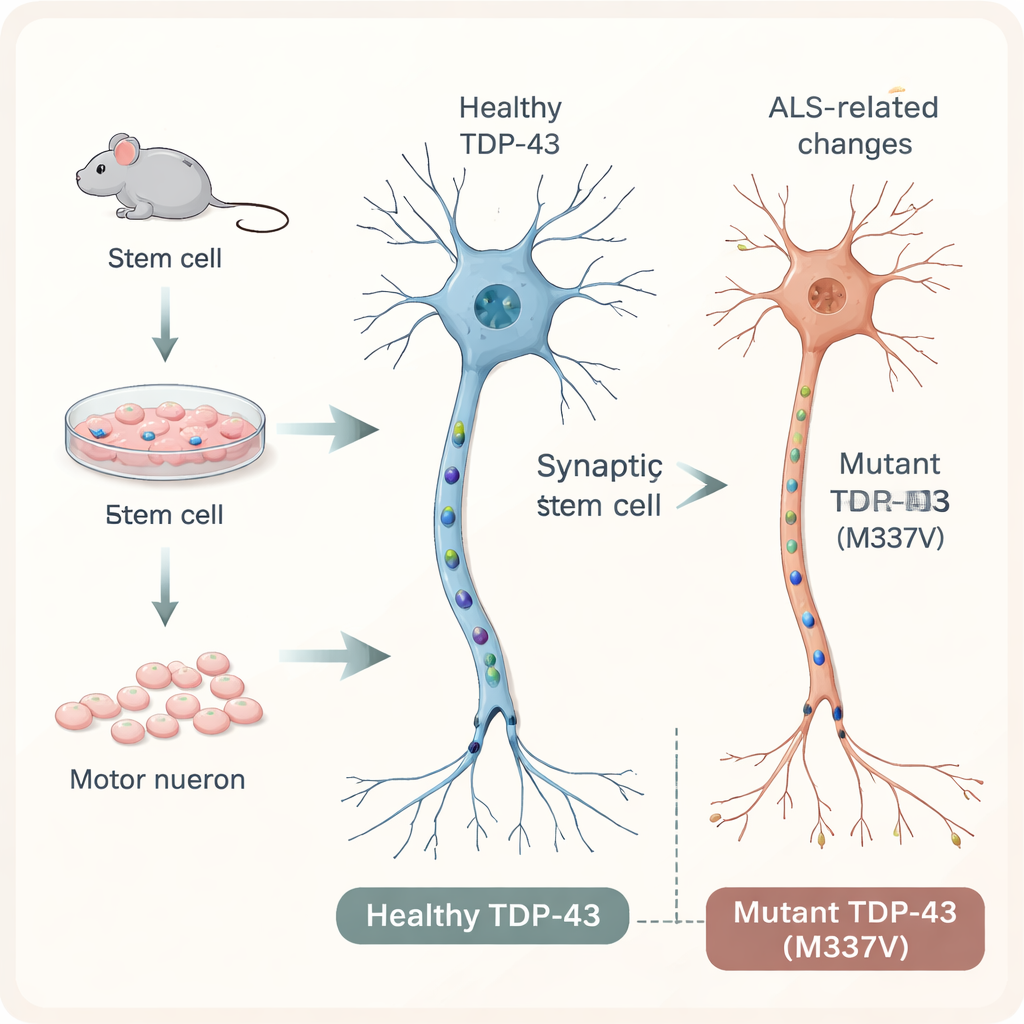
在看不到蛋白团块的情况下出现的隐性损伤
在 ALS 患者中,TDP-43 常从其位于细胞核内的正常位置移动到细胞质,并形成团块,这是一种在显微镜下可见的经典病理标志。令人意外的是,在这个干细胞模型中,突变的 TDP-43 并未比正常型显示出更多的错误定位或聚集。大部分蛋白仍停留在应有的位置。然而,神经元明显更不健康:携带突变蛋白的培养物细胞体更少,神经纤维网络更小,总体存活率降低。这表明在患者大脑和脊髓中可见的明显蛋白团块出现之前,甚至在没有这些团块的情况下,运动神经元就可能已遭受严重损害。
沿神经“高速公路”的交通堵塞
运动神经元依赖快速、高效的运输系统,将重要货物沿其长轴突上下移动。研究团队利用将轴突隔离在微通道内的微流控装置,追踪活细胞中信号传递囊泡(内体)和产生能量的线粒体的运动。在携带突变 TDP-43 的神经元中,这些货物总体上仍朝正确方向移动,但它们行进得更慢。返回细胞体的信号内体速度下降,线粒体在双向移动时均更为迟缓,并有更多时间处于停滞状态。重要的是,驱动这种运动的基础装置——沿内部轨道行走的马达蛋白——的量似乎并未改变,这提示问题可能在于这些装置的功能状态,而非其数量。
糖代谢不足,但线粒体功能并未受损
由于轴突运输耗能很大,研究人员检测了这些神经元如何产生和使用能量。他们测量了两种主要来源:线粒体呼吸(使用氧气燃烧燃料)和糖酵解(分解周围液体中的糖)。线粒体在数量、形态和膜电位上看起来正常,其整体产生能量的能力在突变细胞中似乎没有变化。相反,携带突变 TDP-43 的神经元显示出明显下降的基础糖酵解水平。既往研究表明,轴突局部的糖酵解可以为快速运输囊泡提供“车载”燃料。本研究中观察到的糖代谢能力下降因此可能促成货物运动变慢,为原本脆弱的运动神经元增加额外压力。
对未来 ALS 治疗的启示
总体而言,该研究表明,即便低水平的 ALS 相关突变 TDP-43 也足以使运动神经元更脆弱、减慢轴突上关键货物的运输并削弱其从糖中产生能量的能力——而这些改变并不伴随病理学家通常关注的明显蛋白团块。对非专业读者而言,核心信息是:细胞“交通流”和能量使用的早期、微妙改变可能为 ALS 中更晚期、更剧烈的损伤奠定基础。这突出了轴突运输和细胞能量通路(尤其是糖酵解)作为有前景的治疗靶点,旨在在不可逆退行发生之前保护运动神经元。 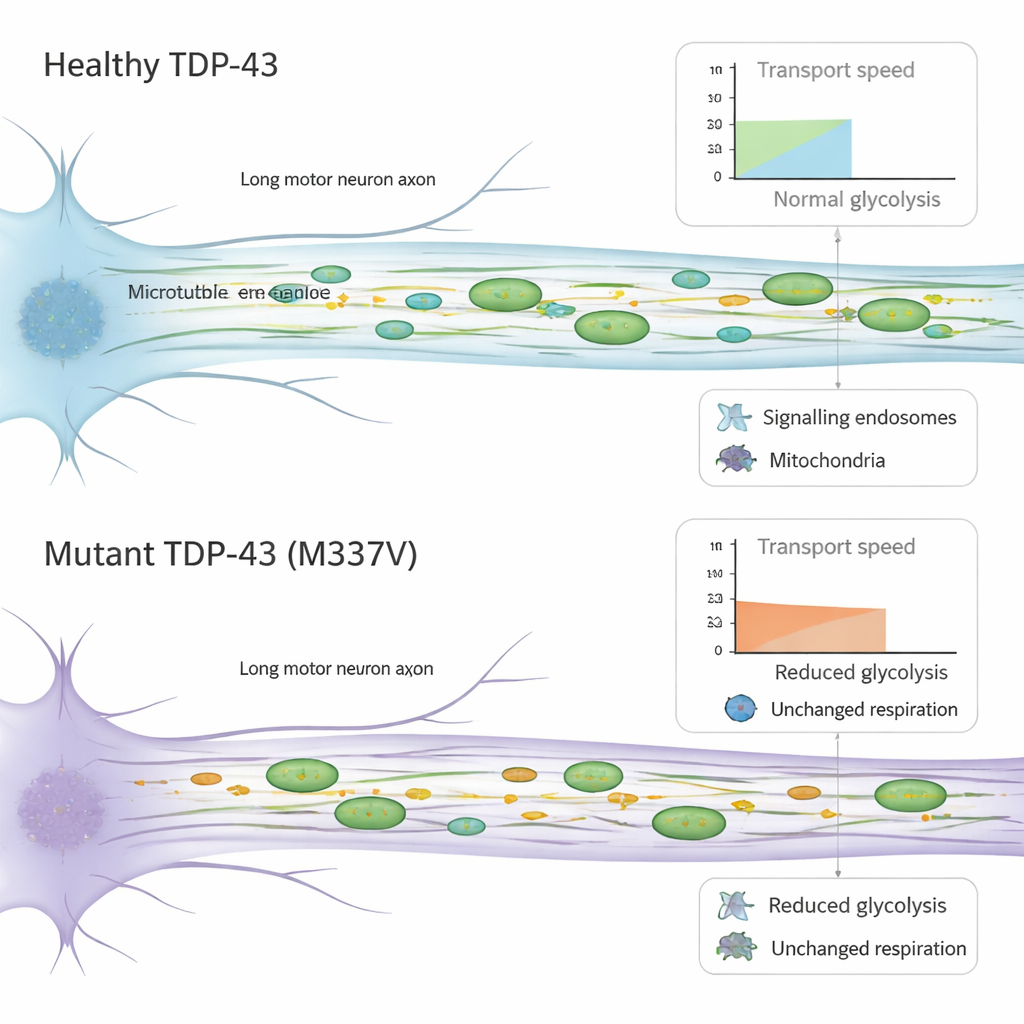
引用: Carroll, E., Scaber, J., Pasniceanu, IS. et al. Mutant TDP-43 drives impairments in axonal transport and glycolysis in a mouse stem-cell-derived motor neuron model of amyotrophic lateral sclerosis (ALS). Cell Death Dis 17, 193 (2026). https://doi.org/10.1038/s41419-026-08437-2
关键词: 肌萎缩侧索硬化症, TDP-43, 运动神经元, 轴突运输, 细胞能量