Clear Sky Science · zh
LAP2α通过减轻复制应激驱动乳腺肿瘤发生
这对乳腺癌为何重要
乳腺肿瘤的生长部分归因于癌细胞在复制DNA过程中找到的各种生存策略。本研究揭示了一种不太为人所知的蛋白质——LAP2α——如何帮助乳腺癌细胞在复制期间保护其DNA,从而促进肿瘤生长并使癌症更难治愈。理解这一隐蔽的支持机制为削弱肿瘤并增强现有药物疗效提供了新的思路。
肿瘤细胞核内的隐秘帮手
每次细胞分裂都必须准确复制其DNA。在癌细胞中,这一过程尤其承受巨大压力:促生长信号持续处于“开启”状态,复制机器被推向极限。这种压力被称为复制应激,会留下大量单链DNA片段,必须由名为RPA的蛋白复合体快速包覆并稳定。研究者此前发现,与细胞核内支架相关的蛋白LAP2α可以与RPA结合并帮助其到达受损DNA。本项研究探问了LAP2α与RPA的这种伙伴关系是否真正助长乳腺肿瘤形成并影响肿瘤对治疗的反应。
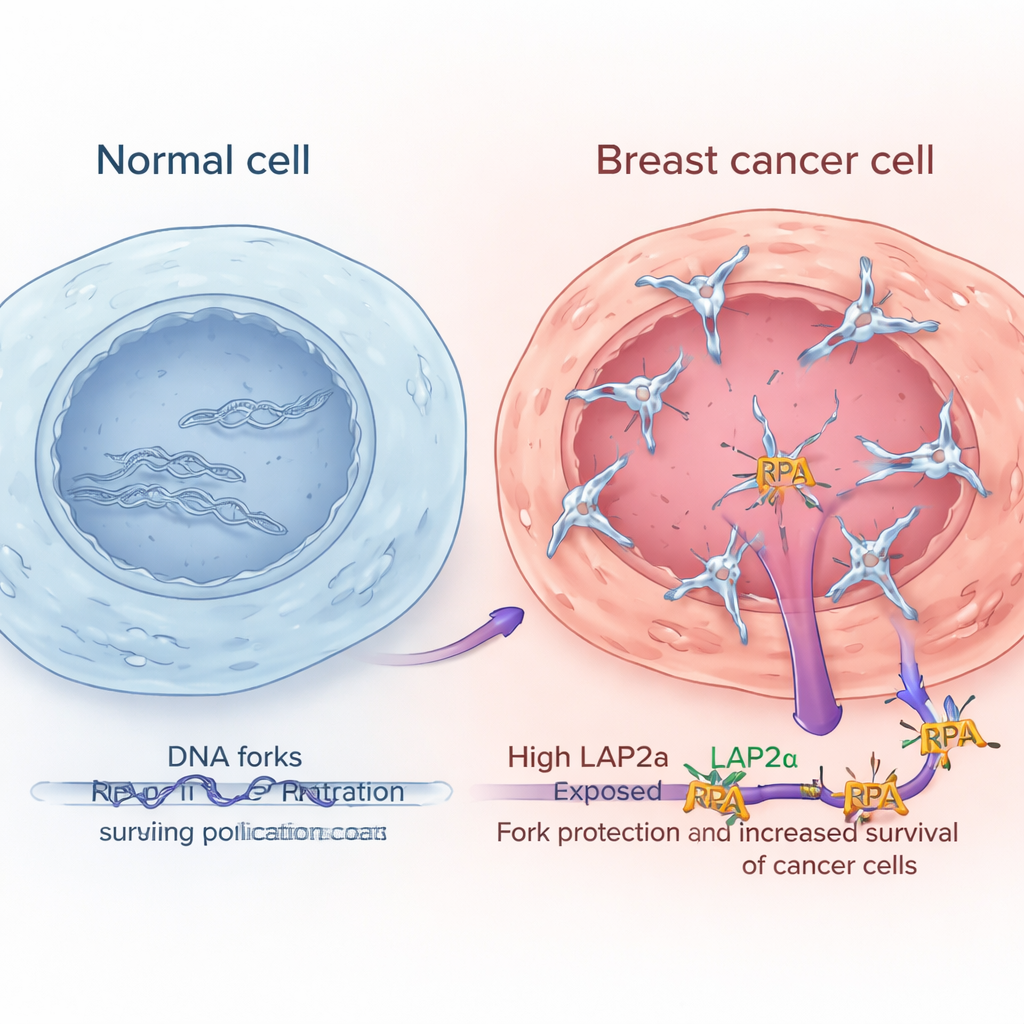
高水平LAP2α标志着更具侵袭性的乳腺肿瘤
通过分析大规模公共基因表达数据集并在显微镜下检查肿瘤样本,研究者证明LAP2α在乳腺癌组织中持续高于邻近正常乳腺组织。其水平随肿瘤分级升高,意味着更异常、更具侵袭性的肿瘤往往具有更多LAP2α。这一模式在多种主要乳腺癌亚型中均有体现,包括激素受体阳性、HER2富集型和三阴性肿瘤。对患者而言,肿瘤中LAP2α水平高的病人通常预后较差。相比之下,RPA的核心成分本身并未表现出类似的变化或与结局的明显关联,这表明帮助癌细胞应对复制应激的是LAP2α功能的增强,而不仅仅是RPA数量的增多。
关闭LAP2α可减缓肿瘤并暴露脆弱点
为超越相关性,研究团队使用了可选择性去除LAP2α的小鼠乳腺癌模型。在乳腺肿瘤形成后,基因删除LAP2α使肿瘤生长变慢并延长了小鼠的存活期。缺失LAP2α的肿瘤细胞分裂减少,并伴随更多的DNA损伤迹象,表现为DNA断裂标志物染色增加和DNA上RPA包覆减少。当这些缺乏LAP2α的肿瘤细胞移植到新小鼠体内时,它们再次形成较小的肿瘤并对损伤DNA的化疗药物(包括铂类药物顺铂和PARP抑制剂)更为敏感。在人的乳腺癌细胞系中进行的类似实验也证实,降低LAP2α使细胞对多种基因毒性药物更脆弱,而恢复正常LAP2α——但不是无法与RPA结合的突变体——则能够恢复DNA保护和药物耐受性。
LAP2α如何帮助保护脆弱的DNA链
为解析机制,研究者在体外重建了DNA结合步骤。他们混合纯化的RPA、单链DNA以及正常的LAP2α或无法与RPA相互作用的变体。结果表明LAP2α直接提高了RPA包覆单链DNA的效率,并帮助RPA展开并稳定这些脆弱区域,起到类似装载辅助或伴护蛋白的作用。当DNA存在时,RPA倾向于离开LAP2α并完全结合单链DNA,表明LAP2α并非最终的保护外衣成分,而是将RPA递送给DNA。如果LAP2α–RPA相互作用失效,会导致更多复制叉崩溃、DNA断裂累积,且癌细胞更易死亡,尤其在化疗诱发额外损伤时。
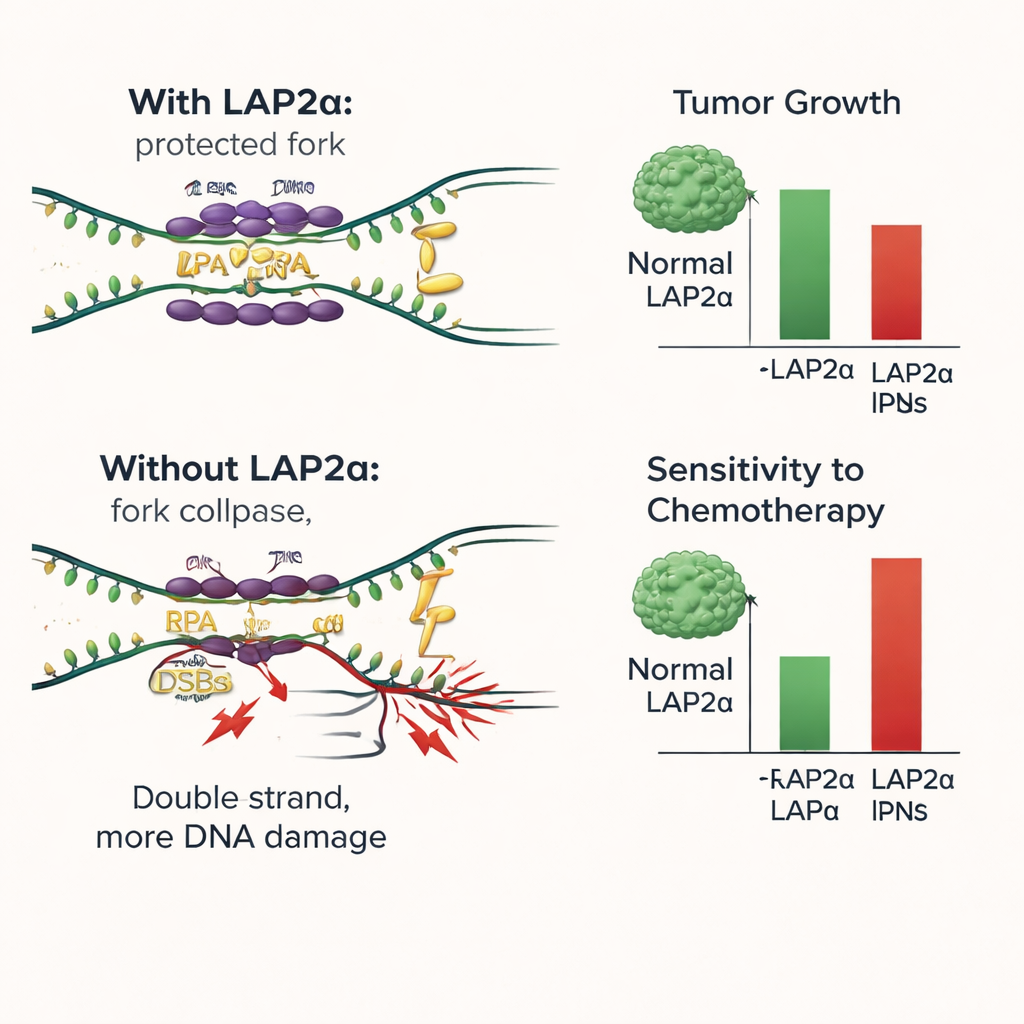
这对未来乳腺癌治疗意味着什么
简而言之,本研究表明LAP2α像舞台幕后助理一样,帮助乳腺癌细胞在复制DNA的压力下存活。通过高效地将RPA装载到脆弱的DNA上,LAP2α减少了损伤并支持持续的肿瘤生长。去除或失活LAP2α会改变这种平衡:DNA损伤积累,细胞停止分裂,攻击DNA的常规药物变得更有效。这些发现表明LAP2α可作为不良预后标志物及新的治疗靶点。阻断LAP2α或其对RPA的结合的药物,可能使现有治疗如铂剂和PARP抑制剂在依赖这一应激缓冲系统的肿瘤中更为有效。
引用: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
关键词: 乳腺癌, DNA复制应激, LAP2 alpha, 复制蛋白A, 化疗敏感性