Clear Sky Science · zh
针对甘油磷脂生物合成可克服由 SLFN11 缺失驱动的尤文肉瘤化疗耐药性
这项研究对儿童癌症为何重要
尤文肉瘤是一种罕见但侵袭性的肿瘤,主要发生在儿童和青少年。许多患者对化疗最初反应良好,但对于那些肿瘤复发的病人,现有治疗常常无效。本研究提出了一个紧迫的问题:当尤文肉瘤细胞对化疗产生耐药时,细胞内部发生了哪些改变帮助其存活——这些改变能否被转化为医生可针对的新弱点?
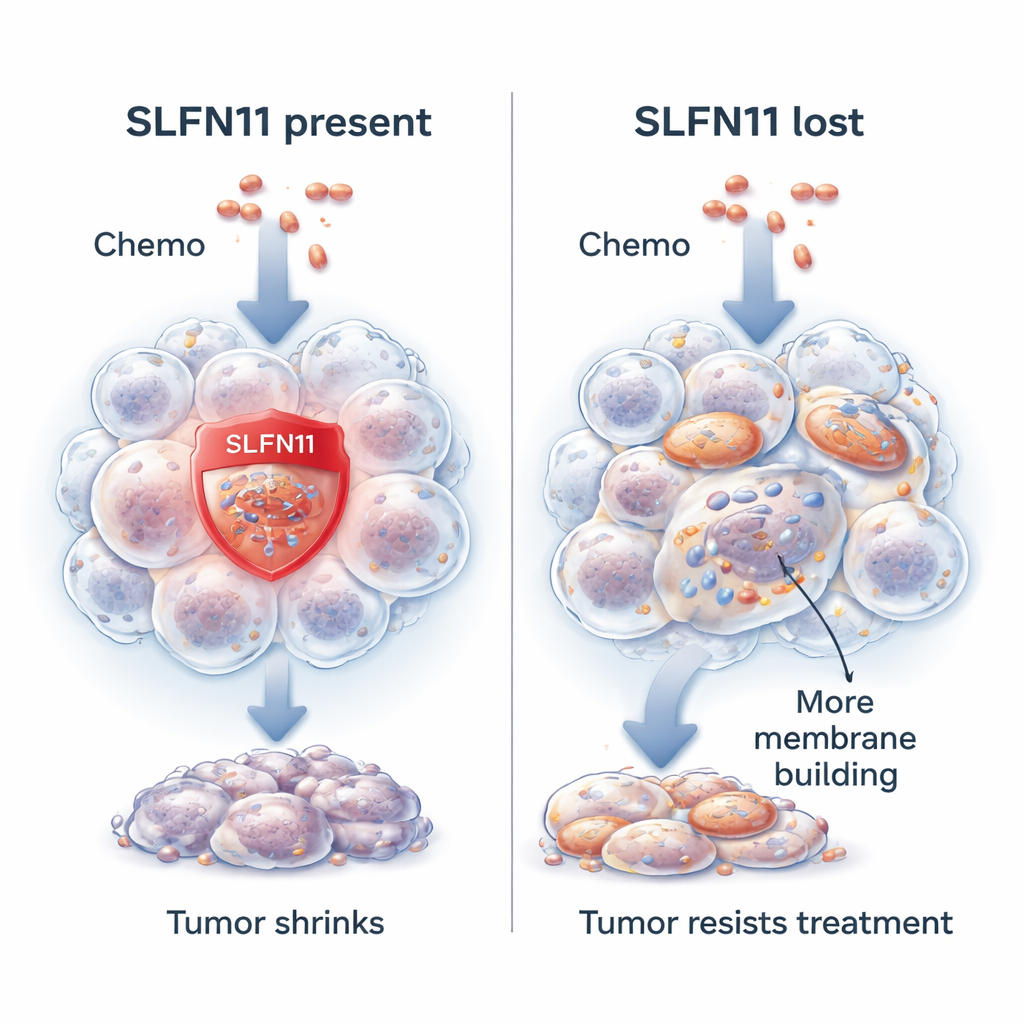
使癌细胞更易被杀死的基因
研究人员关注一个名为 SLFN11 的基因。在许多尤文肉瘤肿瘤中,SLFN11 高表达,使癌细胞对损伤 DNA 的药物更加敏感。当给予这些药物时,SLFN11 有助于抑制 DNA 修复并促使癌细胞走向死亡。肿瘤中 SLFN11 水平较高的患者通常生存期更长、对治疗反应更好。然而,大约十分之一的肿瘤要么从一开始就表达很低或不表达 SLFN11,要么在治疗过程中失去该基因的功能。发生这种情况时,同样的化疗药物效果大打折扣,但这些癌细胞仍然能够正常生长。
癌细胞如何重编排燃料和脂质的利用
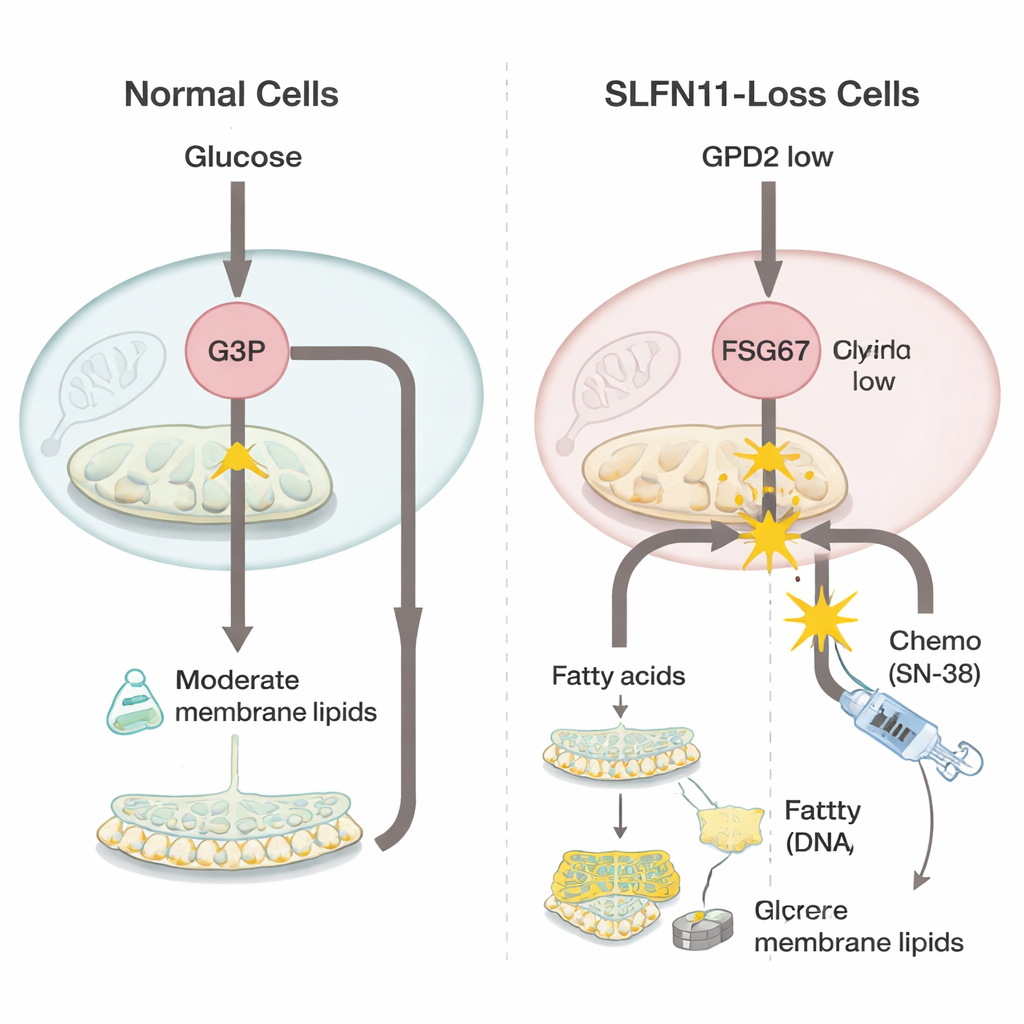
为了解 SLFN11 丧失后发生了什么,研究团队使用强大的“组学”工具比较了有无该基因的尤文肉瘤细胞,这些工具可同时测量数千个基因和小分子。他们发现缺失 SLFN11 的细胞降低了线粒体中一种名为 GPD2 的酶的表达,该酶通常参与将甘油‑3‑磷酸作为能量产生的一部分氧化。当 GPD2 降低时,甘油‑3‑磷酸在细胞中积累。多余的这种前体不会被浪费,而是被转向用于合成构成细胞膜的更多脂类分子——即甘油磷脂类。细胞还显示出合成更多更具柔性的、不饱和脂肪的迹象,这类脂质可帮助快速生长的肿瘤适应压力。
将生存技巧转化为弱点
由于这些缺乏 SLFN11 的细胞更依赖膜构建,科学家们测试了阻断这一过程是否能恢复化疗敏感性。他们使用一种名为 FSG67 的化合物,它抑制甘油磷脂生成途径中的关键步骤。单独使用时,标准的损伤 DNA 药物 SN‑38 在 SLFN11 缺失的细胞中活性显著下降,反映了临床上耐药的问题。但当 SN‑38 与 FSG67 联用时,先前耐药的细胞受到更强的打击,且两药联用的效果优于各自作用的简单相加。相比之下,在仍然表达 SLFN11、对 SN‑38 已高度敏感的细胞中,加入 FSG67 附加益处有限,甚至可能略有不利。这一模式表明,对脂质和膜合成的新依赖性是耐药、SLFN11 低表达状态特有的。
一种可能的无创难治肿瘤信号
研究人员接着探讨这种代谢重编程能否在实际肿瘤中被检测到,而不仅限于细胞培养。他们在小鼠体内培育有或无 SLFN11 的尤文肉瘤,并用核磁共振(NMR)分析肿瘤提取物的化学成分。缺失 SLFN11 的肿瘤显示两种含胆碱分子(与膜周转相关):磷酰胆碱和甘油磷酰胆碱的比值更高。较高的磷酰胆碱/甘油磷酰胆碱比在其它癌症中与更具侵袭性和更差的治疗反应相关。由于胆碱信号可以用先进成像技术测量,这类变化未来有可能作为一种无创标志,用来提示那些已采用这种耐药性膜构建代谢模式的尤文肉瘤。
这对未来治疗可能意味着什么
总体而言,该研究显示,当尤文肉瘤细胞失去 SLFN11 并对损伤 DNA 的化疗变得不敏感时,它们通过代谢重编程向合成更多膜脂倾斜来进行补偿。这一转变不仅有助于细胞存活,还创造了新的阿喀琉斯之踵。用类似 FSG67 的药物阻断甘油磷脂生成可以部分恢复这些耐药细胞对化疗的敏感性。尽管 FSG67 本身尚未成为临床用药,这项工作指向了一种策略:未来医生或可依据肿瘤的 SLFN11 状态及代谢特征来配对治疗,将损伤 DNA 的疗法与针对脂质和膜合成的特异性抑制剂联用,以克服耐药性。
引用: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
关键词: 尤文肉瘤, 化疗耐药, SLFN11, 癌症代谢, 脂质生物合成