Clear Sky Science · zh
靶向低氧诱导的外泌体IGFBP2可克服胶质母细胞瘤中的CD47介导免疫逃逸
为何切断肿瘤氧气反而可能适得其反
医生早已知道,致命的脑癌胶质母细胞瘤常在缺氧区域生长。这些低氧空腔使肿瘤更难治疗。本研究揭示了低氧如何帮助癌细胞躲避免疫系统,并提出了一种新的联合治疗策略,可能使肿瘤更容易被机体清除。
一种能躲避我们防御系统的致命脑肿瘤
胶质母细胞瘤是成年人中最具侵袭性的常见脑肿瘤,典型生存期以数月计。尽管免疫细胞可以浸润这些肿瘤,癌细胞却常常逃脱被清除。其中一个关键逃逸途径是细胞表面的蛋白CD47,常被称为“别吃我”信号,它告诉邻近的免疫细胞(如巨噬细胞)不要吞噬并清除肿瘤细胞。针对CD47的药物已经进入临床试验,但在实体瘤如胶质母细胞瘤中疗效参差不齐,说明肿瘤微环境中的其他因素可能在削弱这些疗法。
低氧区与微小的癌细胞包裹体
研究者使用单细胞RNA测序绘制了来自胶质母细胞瘤不同区域的数千个细胞图谱,比较了肿瘤低氧的核心与外缘。他们在低氧核心中发现了一种特别具侵袭性的细胞亚型——类间质GBM细胞,该亚型高表达CD47和一种名为IGFBP2的蛋白。与此同时,他们发现这些核心细胞释放大量纳米级囊泡,称为外泌体,这些外泌体在表面携带IGFBP2。由于外泌体能在脑内甚至进入血液循环,它们可以将信号传播到远离产生地点的区域。 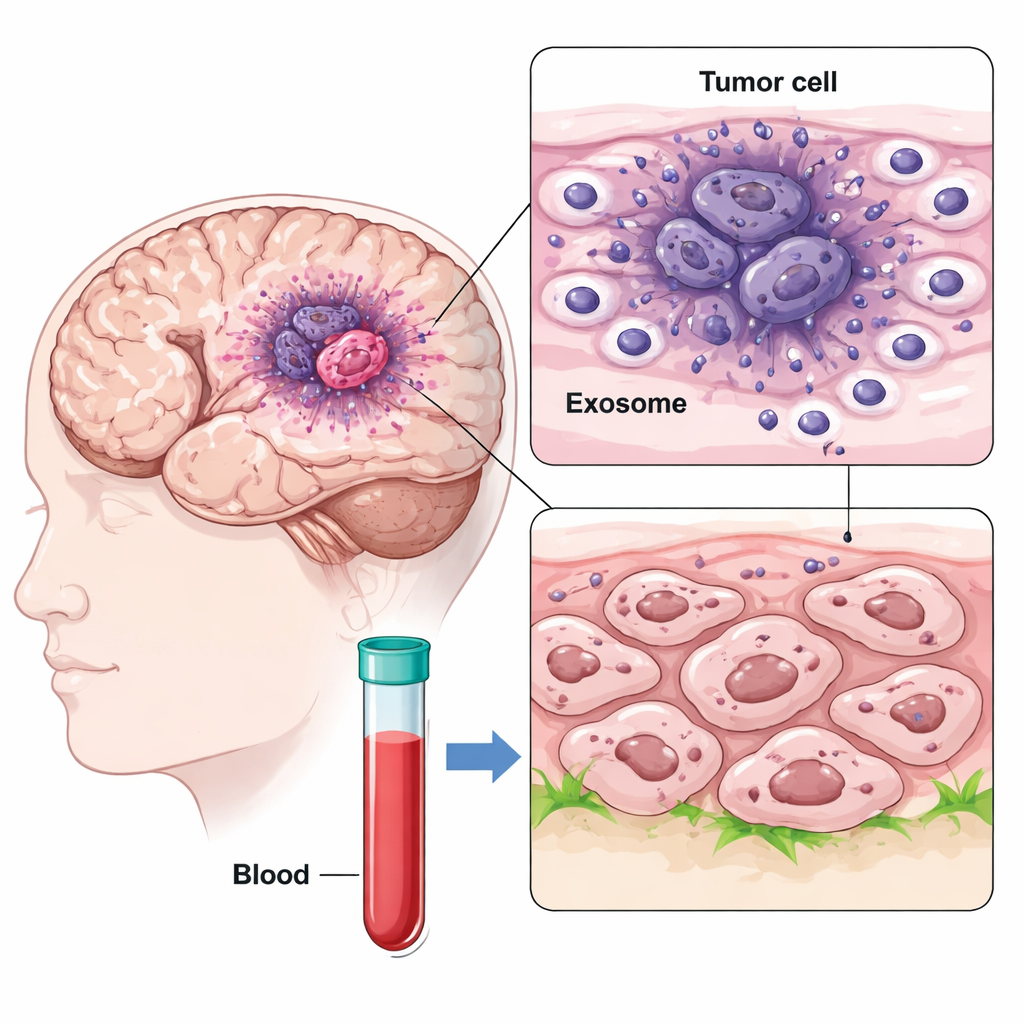
伴侣蛋白如何增强“别吃我”信号
团队随后探究了IGFBP2的功能。他们证明在低氧条件下,低氧感应蛋白HIF-2α在肿瘤细胞中激活IGFBP2基因。IGFBP2随后与外泌体表面的整合素受体结合,装饰在外膜上。当这些被IGFBP2修饰的外泌体与其他肿瘤细胞融合时,会在细胞内激活一系列涉及FAK和STAT3等蛋白的信号通路。该级联反应最终增加肿瘤细胞表面的CD47表达,加强对巨噬细胞的“别吃我”信号,进一步保护癌细胞免受免疫攻击。 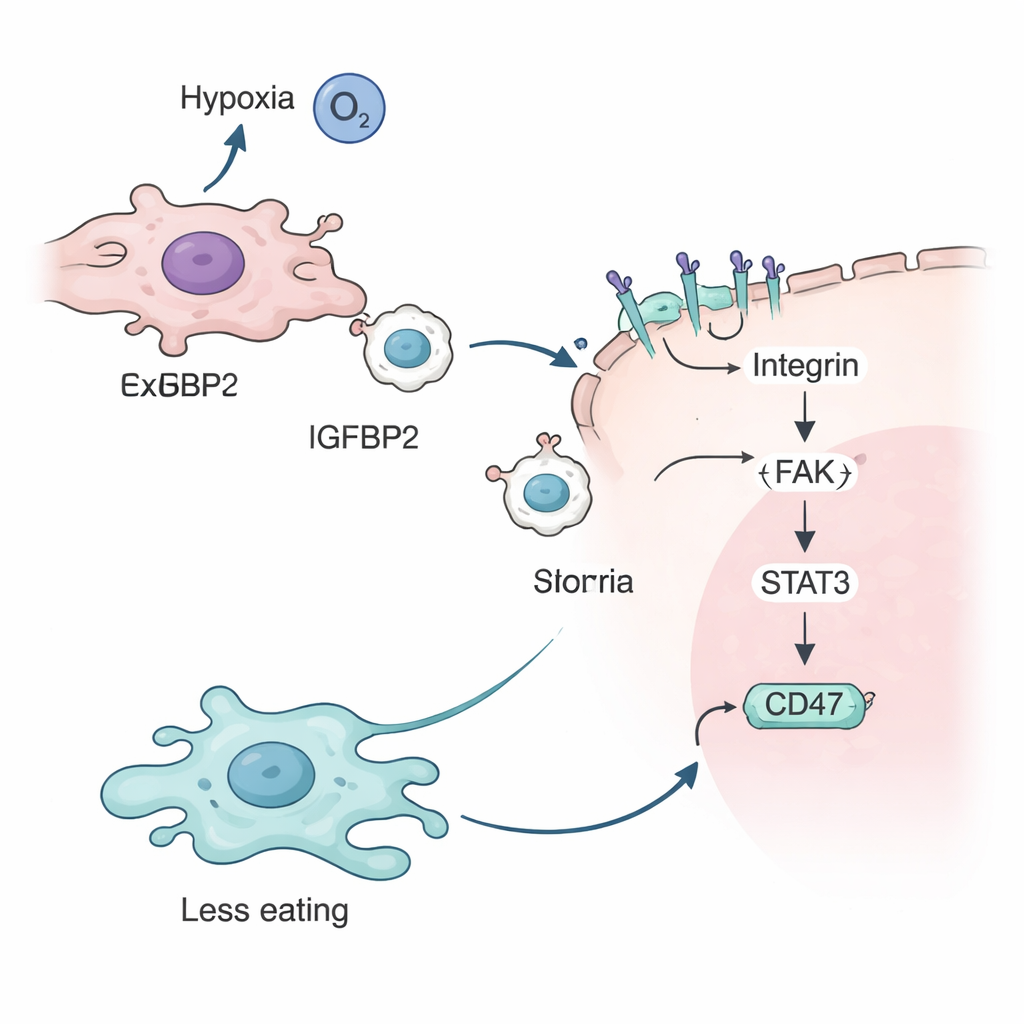
来自患者样本和动物模型的证据
为将这些实验室发现与真实疾病联系起来,研究者检查了胶质瘤患者的肿瘤组织和血液。他们发现,病情更先进的患者在肿瘤组织和血液外泌体中均显示出较高的IGFBP2水平,提示IGFBP2阳性的外泌体可能作为肿瘤分级的血液标志物。在小鼠模型中,降低胶质母细胞瘤细胞中的IGFBP2使其更容易被巨噬细胞吞噬,减缓肿瘤生长并延长存活期。相反,补充含高量IGFBP2的外泌体则提升了CD47水平,减少免疫细胞吞噬并加速肿瘤进展。
有希望的双管齐下治疗策略
最后,团队检验了阻断IGFBP2是否能增强针对CD47的疗法。在带有脑肿瘤的小鼠中,同时使用针对IGFBP2和CD47的抗体治疗,比单独任一治疗产生了更强的巨噬细胞活性、更小的肿瘤和更长的存活期。通过切断由低氧驱动的IGFBP2信号并直接阻断CD47的“别吃我”信号,这种联合疗法从两个方向破坏了肿瘤的免疫伪装。对患者而言,这些发现表明检测血液外泌体中的IGFBP2或可帮助识别最可能从CD47免疫疗法中获益的人群,并且将IGFBP2抑制剂与CD47抑制剂配对,可能比单用任何一种药物对抗胶质母细胞瘤更为有效。
引用: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
关键词: 胶质母细胞瘤, 外泌体, 免疫逃逸, CD47, 低氧