Clear Sky Science · zh
p16介导的G0/G1细胞周期停滞导致SASP和Fuchs角膜内皮营养不良中的纤维化
为何这种眼病重要
随着年龄增长,一种鲜为人知但会威胁视力的疾病是Fuchs角膜内皮营养不良(FECD),它会慢慢使眼睛本应清澈的前窗变得混浊。本文探讨了角膜内表面的某些细胞为何随时间衰竭并形成瘢痕,以及为何女性更易受累。理解这些隐蔽变化可能为开发延缓甚至阻止角膜移植的药物铺平道路。
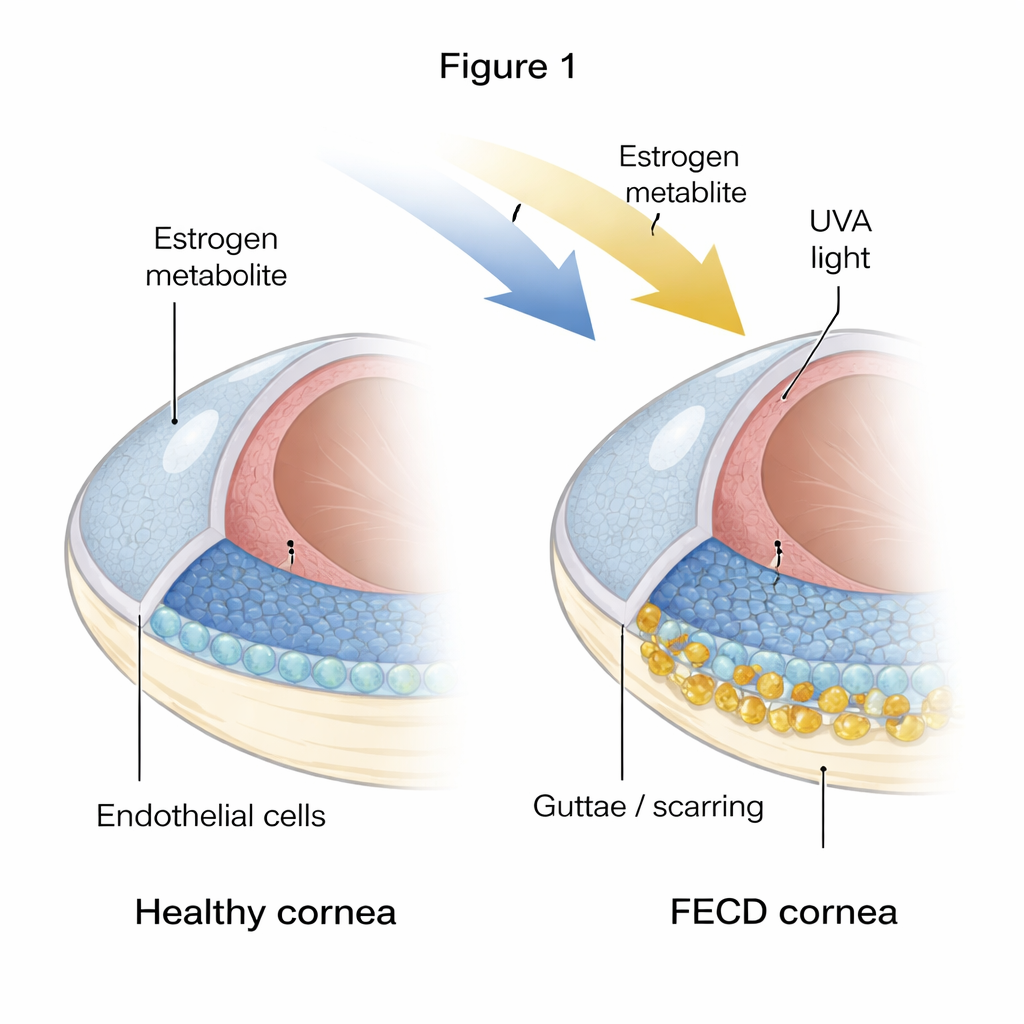
角膜脆弱的内层
角膜必须保持精确的脱水状态以维持透明性,这项工作由一层六边形的细胞——角膜内皮细胞来完成。在FECD中,许多此类细胞死亡,细胞层变得不连续且不规则。同时,内表面会积累称为guttae的硬结和增厚的细胞外基质。作者将健康供体角膜与FECD患者角膜比较,发现病变组织有明显的“老化”和纤维化特征:细胞表现出衰老标志(永久性关闭状态)和纤维化标志(细胞更像成瘢痕细胞并沉积额外基质)。
慢性光照和激素应激将细胞推入死胡同
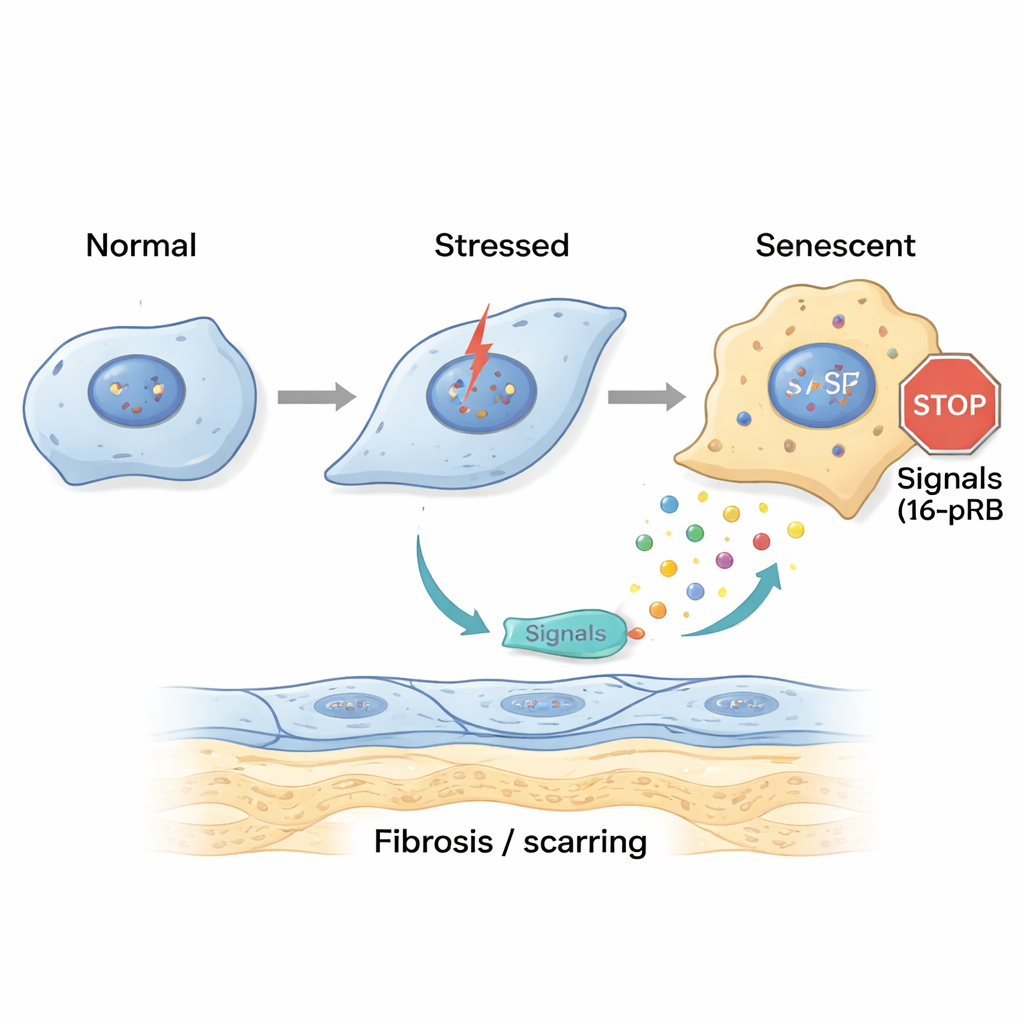
为探究损伤如何起始,研究者在实验室中重现了类似FECD的应激。他们将健康的角膜内皮细胞暴露于长波紫外线(UVA)和4-羟基雌二醇(一种与DNA损伤相关的氧化雌激素代谢物)。短时一次性刺激使细胞在细胞周期的晚期暂时停滞并开始向更像成纤维细胞的状态早期转变,但仍保留一定的恢复能力。相反,反复的慢性暴露将细胞推向另一种状态:它们堆积在称为G0/G1的早期细胞周期阶段并激活p16基因,p16通过其合作蛋白pRB锁定细胞周期。这些细胞变得体积大、扁平,明确呈现衰老表型,同时强烈表达纤维化标志和构成FECD中增厚guttae的蛋白质。
衰老细胞释放有害信号并传播瘢痕化
衰老细胞并非静默无为;它们分泌一种被称为衰老相关分泌表型(SASP)的信号分子混合物。团队收集了受压应激角膜细胞的培养液,并将其施加到新鲜细胞和健康供体角膜上。“急性”SASP引起早期的细胞形态改变,而“慢性”SASP则将许多细胞推入衰老,并上调与纤维化和额外基质沉积相关的基因。详细检测显示,慢性SASP富含炎症性介质,如IL-8和IL-17,这些因子已知促进细胞老化、纤维化瘢痕形成和免疫细胞募集。当研究者阻断IL-17通路或IL-8受体CXCR2时,暴露于慢性SASP的细胞显示出更少的衰老标志和较低的纤维化,表明这些信号是疾病的关键驱动因子。
清除衰老细胞以保护视力
由于p16阳性的衰老细胞与瘢痕密切相关,作者测试了清除它们是否能保护角膜。在一个UVA光诱发FECD样改变的小鼠模型中,他们使用一种消 senolytic药物组合达沙替尼(Dasatinib)和槲皮素(Quercetin)治疗动物,该组合选择性杀死衰老细胞。与未治疗小鼠相比,经消 senolytic治疗的小鼠保持了更规则的内皮细胞镶嵌,整体保留了更多细胞,并显示出更少的衰老、纤维化和过量基质的标志。换言之,清除最受损的细胞减轻了有害分泌物的负担,有助于维持更健康的角膜表面。
这对FECD患者意味着什么
对于患者而言,当视力变得过于模糊时,FECD通常导致需要角膜移植。该研究提示另一条路径:疾病可能由受压应激的、不能分裂的细胞缓慢积累驱动,这些细胞既不能履行职责,又通过炎症和纤维化信号主动毒害邻近细胞。靶向这些信号(如抑制IL-17或IL-8通路),或使用消 senolytic疗法选择性去除状况最差的细胞,或许有一天能延缓瘢痕形成,保留更多天然组织,从而推迟或减少手术需求。
引用: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
关键词: Fuchs营养不良, 角膜内皮, 细胞衰老, 纤维化, 消 senolytic治疗