Clear Sky Science · zh
酸性肿瘤微环境中SLC26A3的乳酰化促进结直肠癌的恶性进展
为何肿瘤酸性重要
结直肠癌仍是全球致死率最高的癌症之一,部分原因在于肿瘤常复发、转移或对药物失去反应。本研究探讨了这一行为背后被低估的元凶:肿瘤内部富含乳酸且呈酸性的环境。研究者揭示了这种严苛环境如何使一种保护性膜蛋白SLC26A3失稳,进而揭示了一条新的事件链,帮助癌细胞变得更具干细胞特性、更具侵袭性并对药物更耐受——为治疗提供了新的思路。
癌细胞周围的恶劣邻域
快速生长的肿瘤消耗大量糖和氧,释放乳酸和氢离子,使周围环境酸化。通过大型患者数据库和组织样本,研究者表明该酸性状态(以标记蛋白CA9跟踪)与侵袭性结直肠肿瘤密切相关。在更晚期的癌症中,CA9水平升高,而SLC26A3水平持续偏低。SLC26A3通常位于结肠细胞表面,参与盐和碳酸氢盐平衡,从而帮助控制酸碱度。在肿瘤样本、癌细胞系和单细胞分析中,团队发现随着酸性增强,SLC26A3水平下降——尤其在恶性、类干细胞样的癌细胞中明显。 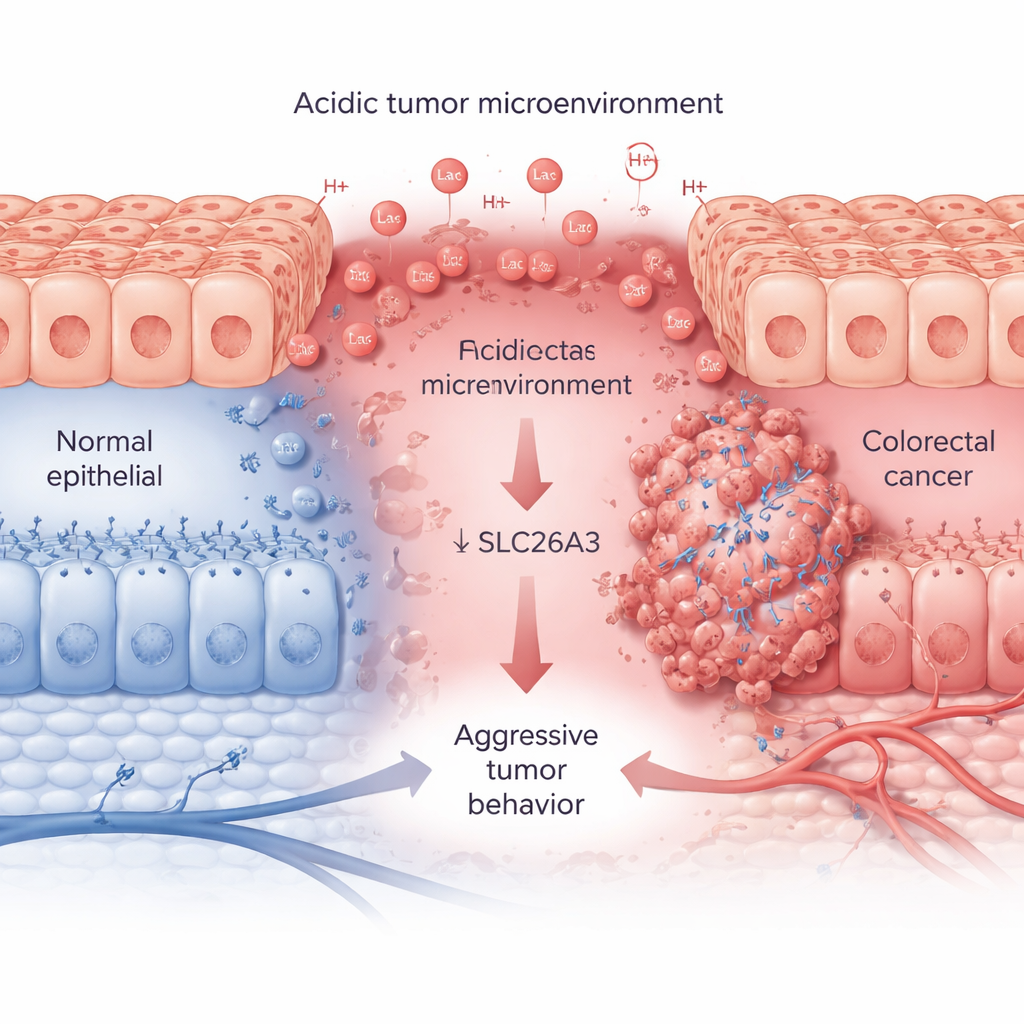
乳酸如何为“销毁”做标记
作者接着询问为何SLC26A3在酸性肿瘤中下降。他们将注意力集中在乳酰化上,这是一种由乳酸衍生、可加到蛋白上的新发现化学修饰。当结直肠癌细胞暴露于乳酸或在酸性条件下培养时,SLC26A3会被大量乳酰化。精细的蛋白质分析精确定位到一个关键位点——氨基酸K536,是该修饰加到位点。K536处的乳酰化使SLC26A3稳定性下降:该蛋白更易被泛素标记(细胞的“丢弃”信号)并送入细胞回收降解途径。抑制帮助添加乳酰化标记的酶p300可以在一定程度上保护SLC26A3免于降解。因此,酸性和乳酸建立了一个有害的反馈回路——更多乳酸导致更多乳酰化,降低SLC26A3,进一步扰乱pH平衡,促成更酸性的微环境。
关闭对癌症干性与扩散的刹车
SLC26A3减少后,癌细胞表现得更具侵袭性。在细胞培养中,结直肠癌类干细胞天然表达的SLC26A3低于非类干细胞。当研究者有意降低SLC26A3水平时,肿瘤细胞形成更多球体(干性标志)、自我更新能力更强、更能穿透人工基质并在划痕愈合实验中迁移更快。它们对常用化疗药物如奥沙利铂和5‑氟尿嘧啶的敏感性也下降。相反,提高SLC26A3可减少干性标志、减缓侵袭和迁移——但当额外加入乳酸时,这种益处会被减弱,凸显出酸性如何抵消这种保护作用。
与基因调控的隐秘联系
除了帮助调节酸碱外,SLC26A3还作为支架结合两种RNA结合蛋白HuR和CUGBP1。这些蛋白控制许多编码与癌症相关蛋白的信使RNA的寿命。当SLC26A3充足时,它能束缚部分HuR和CUGBP1,限制它们对某些癌相关转录本的稳定作用或不利影响。SLC26A3通过乳酰化并被降解后,HuR和CUGBP1更自由地结合促癌mRNA,促进干性、上皮-间质转化(EMT)、侵袭和存活。实验表明HuR有助于稳定干性标志和细胞连接蛋白的mRNA,而CUGBP1对某些靶点可与HuR相对,降低连接完整性并促进EMT——二者均有利于肿瘤扩散。
通过重建环境平衡来抗癌
为了检验这些见解是否可转化为治疗策略,研究者使用了结直肠癌小鼠模型。用碳酸氢钠中和肿瘤酸性、用MCT1抑制剂阻断乳酸转运或过表达SLC26A3均能减缓肿瘤生长。将SLC26A3恢复与化疗联合使用能进一步缩小肿瘤。在患者数据中,较高的SLC26A3水平与更佳生存、更少复发、更少转移以及更好的化疗反应相关,提示该蛋白既可作为生物标志物,也可能成为治疗靶点。 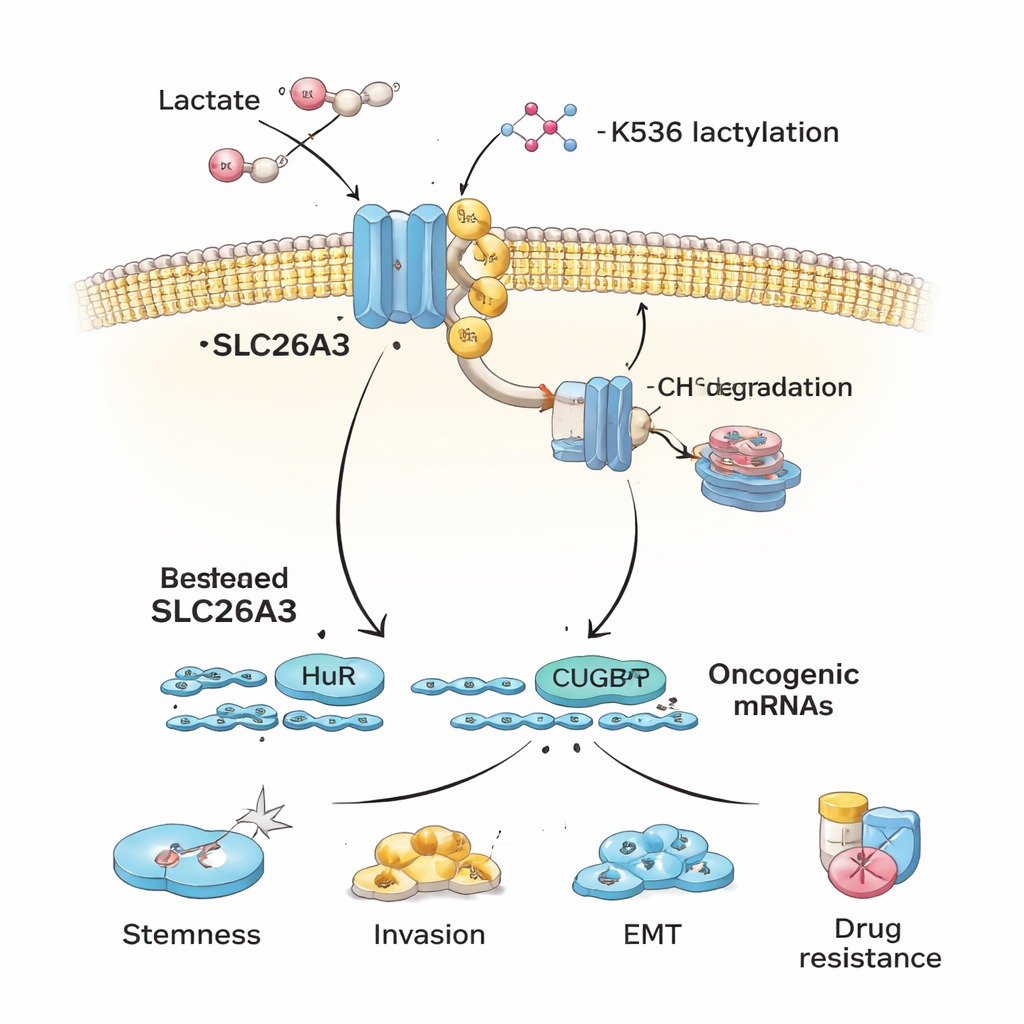
这对患者意味着什么
通俗地说,本研究表明结直肠肿瘤在一个酸性、富含乳酸的环境中茁壮成长,该环境化学性地“标记”并破坏了一个保护性守门人SLC26A3。一旦这个守门人消失,癌细胞更容易获得类干细胞特性、扩散并抵抗治疗,细胞内的强效RNA调控因子也助推了这一过程。通过缓冲肿瘤酸性、阻断乳酸处理或恢复SLC26A3,或许能削弱这一恶性反馈回路并提高常规疗法的效果。尽管这些方法仍需严格的临床验证,但它们为通过管理肿瘤化学环境来控制结直肠癌提供了一个有希望的新方向。
引用: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
关键词: 结直肠癌, 肿瘤微环境, 乳酰化, 癌症干细胞, 化疗耐药