Clear Sky Science · zh
通过抑制自噬靶向GNG4可抑制肿瘤进展并恢复前列腺癌对恩杂鲁胺的敏感性
这项研究为何重要
对于许多晚期前列腺癌患者,像恩杂鲁胺这样的强效激素抑制药最初通常有效,但随着时间推移疗效会逐步减弱。本研究揭示了肿瘤细胞使用的一种隐蔽生存策略,并指出了帮助癌细胞持续生长并抵抗治疗的特定蛋白——GNG4。理解这一机制可能促成联合疗法的开发,使现有药物的疗效更强且更持久。
一个明眼可见却被忽略的蛋白开关
前列腺癌细胞高度依赖男性激素信号,因此晚期疾病的标准治疗是切断这些信号。但多数肿瘤最终会变为“去势抵抗性”,再次开始生长。作者在同一患者的肿瘤组织与邻近正常前列腺组织中筛选出明显上调的基因。在若干候选基因中,GNG4尤为突出:当他们在前列腺癌细胞中降低其表达时,肿瘤细胞增殖显著下降。对数百例患者样本的分析证实,GNG4在原发性前列腺癌中高于正常组织,且在更具侵袭性、更高分级的肿瘤中尤为升高。
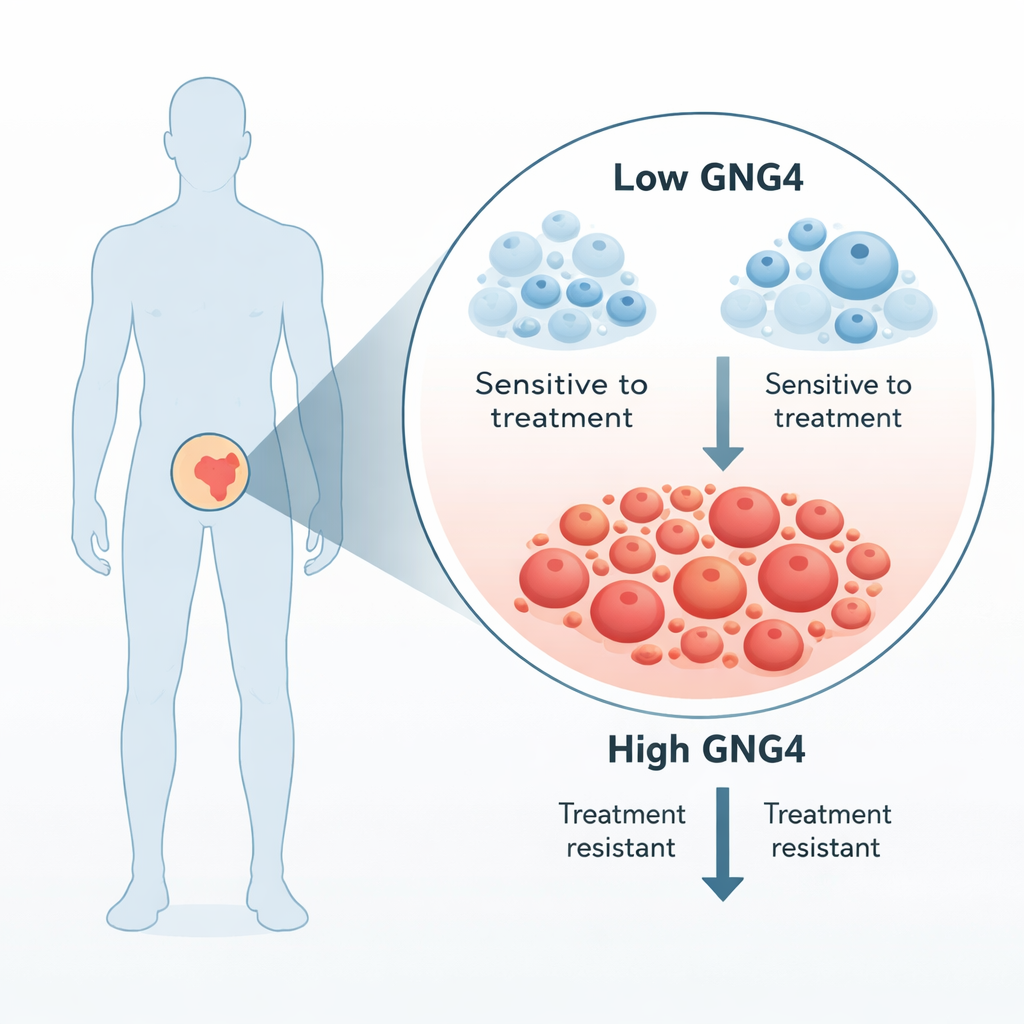
GNG4如何助力肿瘤生存
GNG4属于被称为G蛋白的更大信号家族,位于细胞膜处,将细胞外信号传递到细胞内部。研究团队证明,下调GNG4可减缓前列腺癌细胞系的分裂,使细胞在细胞周期的检查点停滞,并增加程序性细胞死亡。这些变化还降低了癌细胞在体外迁移与伤口愈合实验中的能力,且由GNG4缺陷细胞形成的肿瘤在小鼠体内生长更慢。综合来看,这些发现表明GNG4像加速踏板一样促进前列腺癌的生长与转移。
自噬:癌细胞的应急储备
研究者接着关注一个称为自噬的过程——细胞分解并回收自身组分以在饥饿或药物处理等胁迫下存活。在许多晚期癌症中,自噬作为应急储备,帮助肿瘤细胞应对恶劣环境。本研究中,GNG4高表达的前列腺癌细胞显示出更多活跃自噬的迹象,而敲低GNG4的细胞则具有较少的回收结构和较低水平的关键自噬标志物。当过表达GNG4时,细胞对恩杂鲁胺的耐受性增强,细胞死亡减少。用化学抑制剂阻断自噬能显著消除这种保护作用,说明GNG4主要通过增强这一回收系统帮助肿瘤耐受治疗。
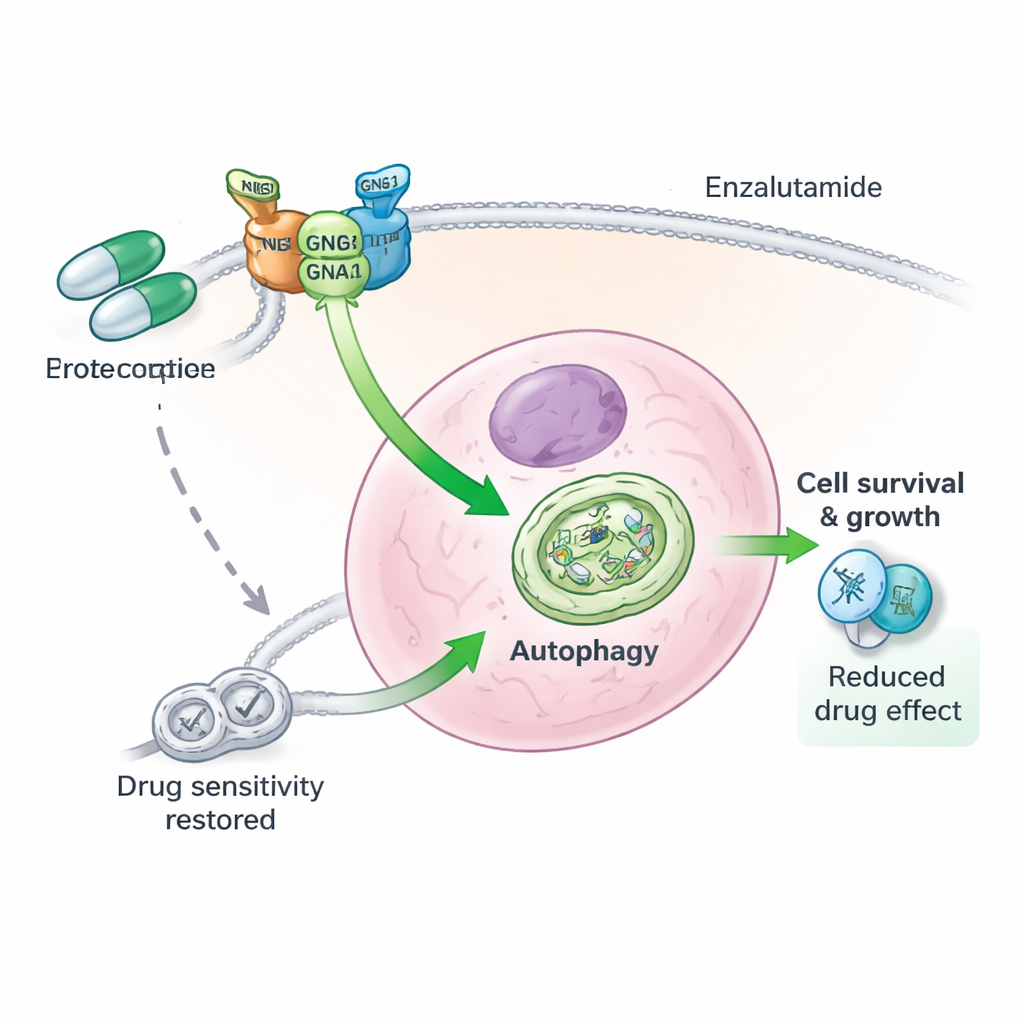
由三种蛋白组成的耐药团队
进一步研究发现,GNG4并非单打独斗。它与另一种G蛋白组分GNB1发生物理相互作用,以稳定第三种蛋白GNAI3。三者共同形成一个功能复合体,增强前列腺癌细胞内的自噬。当GNG4被减少时,GNAI3蛋白更容易被标记并通过细胞的废物清除机制降解,从而关闭自噬信号。去除GNAI3本身可以抵消额外GNG4带来的生长与存活优势,无论是在培养细胞还是小鼠肿瘤中。换言之,GNG4主要通过GNG4–GNB1–GNAI3轴推动恶性行为和胁迫耐受性。
让现有药物更有效
最后,团队探讨了在靶向GNG4的同时使用恩杂鲁胺会发生什么。在体外,敲低GNG4显著增强了癌细胞对恩杂鲁胺的敏感性,并降低了治疗后形成克隆的能力。在小鼠模型中,GNG4降低的肿瘤在接受恩杂鲁胺治疗后比GNG4正常的肿瘤萎缩得更多,且未见明显额外毒性。直接阻断自噬也产生了类似改善。这些结果表明,干预GNG4驱动的自噬可以剥夺肿瘤细胞的重要应对机制,使现有的激素阻断疗法发挥更强且更持久的作用。
对患者意味着什么
对非专业读者来说,核心信息是:某些前列腺癌通过开启一种内部回收系统来在治疗下存活,这个系统像备用发电机。研究确认GNG4是打开该系统的主要开关,并与伙伴蛋白共同保护癌细胞免受恩杂鲁胺的作用。通过关闭这一开关——无论是直接靶向GNG4还是安全地抑制自噬——未来的治疗有望减缓肿瘤生长并在那些已难以治疗的患者中恢复药物敏感性。
引用: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
关键词: 前列腺癌, 药物耐受性, 自噬, G蛋白, 恩杂鲁胺