Clear Sky Science · zh
DNA-PKcs 协调由 CTLA-4 缺失引发的癌细胞衰老
将癌细胞的“生长开关”变为“停止信号”
基于免疫的抗癌药物通常聚焦于一种称为 CTLA-4 的分子,该分子存在于免疫细胞表面,帮助机体攻击肿瘤。这项研究揭示了一个令人惊讶的转折:CTLA-4 也存在于癌细胞内部,并可能作为一种隐藏的生长助推因子。科学家有意去除黑色素瘤细胞内的 CTLA-4 后,癌细胞停止增殖并进入一种长期“退休”状态,即细胞衰老。理解这一意想不到的作用为通过靶向癌细胞内的 CTLA-4(而不仅仅是免疫细胞上的 CTLA-4)来减缓甚至缩小肿瘤开辟了新途径。
当细胞选择“退休”而不是失控增殖
细胞通常会分裂、修复,并在损伤不可修复时要么死亡、要么进入衰老——一种永久的生长停滞。衰老细胞通常体积变大、形态改变,并产生可在实验室检测到的特定标记。研究者发现,当他们在小鼠和人源黑色素瘤细胞中下调 CTLA-4 时,细胞体积变大、增殖显著下降,经典的衰老信号上升,包括可通过特殊染色检测到的酶活性以及像 p16 和 p21 这样的细胞周期阻断蛋白。这些变化无论是在短期沉默 CTLA-4 还是通过基因编辑永久敲除 CTLA-4 时都能观察到。
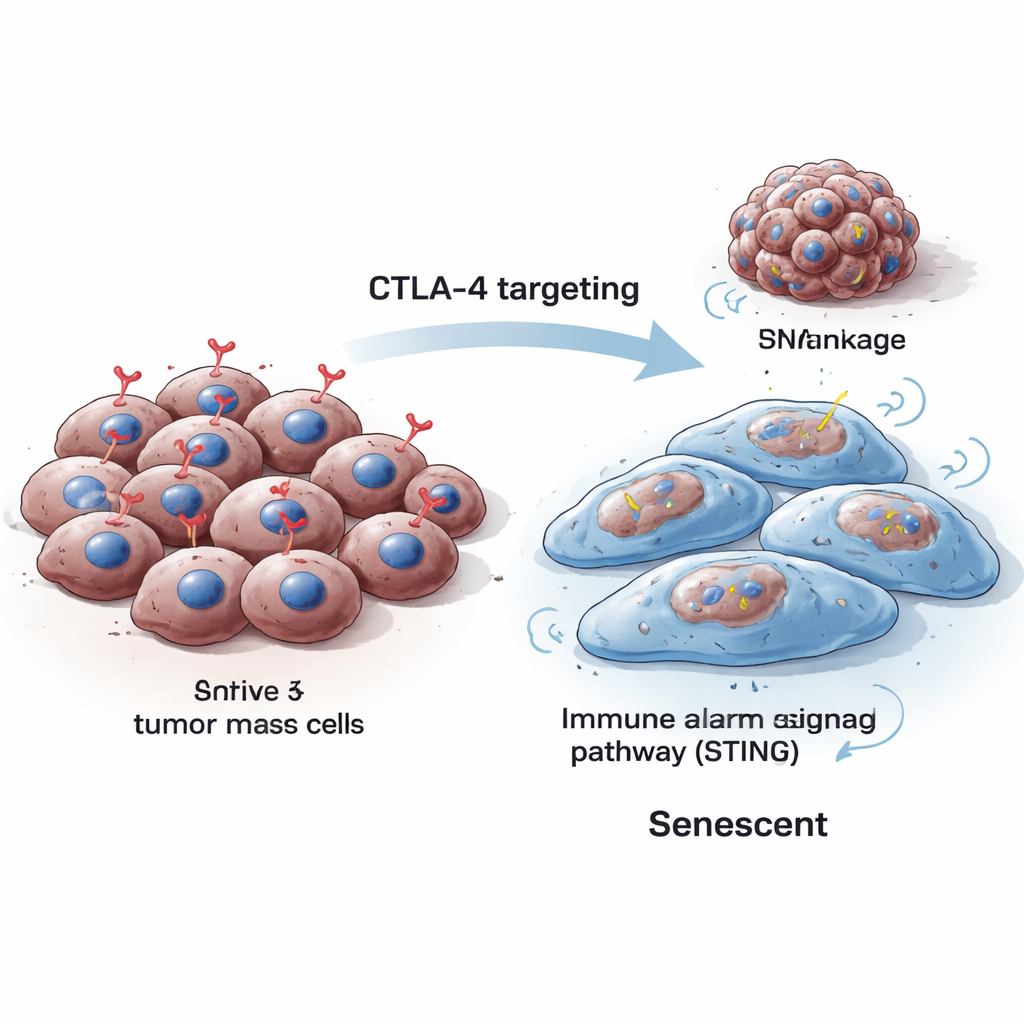
基因蓝图的裂痕导致停滞
为了解为何 CTLA-4 丧失会促使癌细胞进入衰老,团队考察了这些细胞在分裂时如何处理其 DNA。他们发现 CTLA-4 缺失降低了 Aurora B 的水平——一种帮助染色体在细胞分裂时正确分离的蛋白。当 Aurora B 水平下降时,细胞出现基因组不稳定:形成含有 DNA 的微核,并且 DNA 损伤标志物增加。这类 DNA 应激已知会将细胞推向衰老而非无限增殖。重要的是,恢复 Aurora B 可减少这些微核,表明 CTLA-4 的丢失与染色体处理错误和 DNA 损伤直接相关。
DNA 损伤触发内在警报网络
CTLA-4 缺失细胞中断裂和错位的 DNA 没有被忽视。它激活了 DNA 损伤感应器 DNA-PKcs,进而触发 STING 通路——一种响应细胞内游离 DNA 的内在警报系统。STING 被激活后,向下游分子(包括 TBK1 和 IRF3)传递信号,并同时增强另一路关乎生长控制的 AKT 通路。与促进生长相反,这些联合信号最终提高了 p21 的水平——一个强有力的细胞周期刹车,巩固了衰老状态。当科学家阻断 DNA-PKcs 时,STING 的激活和衰老特征显著减少,表明 DNA-PKcs 位于这条警报传导的核心。
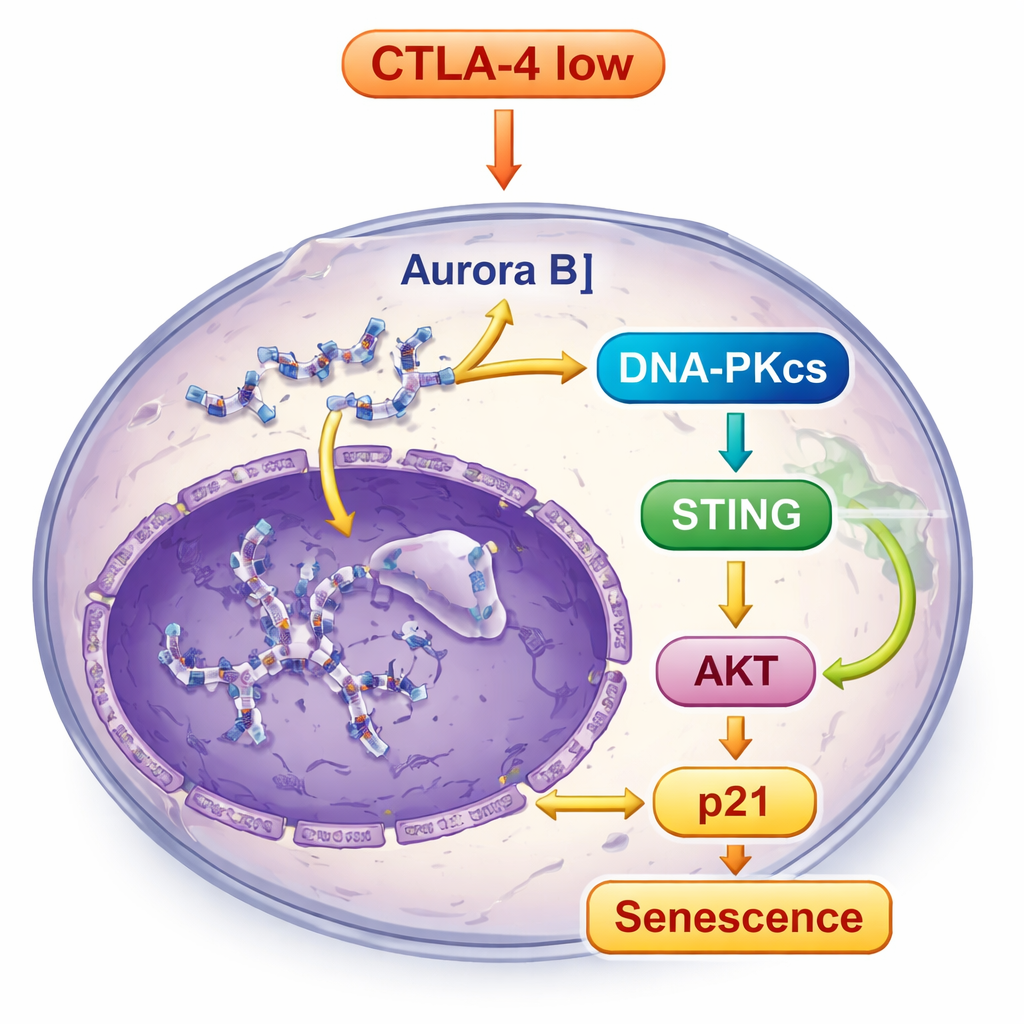
从细胞培养到活体肿瘤
培养皿中的结果只能说明部分情况,因此研究者测试了 CTLA-4 丧失是否会影响小鼠体内的真实肿瘤。他们将有或无 CTLA-4 的黑色素瘤细胞分别植入同一只动物的两侧。缺失 CTLA-4 的肿瘤生长更慢、重量更轻、体积更小。那些 CTLA-4 缺陷肿瘤还显示出更强的衰老染色、更高的 DNA 损伤和更明显的 STING 通路激活。来自大型公开数据库的患者癌症数据分析进一步支持该关联:在多种癌症类型中,CTLA-4 的表达往往与 DNA-PKcs 及其他 DNA 修复成分呈负相关,呼应了实验室在人体疾病中的发现。
这对未来癌症治疗意味着什么
总体而言,该研究表明癌细胞内的 CTLA-4 有助于维持基因稳定性并持续分裂。当 CTLA-4 被去除,染色体变得不稳定、DNA 断裂累积,以 DNA-PKcs 和 STING 为中心的内在警报通路将细胞驱入永久性生长停滞。对普通读者而言,这意味着在肿瘤细胞中关闭 CTLA-4 会将癌症从危险的快速生长状态引导到更安全的“退休”状态。这些见解表明,未来的癌症疗法不仅可以通过阻断免疫细胞上的 CTLA-4 来释放免疫系统,也可以通过直接解除肿瘤细胞内的 CTLA-4 来利用衰老作为抑制癌症生长的内建刹车。
引用: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
关键词: 细胞衰老, 黑色素瘤, CTLA-4, DNA 损伤, STING 通路