Clear Sky Science · zh
TET2 在细胞质与细胞核之间穿梭:结直肠癌进展中的内在刹车
癌细胞如何携带自身的刹车
结直肠癌是全球最常见的癌症之一,当肿瘤细胞学会侵入邻近组织并转移到其他器官时,往往会变得致命。这项研究揭示,许多癌细胞实际上携带一种内在的“刹车系统”——一种名为 TET2 的蛋白,当它进入细胞核时可以减缓肿瘤的扩展。了解这一内置刹车如何被开启或关闭,可能为抑制肿瘤生长开辟新途径,而不仅仅是试图直接杀死癌细胞。
观察肿瘤细胞内关键蛋白的移动
研究者将注意力集中在 TET2 上,这是一种通过去除 DNA 上的某些化学标记来控制基因开关状态的蛋白。在数百例结直肠癌患者的组织样本中,他们追踪了 TET2 在肿瘤细胞内的位置。发现了四种主要模式:主要位于细胞核、主要位于细胞质,或明显偏向某一侧。肿瘤中 TET2 在细胞核中更多的患者生存期倾向于更长,而将 TET2 保持在细胞质的患者预后较差。随着癌症发展到更晚的临床分期,细胞核内的 TET2 变得更少,提示失去这种核内保护是肿瘤变得更具侵袭性的一个环节。
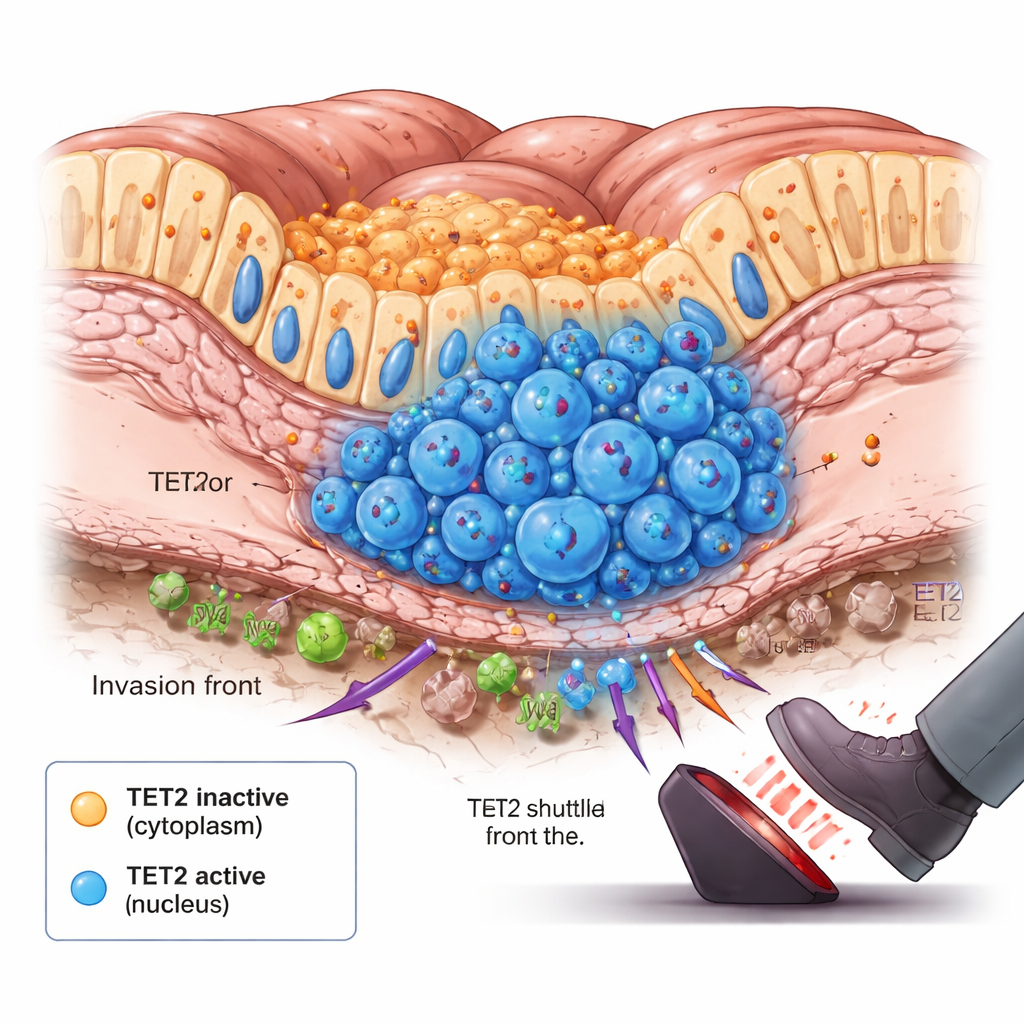
肿瘤前线与变化的瞬间
深入分析时,团队注意到一个令人意外的现象:在刚开始扩散的肿瘤中,细胞核内 TET2 略有增加。这些细胞聚集在肠道上皮的底部——即癌细胞首次向深层组织推进的侵袭前沿。动物实验和模拟肿瘤生长的长期细胞培养模型也显示了类似的时间动态。早期,TET2 多留在细胞质并大体处于非活性状态。随着肿瘤体积增大、内层区域出现缺氧与营养匮乏的情况,细胞内信号促使 TET2 在特定细胞亚群中穿梭进入细胞核。一旦进入核内,TET2 开始去除 DNA 甲基化标记并减缓肿瘤生长,像是在癌症越过危险阈值时触发的应急刹车。
当“前进”信号也触发刹车
结直肠肿瘤常依赖两个强大的“前进”程序:一种叫上皮–间质转化(EMT)的形态转换过程,帮助细胞变得更具移动性和侵袭性;以及促进生长和存活的 WNT 信号通路。这些通路通常被视为癌症中的纯粹有害因素。然而,本研究显示,当 EMT 和 WNT 强烈激活时,它们也会促使 TET2 进入细胞核。在细胞培养中使用药物和遗传学工具,科学家们证明激活 EMT 或 WNT 会增加进入核内的 TET2 细胞数量,而阻断这些通路则产生相反效果。一旦到达细胞核,活性 TET2 随即下调与 EMT 和 WNT 相关的基因,减少细胞迁移并放慢增殖。换言之,既促使肿瘤生长的信号同时也唤醒了一股内在的反作用力。
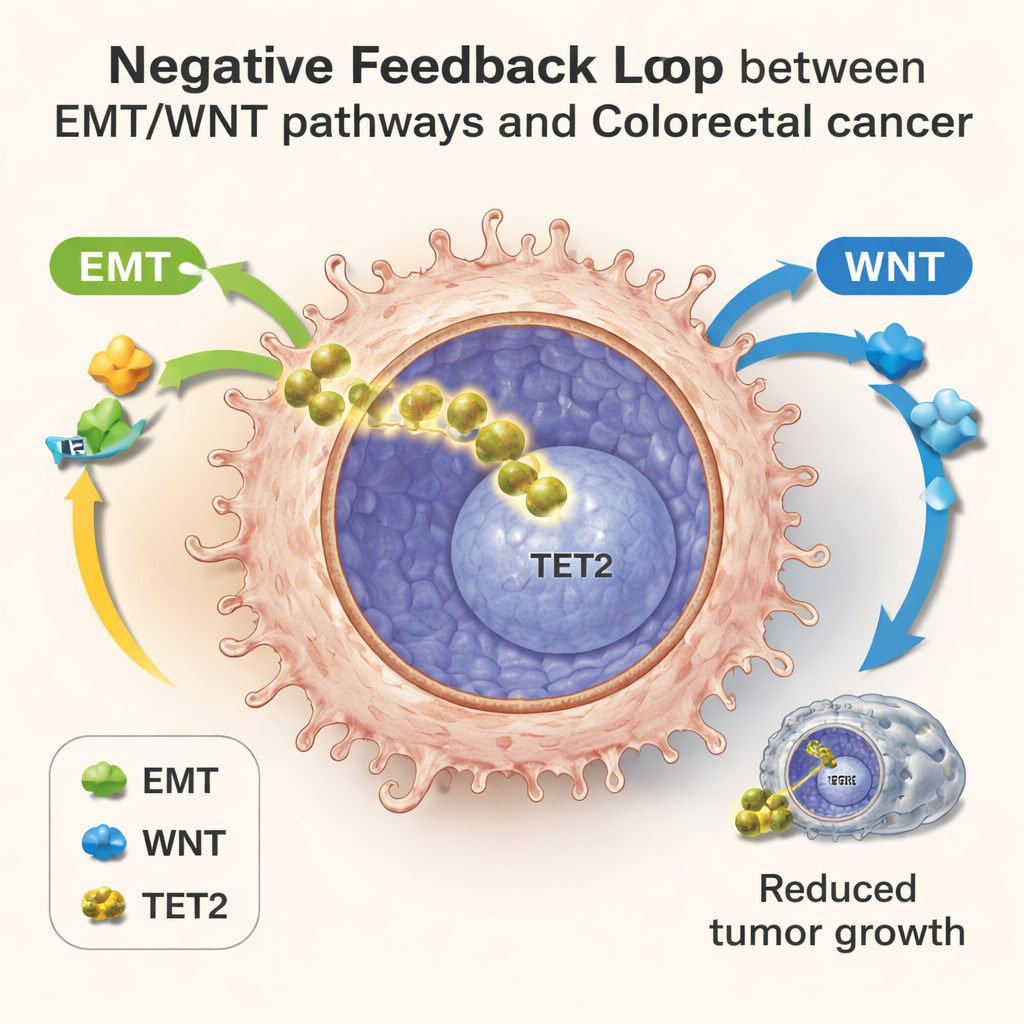
单细胞揭示隐藏的负反馈回路
为了详细绘制这场拉锯战,团队使用了单细胞 RNA 测序技术,可以同时读取数千个单细胞中哪些基因处于活跃状态。在体外培养的菌落、小鼠肿瘤以及结直肠癌患者样本中,他们观察到细胞沿着一个进展时间线分布。早期细胞显示正常的能量利用和较弱的 EMT/WNT 活性;晚期细胞则表现出代谢重编程、强烈的 EMT/WNT 信号,随后出现上升的 TET2 目标基因。在这些后期阶段,TET2 活性较高的细胞侵袭相关基因表达较低,并且即便在已经开始转移的肿瘤中也与更好的患者结局相关。这一模式支持负反馈回路的观点:代谢压力以及 EMT/WNT 的激活将 TET2 推入细胞核,而核内 TET2 反过来抑制这些侵袭性方案。
这对未来癌症治疗意味着什么
对于非专业读者,关键的信息是结直肠癌进展并非一个简单的“开/关”切换,而是存在一个内置的、延迟起效的安全机制:随着肿瘤细胞变得更具侵袭性,它们也会在核内激活 TET2,从而在一定程度上收抑自身。随着时间推移,许多肿瘤通过失去核内 TET2 或压倒其作用来逃避这一控制。若能找到保持 TET2 位于细胞核或增强其活性的方式——可能与调节 EMT 或 WNT 的药物联合使用——临床医生或可加强这一自然刹车,减缓癌症扩散。未来的治疗或许不再仅仅从外部攻击癌细胞,而是通过恢复并放大这种内在调控系统来发挥作用。
引用: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
关键词: 结直肠癌, TET2, 表观遗传学, EMT WNT 信号, 癌症进展