Clear Sky Science · zh
发育转录因子PAX6异常维持通过JNK3信号通路促进神经元细胞死亡
这项研究为何与视力相关
青光眼是导致永久性失明的主要原因之一,主要因为将视觉信息从眼睛传至大脑的神经细胞会慢慢死亡。尽管许多治疗方法可以降低眼压,但即便在眼压得到良好控制的情况下,人们仍可能失明。本研究探讨了一个更深层的问题:在压力之下,是什么促使这些视网膜神经细胞作出死亡的决定?我们能否在细胞核内的基因调控层面关闭这一决定?
受压的视网膜正遭受攻击
青光眼及相关眼病的核心是视网膜神经节细胞(RGCs)的缓慢丧失,这些是眼睛的输出神经元。RGCs对多种压力极为敏感,包括神经递质谷氨酸的毒性水平,它会过度激活NMDA受体并引发有害的钙超载。研究人员使用了一种成熟的小鼠模型:向眼内注射少量NMDA,有选择性地伤害RGCs,同时大体保持其他视网膜层完整。他们确认该处理并未改变眼压,但确实在RGCs中引发了程序性细胞死亡的典型迹象,例如线粒体释放细胞色素c和出现TUNEL阳性的细胞核。
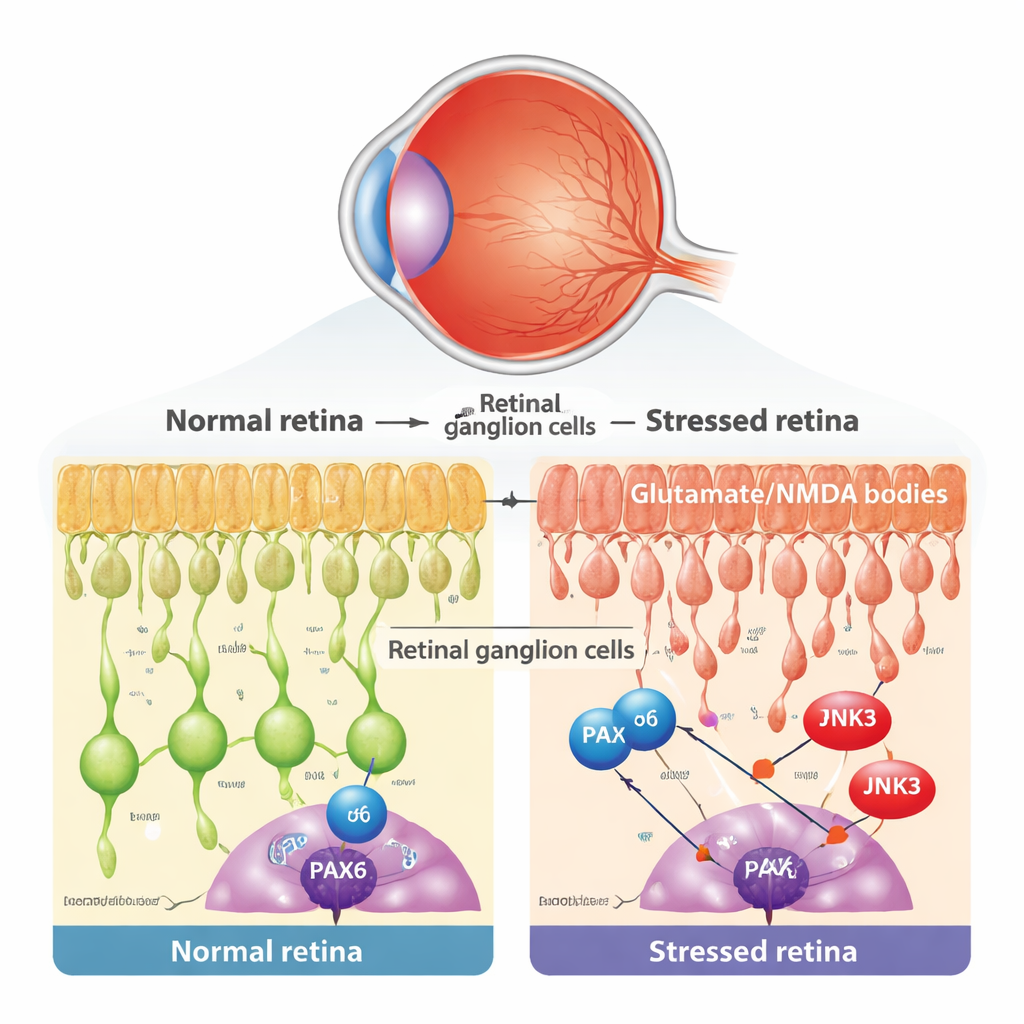
一个不愿退场的发育基因
在早期发育阶段,一个名为PAX6的基因调控因子是眼睛的主要“建筑师”,指导不同视网膜细胞的生成和连线。传统观点认为此类发育程序在成年后大多关闭。通过重新分析来自小鼠和人类视网膜的单细胞RNA测序数据,研究团队发现PAX6在成熟的RGCs和某些中间神经元中实际上被强烈且选择性地维持。通过显微免疫染色,他们显示在RGCs所在的层中,PAX6主要存在于节细胞而非相邻的无长突细胞(amacrine cells)。这提出了一个有趣的可能性:在成人疾病中,原本的发育程序可能被挪用并转变为驱动退化的因素。
从守护者到执行者:PAX6角色转换
为测试PAX6在压力下是帮助RGCs生存还是导致其死亡,研究者采用了类似基因治疗的方法。他们在视网膜中递送携带特异性小RNA的病毒载体以敲低PAX6,然后用NMDA处理眼睛。与对照处理眼相比,PAX6缺失的视网膜显示出明显更少的凋亡RGCs和更少的线粒体损伤,表明在该模型中PAX6对完全的细胞死亡是必需的。全基因组RNA测序显示,许多促凋亡基因,尤其是涉及线粒体损伤和半胱天冬酶激活的基因,在正常小鼠中被NMDA强烈诱导,但在PAX6被沉默时被显著抑制。换言之,PAX6有助于开启一组推动RGCs濒临死亡的基因网络。
翻转PAX6开关的应激激酶
压力如何在不增加PAX6数量的情况下激活它?团队将注意力集中在主要存在于神经元中的应激响应酶JNK3上。在NMDA损伤下,JNK3迁移到RGCs的细胞核并与PAX6发生物理相互作用。使用纯化蛋白的体外生化实验表明,JNK3可以直接在PAX6上加入磷酸基团,这一反应可被JNK抑制剂阻断。在缺失Jnk3基因的小鼠中,NMDA不再产生相同的PAX6磷酸化模式。染色质定位(ChIP-seq)和针对性DNA结合实验显示,在应激下,磷酸化的PAX6与JNK3一道,在关键促凋亡基因如Bax和Gadd45a的控制区结合更强,增强了它们的活性。当PAX6被敲低或JNK3被遗传性移除时,这种结合以及相应的促死基因激活都显著降低。
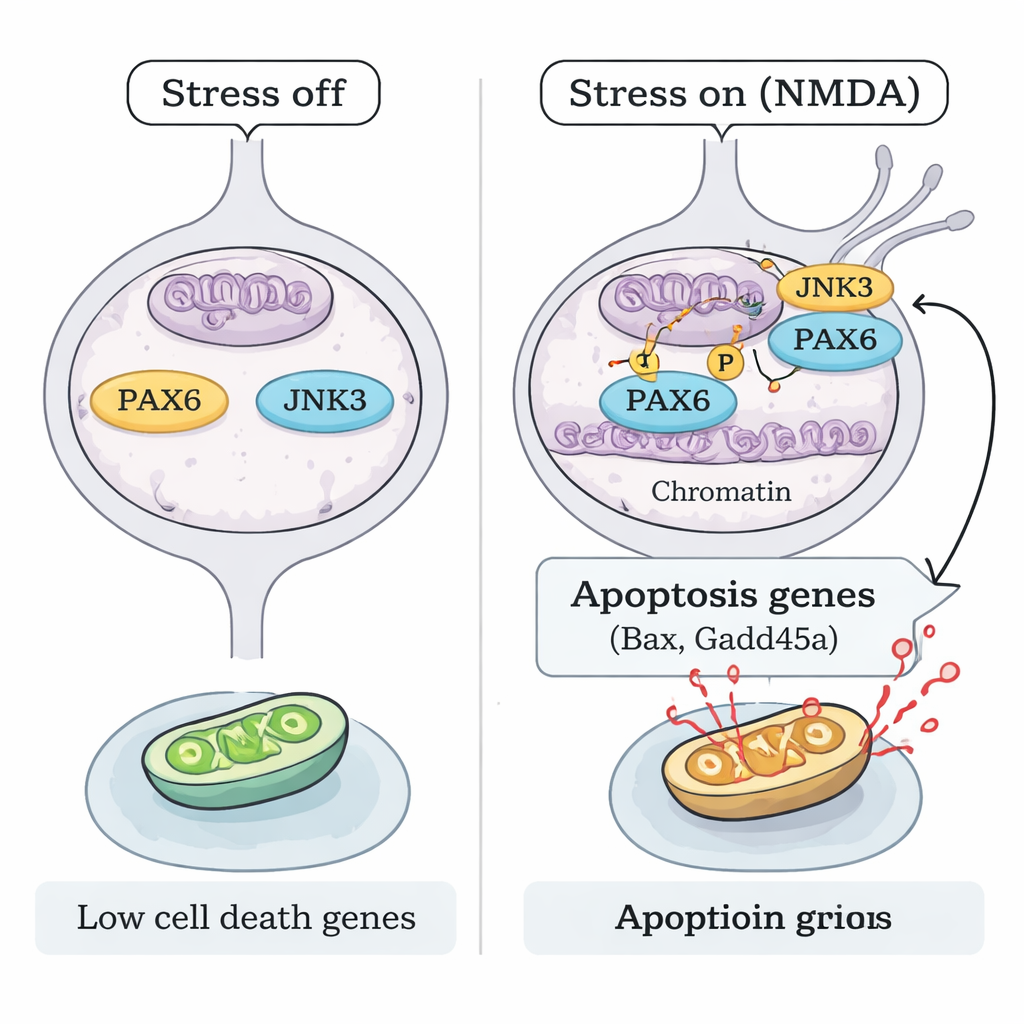
关闭死亡程序以保护视力
最后,研究者询问阻断该JNK3–PAX6轴是否足以保护对视力至关重要的细胞。在PAX6敲低的小鼠和缺失JNK3的小鼠中,RGCs在NMDA暴露后都显著得以保存,死亡细胞更少,视网膜结构更健康。这指向一个清晰的机制模型:在兴奋性毒性应激下,JNK3磷酸化持续表达的PAX6,将其从发育期的构建者转变为成年RGCs中强有力的细胞死亡基因程序激活者。中断这条链——通过沉默PAX6或使JNK3失活——可以使许多这些神经元存活。对患者而言,这项工作表明未来的青光眼治疗可能超越降低眼压,直接针对决定视网膜神经元生死的基因开关。
引用: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
关键词: 青光眼, 视网膜神经节细胞, PAX6, JNK3, 神经退行性变