Clear Sky Science · zh
靶向ENO1使巨噬细胞极化重编程以激发抗肿瘤免疫并改善放疗疗效
将肿瘤的护盾变为靶点
癌症不仅通过快速生长存活,还通过悄然削弱机体防御而得以延续。本研究探讨了一种存在于癌细胞上的隐匿分子ENO1,ENO1助力肿瘤逃避免疫监视并抵抗放射治疗。通过开发一种针对ENO1的新型抗体药物,研究者展示了可以清除肿瘤的保护性化学物质、唤醒免疫细胞,并在结直肠癌和三阴性乳腺癌模型中增强放疗效果。 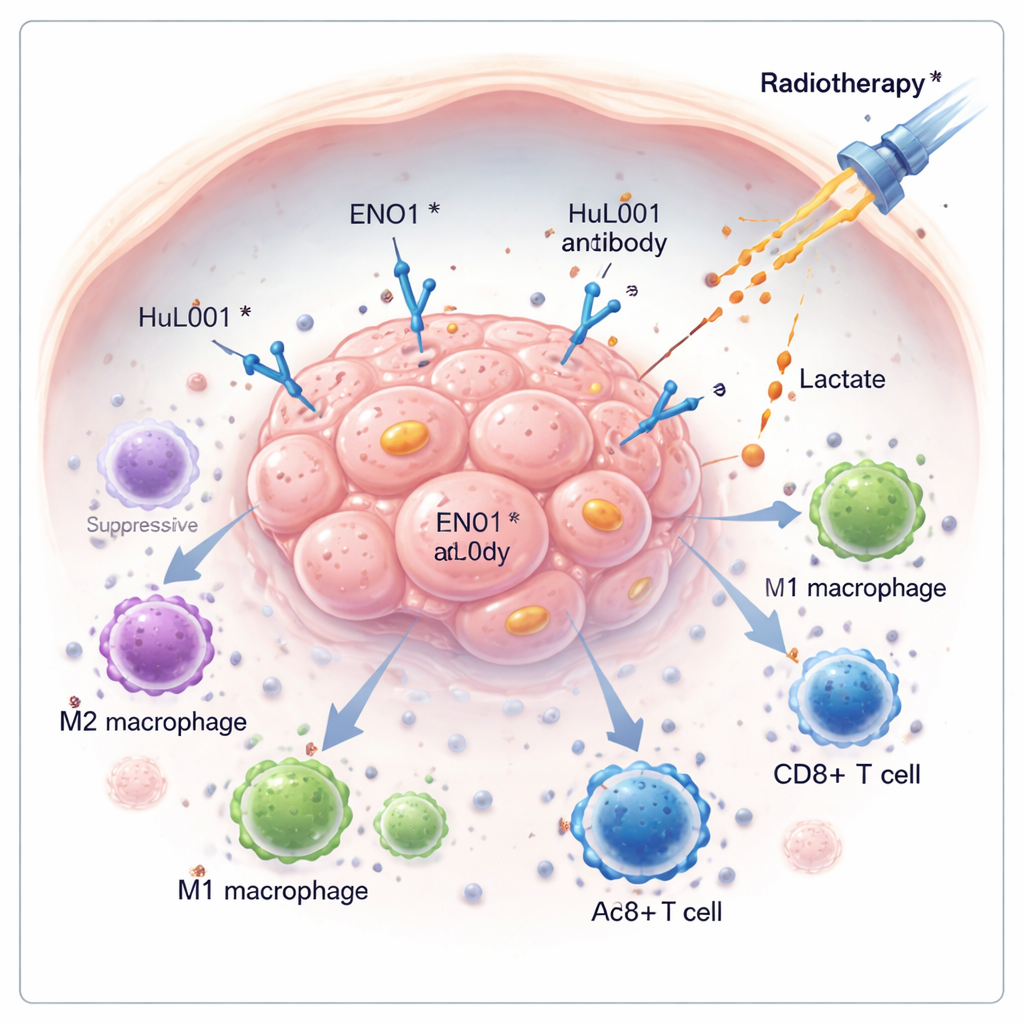
使免疫沉默的代谢伎俩
许多肿瘤重编程其能量利用途径,在有氧情况下仍大量分解糖产生乳酸。这些乳酸被从癌细胞外泵出并在肿瘤周围积累,使周围环境变得酸性且恶劣,从而削弱免疫攻击。在这项工作中,作者聚焦ENO1——一种参与糖酵解的酶,也可出现在癌细胞表面。当位于细胞表面时,ENO1与另一种称为MCT4的运输蛋白协同,帮助外排乳酸——助长有利于肿瘤生长并抑制免疫细胞的环境。
放疗如何可能适得其反
放射治疗旨在破坏肿瘤DNA并触发免疫反应,但它也会在肿瘤微环境中产生副作用。研究团队发现,放疗增强的一种分子信号TGFβ1会激活一种酶(PRMT5),该酶对ENO1进行化学修饰并将其搬运到癌细胞表面。ENO1到达表面后会与MCT4发生物理相互作用以稳定MCT4并促进乳酸外排。在晚期结直肠癌和三阴性乳腺癌患者中发现更高的表面ENO1水平,并与更多转移和更差的生存相关,这提示放疗可能无意中强化了由乳酸驱动的、抑制免疫的肿瘤屏障。
对“友军”和“敌军”免疫细胞的重编程
在肿瘤周围的酸性光晕中,被称为巨噬细胞的免疫细胞会被推动进入一种“修复者”状态(通常称为M2),这种状态实际上通过抑制炎症和促进修复来帮助肿瘤,而不是消灭癌细胞。研究者制备了一种人源化抗体HuL001,可识别小鼠和人类癌细胞表面的ENO1。在细胞培养和小鼠模型中,HuL001破坏了ENO1对MCT4的支持,减少了乳酸释放,并使巨噬细胞从促肿瘤的M2状态转向更具攻击性的M1状态,M1更善于吞噬和杀灭肿瘤细胞。重要的是,HuL001并没有简单地杀死巨噬细胞;相反,它对巨噬细胞进行了重新教育,同时直接增加了癌细胞凋亡。
让放疗更有效
在结直肠癌和三阴性乳腺癌的小鼠模型中,将HuL001与放疗联合使用能使肿瘤更明显缩小、复发更慢,且在许多动物中肿瘤完全消失。 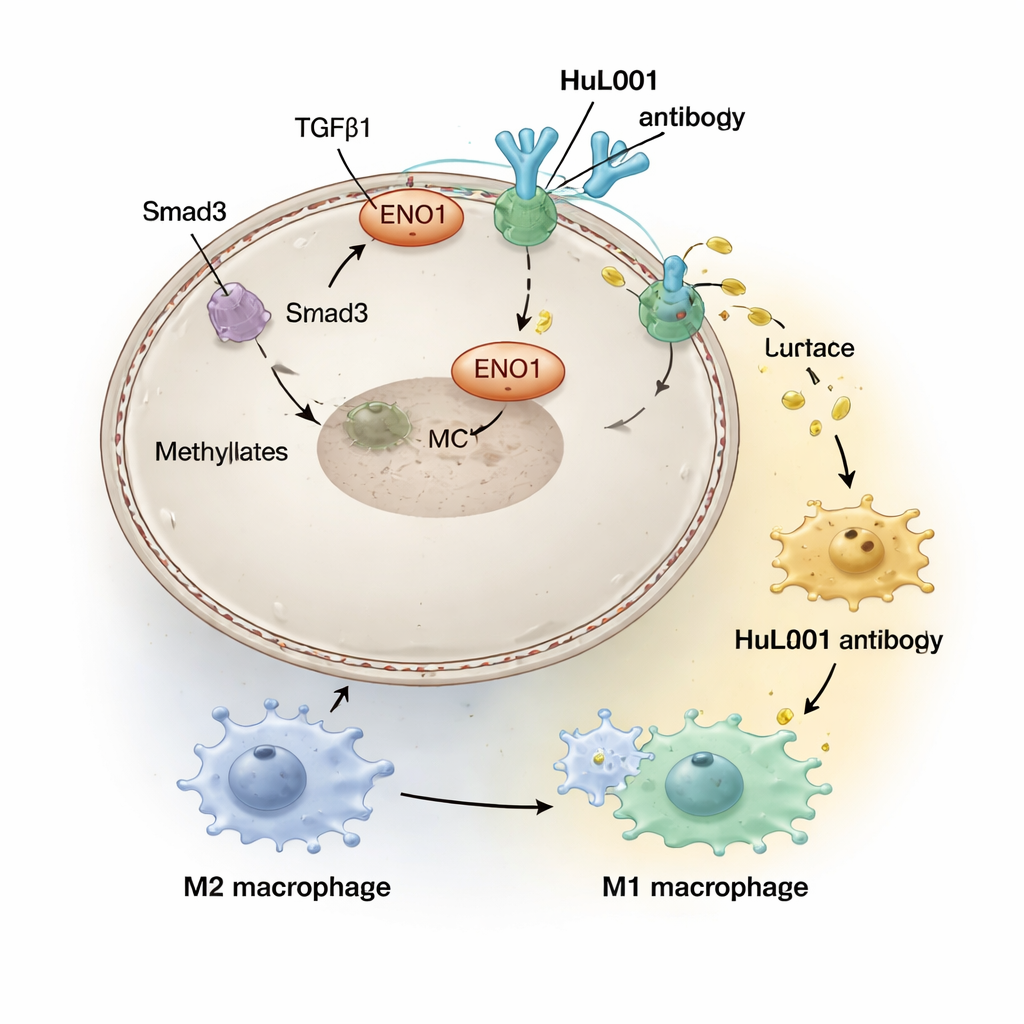
从复杂通路到可行希望
对非专业读者而言,这项研究传达的信息是:肿瘤的化学特性及其免疫细胞的邻里关系紧密相连。ENO1处于交汇点:它帮助肿瘤燃烧糖、外排乳酸并招募错误类型的免疫支持。通过用靶向抗体阻断表面ENO1,研究者能够减少有害乳酸的积累,将巨噬细胞从肿瘤帮手转为肿瘤战士,并在难治性癌症模型中使放疗更为有效。尽管HuL001尚未成为临床用药,这项工作表明,针对像ENO1这样的代谢“守门员”可能成为将肿瘤自身防御转化为弱点并增强现有疗法(如放疗)的有力策略。
引用: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
关键词: 肿瘤代谢, 巨噬细胞极化, 放疗, 免疫治疗, 乳酸