Clear Sky Science · zh
Sec8:抗RNA病毒防御中RIG-I的新型正向调节因子
我们的细胞如何识别狡猾的病毒
许多危险病毒,包括流感病毒和新出现的动物病毒,其遗传物质以RNA形式存在。我们的细胞依靠内部警报系统迅速发现这些入侵者并启动抗病毒反应。本文研究了一种鲜为人知的细胞蛋白Sec8,表明它在维持我们关键病毒传感器RIG‑I的存活和活性方面发挥了重要作用,确保RIG‑I有足够时间保护机体。
受威胁的细胞警报器
RIG‑I是一个分子“入侵警报器”,在细胞内部巡逻以寻找病毒RNA的片段。当它发现可疑RNA时,会构象改变并被激活,发送信号最终触发I型干扰素——这些强效的警示分子帮助邻近细胞抵御感染并激活免疫防御。由于过度活跃的警报可能引发有害的炎症或自身免疫病,细胞对RIG‑I的水平进行严格控制。若干其他蛋白可通过连接小的泛素链来标记RIG‑I,从而将其送往称为蛋白酶体的细胞“碎纸机”降解。直到现在,尚不清楚在活跃的RNA病毒感染期间,哪些额外的细胞因子能够保护RIG‑I避免被过早降解。
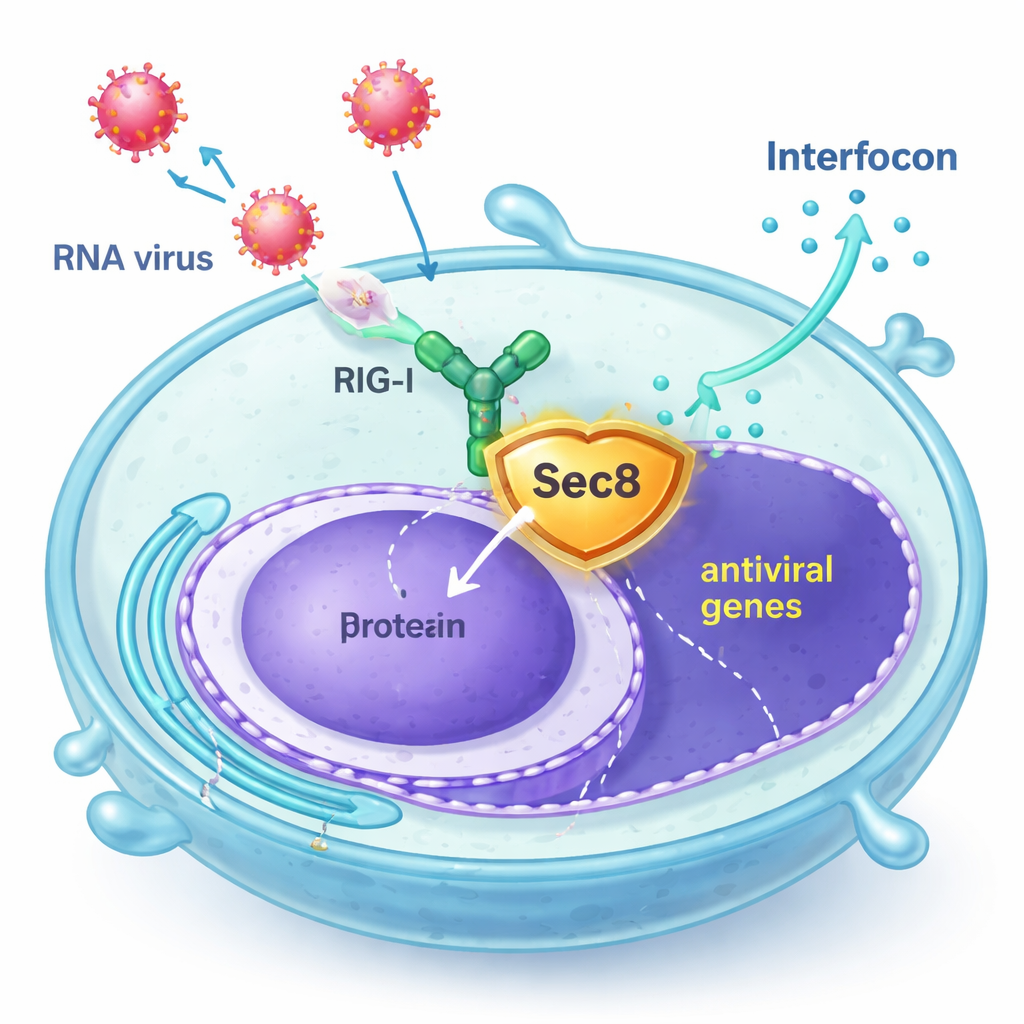
Sec8作为贴身保镖出场
作者发现,Sec8(最为人所知的是作为一个由八个蛋白组成的复合体的一部分,帮助分泌囊泡与细胞表面融合)实际上能增强抗病毒信号。在人细胞系和小鼠原代免疫细胞中,增加Sec8水平会在感染囊泡性口炎病毒(VSV)、仙台病毒或暴露于合成病毒RNA后,导致干扰素相关基因更强的激活。相反,降低Sec8会减少干扰素及干扰素刺激基因的产生,使细胞对病毒复制的抵抗能力下降。这些发现表明,Sec8不仅参与分泌过程,还作为抗病毒警报通路内的正向调节因子发挥作用。
阻挡细胞碎纸机
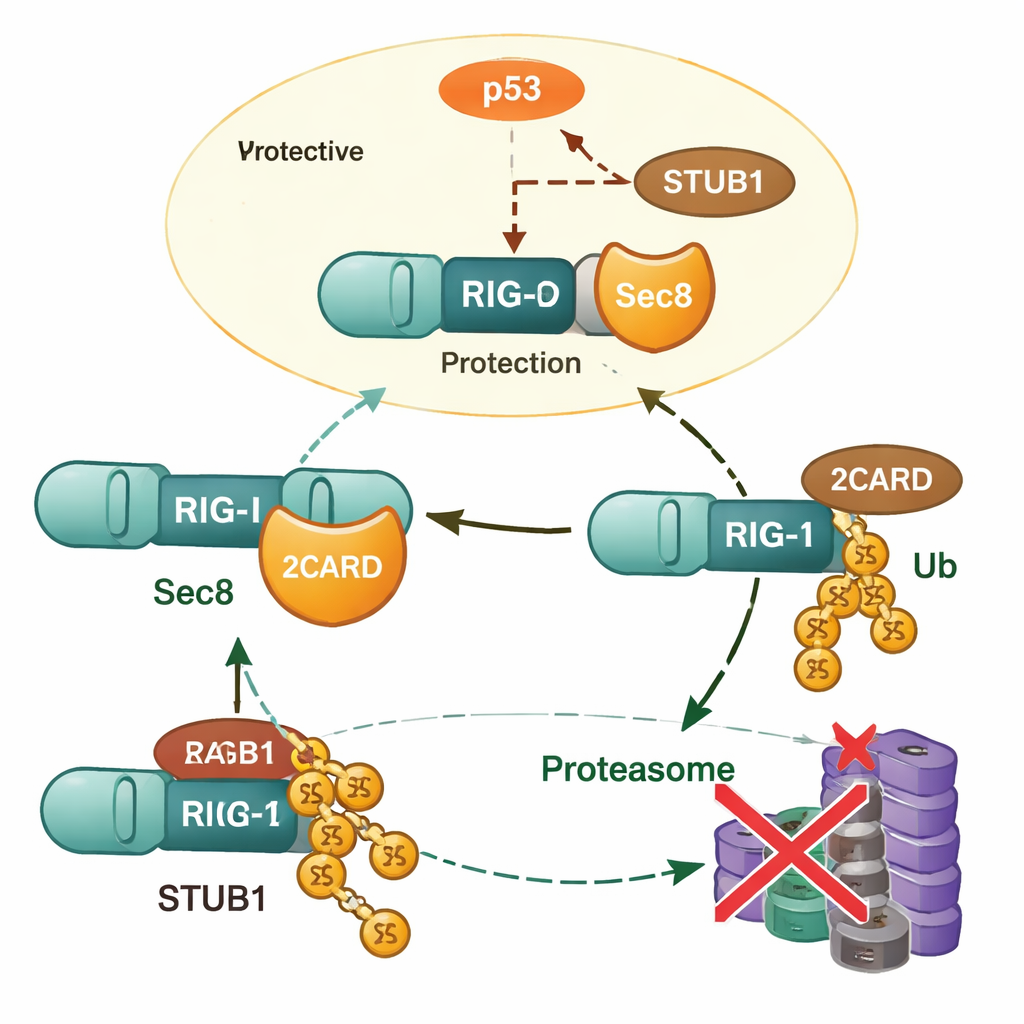
进一步研究表明,Sec8并不提升RIG‑I的基因表达;相反,它防止RIG‑I蛋白被降解。当去除Sec8时,RIG‑I水平下降更快,而使用抑制蛋白酶体的药物可以阻止这种丢失,暗示涉及细胞的蛋白回收机械。研究团队识别出另一种蛋白STUB1作为关键的“标记者”,它在RIG‑I的第190位赖氨酸处连接一种特定类型的泛素链(K48连结),将RIG‑I标记为待降解。Sec8通过两种方式干扰这一过程:一是物理上与STUB1竞争结合RIG‑I相同的激活区域,二是降低细胞产生STUB1的量。
Sec8、p53与对标记者的控制
为了解Sec8如何减少STUB1的产生,作者转向基因调控研究。他们定位出一段作为STUB1基因启动子核心的短DNA序列,并表明著名的肿瘤抑制蛋白p53能结合该区域并提升STUB1水平。Sec8降低了p53的量及其激活性磷酸化,从而使p53无法有效驱动STUB1的产生。当阻断p53或沉默STUB1时,丧失Sec8对干扰素产生和病毒增殖的不利影响在很大程度上被逆转。这将Sec8置于一条从p53到STUB1再到RIG‑I稳定性的调控链的顶部。
从培养皿到活体动物
研究团队随后在基因工程小鼠中测试了Sec8的重要性,这些小鼠在特定免疫细胞中缺失Sec8基因。感染VSV后,这些动物产生的干扰素更少,脾、肝、肺等器官的病毒负荷更高,且表现出更严重的肺损伤、体重下降更大和生存率更低,均优于对照小鼠。这些体内结果证实了Sec8在整个生物体对RNA病毒感染的防护中并非配角,而是重要的保护因子。
为何这对未来疗法重要
简而言之,本研究表明Sec8像RIG‑I的贴身保镖。通过抑制“标记者”蛋白STUB1并直接保护RIG‑I免于被送往细胞碎纸机,Sec8使细胞能够及时产生干扰素响应,更好地控制RNA病毒。理解这一新描述的p53–STUB1–RIG‑I轴为未来抗病毒策略打开了通路,可能通过稳定RIG‑I或模拟Sec8的保护作用,增强我们对广泛RNA病毒感染的防御能力。
引用: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
关键词: 固有免疫, RNA病毒, RIG-I, 泛素化, 干扰素信号传导