Clear Sky Science · zh
来自缺氧肿瘤细胞的乳酸传递通过DNMT1-NHE7轴促进巨噬细胞衰老与M2极化,加速子宫内膜癌进展
为什么剥夺肿瘤氧气很重要
子宫内膜癌起源于子宫内膜,在全球范围内变得越来越常见。许多晚期肿瘤难以治愈,因为它们容易复发、转移或对常规治疗产生耐药性。本研究探讨了快速生长的癌症常见特征——缺氧——在肿瘤内部引发的变化,并展示了一个看似简单的代谢废物乳酸如何重新编程周围的免疫细胞,使其有利于肿瘤而非攻击肿瘤。
低氧把肿瘤变成乳酸工厂
随着子宫内膜癌细胞增殖,血供无法跟上,产生低氧或缺氧区域。细胞通过激活名为HIF1A的主调控因子来应对,这一因子重塑了细胞的能量代谢。细胞不再主要依靠高效的能量产生途径,而是增强糖酵解——一种快速但低效的过程,会产生大量乳酸。研究人员分析了数百名患者的肿瘤数据,发现HIF1A水平升高与许多糖酵解相关基因和将乳酸泵出癌细胞的转运蛋白活性增加密切相关。肿瘤中HIF1A更多的患者预后通常更差,提示这种代谢转变与更具侵袭性的疾病紧密相连。
肿瘤废物如何重塑“有益”免疫细胞
巨噬细胞是可以攻击或支持肿瘤的免疫细胞,其作用取决于所处状态。本研究显示,在缺氧条件下,子宫内膜癌细胞向周围释放更多乳酸。这些乳酸由肿瘤细胞表面的MCT3转运出细胞,再通过巨噬细胞上的另一种转运蛋白MCT1被摄入。一旦进入细胞,乳酸会将巨噬细胞从防御性状态推向所谓的M2状态,该状态与组织修复、抑制炎症以及不幸的是支持肿瘤生长有关。在体外实验中,暴露于高乳酸肿瘤细胞上清的巨噬细胞表现出更多M2型标志物,而这些巨噬细胞分泌的因子又促进了癌细胞的生长、迁移和侵袭。 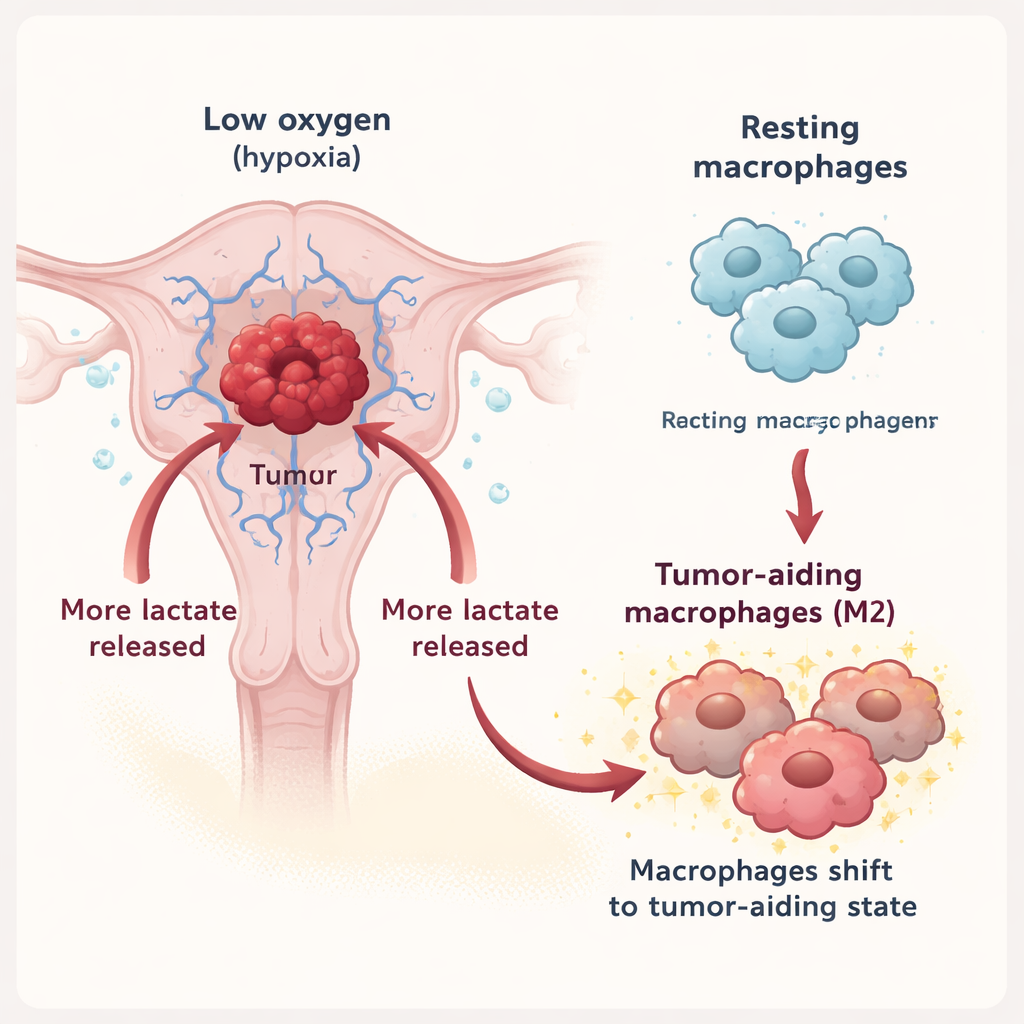
使细胞“pH阀门”沉默的表观遗传开关
研究更进一步揭示了连接肿瘤来源乳酸与巨噬细胞有害行为的分子开关。乳酸不仅在细胞中游离存在;它还可以修饰细胞核内的组蛋白——一种称为乳酰化的化学标记——从而影响基因的开启或沉默。研究人员发现,乳酸在DNMT1基因的调控区增加了特定的组蛋白修饰,提升了该基因的活性。DNMT1是一种能在DNA上添加甲基并沉默基因的酶。这里的一个靶基因是NHE7,它帮助控制细胞某些隔室内的酸碱度。DNMT1上调会增加NHE7基因的甲基化,导致其表达下降。NHE7减少扰乱了细胞内部的pH平衡并激活名为MAPK的信号通路。该通路反过来促使巨噬细胞朝向有利肿瘤的M2状态和一种称为衰老(senescence)的老化表型,使它们陷入慢性、促肿瘤的工作模式。
从分子连锁反应到肿瘤更快生长
为检验这一连锁事件在生物体内是否重要,科学家构建了在小鼠体内共同移植人类子宫内膜癌细胞与类人巨噬细胞的模型。当额外供应乳酸时,肿瘤增大,分裂细胞增多,并含有更多呈M2型、处于衰老状态且DNMT1高表达、NHE7低表达的巨噬细胞。令人印象深刻的是,当对巨噬细胞进行NHE7过表达改造时,这削弱了乳酸的促肿瘤作用:肿瘤更小,凋亡细胞更多,且M2型和衰老巨噬细胞减少。抑制DNMT1酶或阻断MAPK通路也削弱了乳酸重编程巨噬细胞的能力,进一步支持这些分子组成了一个相互关联的轴线的观点。 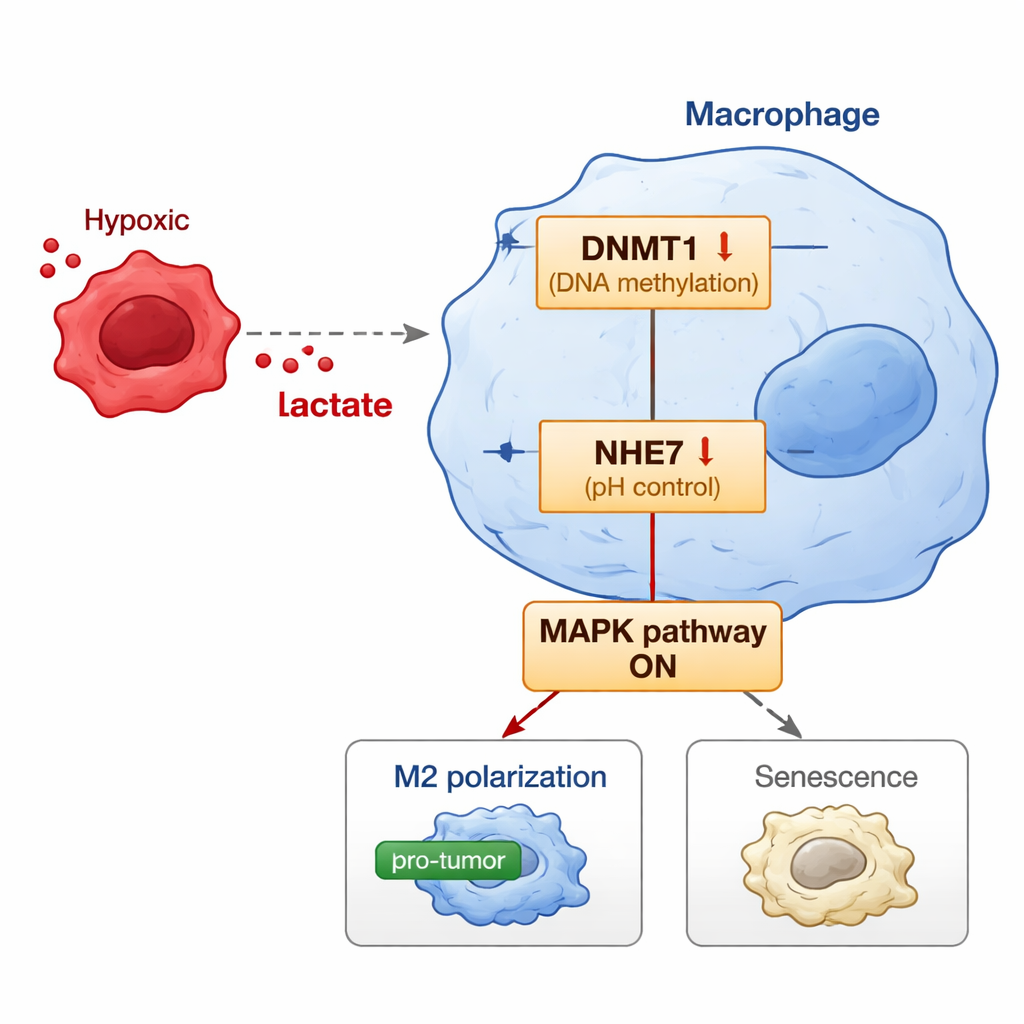
将肿瘤自有伎俩转化为治疗靶点
对非专业读者而言,核心信息是:子宫内膜肿瘤可以利用低氧和乳酸——曾被视为单纯的细胞代谢废物——来“洗脑”邻近免疫细胞,使其帮助而非阻止癌症。它们通过一条表观遗传传递链实现:乳酸提升DNMT1,DNMT1沉默NHE7,继而激活信号通路将巨噬细胞固定为肿瘤友好且衰老的状态。通过干预乳酸–DNMT1–NHE7–MAPK链中的任一步,可能有望恢复更有效的抗肿瘤免疫反应并减缓癌症生长。这项工作指向未来的治疗策略,不仅直接靶向癌细胞,还重新教育被肿瘤劫持的周围免疫细胞。
引用: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
关键词: 子宫内膜癌, 肿瘤微环境, 乳酸代谢, 巨噬细胞极化, 表观遗传调控