Clear Sky Science · zh
超越代谢:探索乳酸与乳酰化在癌症调控性细胞死亡中的调控与治疗意义
为什么来自糖的“废物产物”对癌症很重要
数十年来,乳酸——使过度劳累的肌肉感到灼热的物质——被视为细胞的垃圾。本文综述表明,在癌症中乳酸绝非废物。它既是燃料,又是化学信号,甚至可以作为开关决定肿瘤细胞的生死。理解这一隐藏作用可能为在保护健康组织的同时诱导癌细胞自毁开辟新途径。
重编程癌细胞的糖类捷径
癌细胞以“嗜糖”著称。即便在氧气充足时,它们也倾向于将葡萄糖快速分解为乳酸,而非在线粒体中完全氧化,这种转变称为瓦尔堡效应。这一策略使肿瘤能够高速产生能量和构建块。随之而来的乳酸大量被特殊转运蛋白泵出,形成酸性、富含营养的肿瘤微环境,支持生长并帮助肿瘤适应低氧或化疗等应激。
乳酸作为不同细胞死亡类型的调节钮
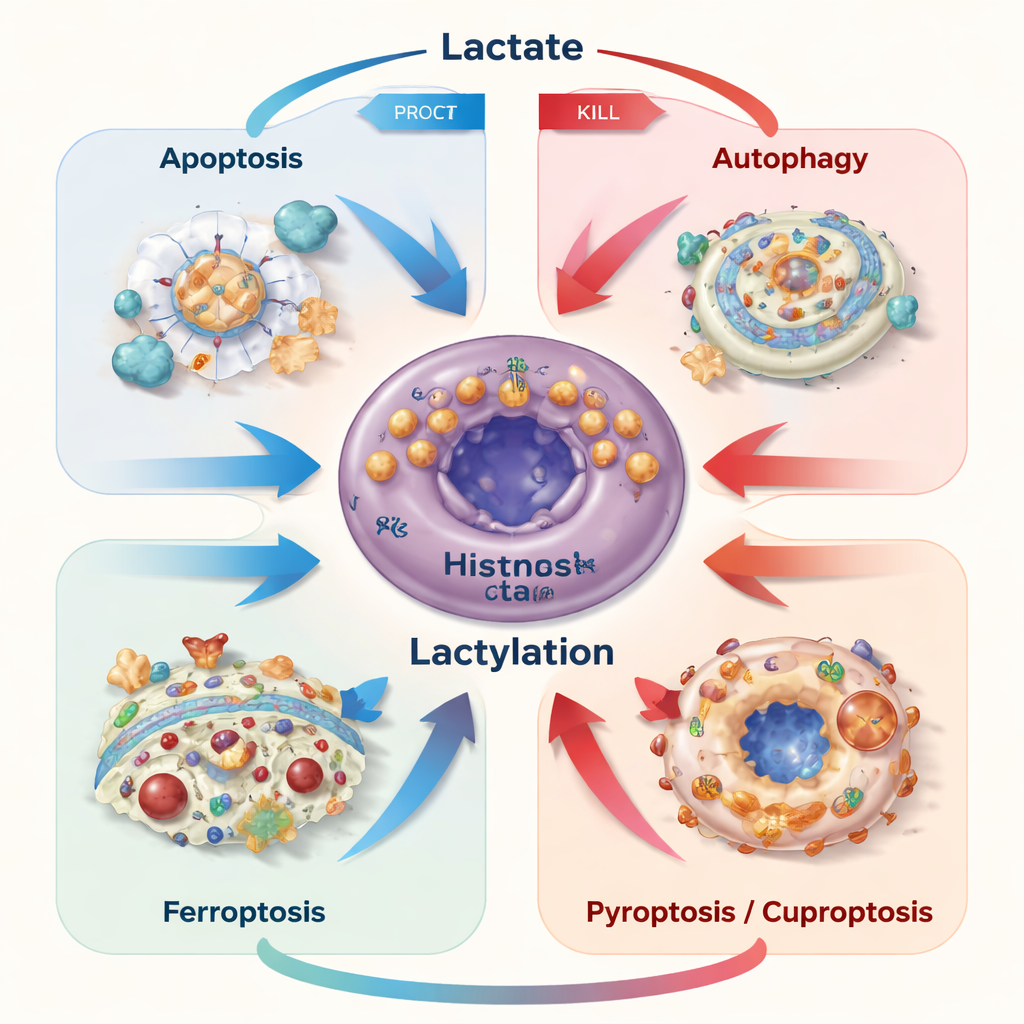
我们体内的细胞死亡通常受严格控制,有助于清除受损或有害细胞。癌细胞常常逃避这些程序。作者描述了乳酸如何既抑制又触发多种调控性死亡途径——细胞凋亡(细胞“自杀”)、自噬(自我消化)、铁死亡(铁介导的膜损伤)、焦亡(炎性爆裂)和铜死亡(铜介导的衰败)。当癌细胞生成或摄取适量乳酸时,常将其用作燃料和生存信号,启动保护通路以抵抗化疗、营养缺乏或靶向药物。但当乳酸在细胞内积累,例如其外排受阻时,随之而来的酸性应激和线粒体损伤可触发开关,将细胞推向凋亡或铁死亡等路径。
乳酰化:乳酸在蛋白上的书写
一项令人瞩目的新发现是乳酸可以被转化为小的化学标签并附着于蛋白的赖氨酸残基上,这种修饰称为乳酰化。酶作为这些标签的“写入者”和“擦除者”,既修饰与DNA相关的组蛋白,也作用于许多其他蛋白。这些标记改变基因的开启状态、酶的行为以及关键调控因子的稳定性。在癌症中,乳酰化微调生存与自毁之间的平衡。例如它可以上调阻止凋亡的蛋白、增强通过自噬的回收、通过收紧铁稳态并提升抗氧化能力来保护细胞免受铁死亡,或通过改变细胞处理铜敏感蛋白的方式影响诸如铜死亡之类的新型死亡形式。
代谢与死亡程序之间的双向对话
这种关系并非单向:细胞死亡通路也会重塑肿瘤如何利用糖并产生乳酸。当线粒体在早期凋亡或选择性去除线粒体(线粒体自噬)过程中受损时,细胞常退回到快速糖酵解,增加乳酸产出。周围的支持细胞,如癌相关成纤维细胞,也可能经历类似重编程,成为为附近肿瘤细胞供能的乳酸工厂。其他类型的死亡,如铁死亡,则倾向于抑制糖酵解,从而降低乳酸水平。其结果是一个动态的反馈回路,代谢与死亡机制在肿瘤演化和对治疗反应时不断相互调整。
把弱点变成治疗策略
由于乳酸和乳酰化可根据情境对癌细胞起保护或杀伤作用,作者主张治疗不能仅仅阻断乳酸生成。未来的治疗可能需要选择性地重定向乳酸流、调整其转运蛋白或靶向特定乳酰化标记,以将癌细胞推向死亡边缘,同时重新激活被酸性环境抑制的抗肿瘤免疫细胞。响应局部乳酸或pH水平的智能给药系统和纳米药物正在成为实现这种精确性的途径。简单来说,文章的观点是曾被视为代谢垃圾的物质实际上是控制癌细胞命运的强大旋钮——学会正确地转动该旋钮可以显著提升现有疗法的效果。
引用: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
关键词: 乳酸, 乳酰化, 癌细胞死亡, 肿瘤代谢, 铁死亡