Clear Sky Science · zh
散发性与林奇综合征相关微卫星不稳定结直肠癌的肿瘤免疫组织构成与免疫逃逸
这对癌症患者为何重要
免疫治疗已显著改变许多结直肠癌患者的预后,但并非所有人都能从中受益。本研究提出了一个关键问题:为什么有些理论上对免疫系统高度可见的肿瘤,仍能躲过免疫监视?通过比较两类基因不稳定的结肠癌——与遗传性林奇综合征相关的和散发性发生的——研究人员发现了肿瘤周围免疫细胞如何包围、攻击或在某些情况下保护肿瘤的重要差异。
通向同一类肿瘤的两条路径
微卫星不稳定(MSI)结直肠癌携带大量DNA错误,这些错误产生异常蛋白,可作为免疫系统的“标记”。此类肿瘤可因遗传性DNA修复缺陷(林奇综合征)而发生,也可因仅在肿瘤中出现的改变(散发性MSI癌)而形成。尽管两种肿瘤在显微镜下外观相似,但它们的免疫环境——以及可能的治疗反应——并不相同。研究团队收集了来自芬兰患者的43例MSI结直肠癌样本,包括林奇相关和散发性病例,并通过组织染色、全基因组测序和RNA测序对其进行分析,以详细描绘存在哪些免疫细胞以及肿瘤如何避免被清除。
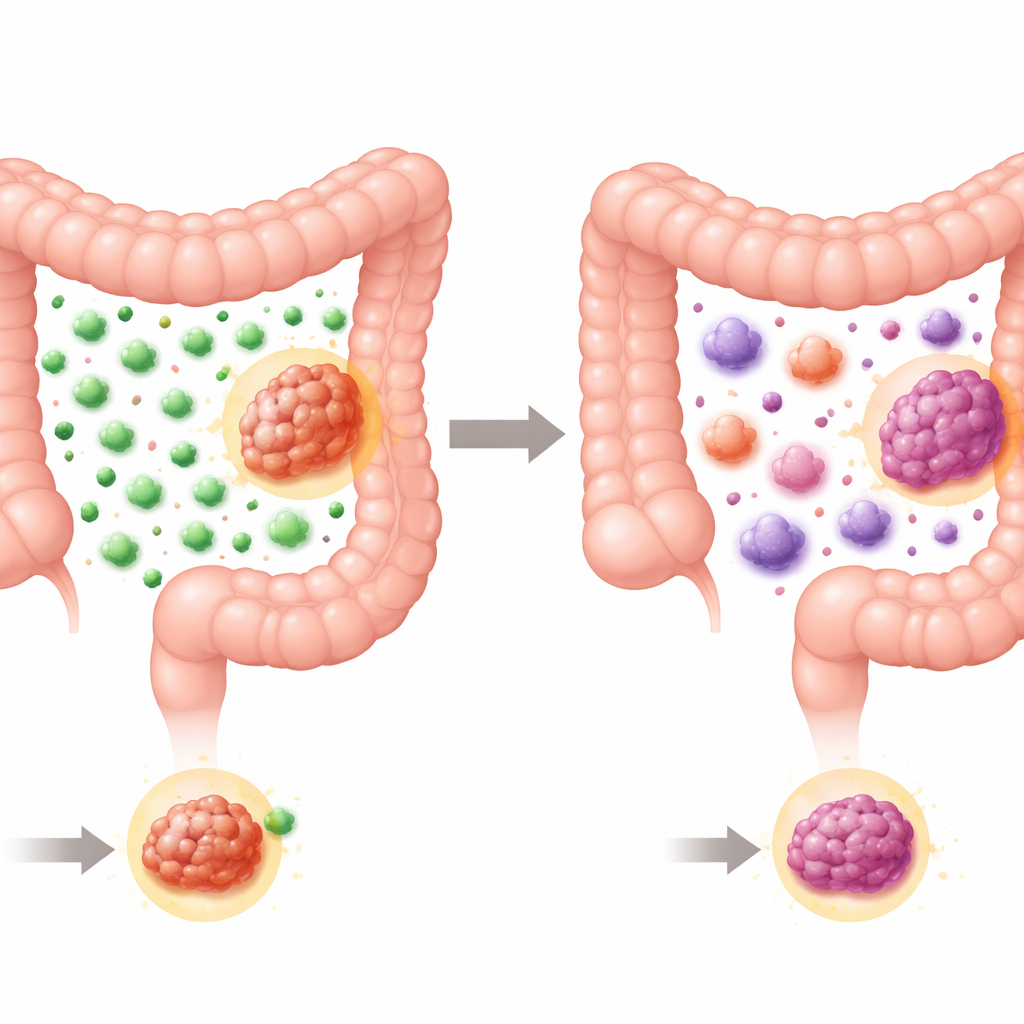
有多少免疫细胞到场
研究者首先关注T细胞——免疫系统的定向“打手”。他们测量了一项既定的免疫细胞评分,该评分结合了肿瘤中心与侵袭边缘处总T细胞和杀伤性T细胞的密度。如预期,整体而言MSI肿瘤的评分高于更典型的结直肠癌,反映出它们更能吸引T细胞。但在MSI组内,出现了明显差异:所有林奇综合征相关的肿瘤均为高免疫细胞评分,而散发性MSI肿瘤则大致一分为二,高低并存。换言之,遗传性MSI癌几乎总是吸引到强烈的T细胞浸润,而散发性MSI癌更为多样化,有些对免疫系统看起来相对“冷淡”。
有利与不利的辅助细胞
接着,研究转向髓系细胞——包括巨噬细胞和中性粒细胞等先天免疫细胞,它们既可帮助T细胞抗癌,也可能矛盾地保护肿瘤。通过多重染色同时标记多种蛋白,作者将巨噬细胞分为两类广义类型:M1样细胞,支持炎症与肿瘤杀伤;以及M2样细胞,倾向于抑制性、促愈合并常常促进肿瘤生长。林奇和散发性MSI肿瘤都含有大量髓系细胞,但散发性肿瘤在侵袭边缘的支持性组织中表现出更多的M2样巨噬细胞。在该区域,散发性肿瘤的M2样细胞数量甚至超过M1样细胞。在散发性组内,那些具有高T细胞评分的肿瘤也显示出更多的M1样巨噬细胞,而M2样水平普遍保持较高——这提示M1与M2巨噬细胞之间的平衡可能影响T细胞能否发起有效攻击。
遗传伎俩与肿瘤异质性
为了解为何某些MSI肿瘤能逃避免疫系统,研究者检查了影响肿瘤抗原呈递以及调节免疫反应“刹车”的基因改变。林奇和散发性MSI癌都经常带有影响抗原呈递关键成分的突变,但两组之间仅有细微差别。更为显著的是免疫“检查点”信号的差异。散发性肿瘤表达更高水平的PD-L2和CD40L,这些分子能影响免疫细胞行为,且日益作为与现有检查点抑制剂联合的潜在药物靶点被研究。团队还测量了每个肿瘤潜在新抗原的数量以及肿瘤在遗传上是均一还是混合(克隆性 vs 异质性)。令人意外的是,预测的新抗原负荷更高并不等同于更多的T细胞浸润。相反,遗传多样性更高的肿瘤——尤其是散发性MSI癌——往往携带更多新抗原,但也显示出诸如中性粒细胞减少等模式,暗示免疫系统并未充分利用这些靶点。
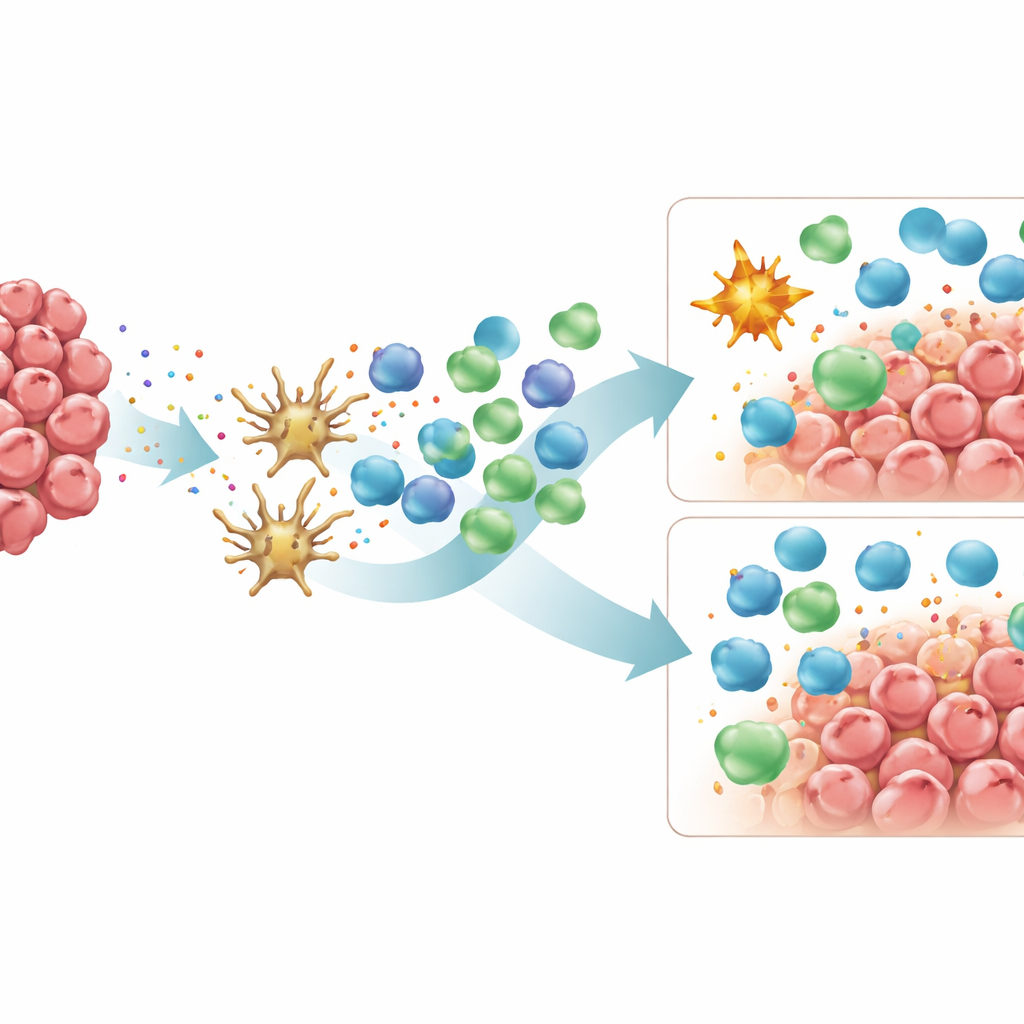
这对未来治疗意味着什么
总体而言,研究将林奇相关的MSI结直肠癌描绘为持续“热性”的肿瘤,富含T细胞,而散发性MSI癌则呈现更混合的格局,部分肿瘤浸润显著,另一些则被免疫抑制性巨噬细胞和更高表达的某些检查点分子所缓冲。与此同时,散发性肿瘤更常表现出高遗传多样性和分布在不同肿瘤细胞亚克隆中的大量新抗原,这一模式以往研究表明可能削弱T细胞反应的有效性。对患者而言,这些发现有助于解释为什么并非所有MSI结直肠癌即便具有高突变率也对免疫治疗反应相同。研究还指向了新的策略,例如重新编程或清除M2样巨噬细胞的药物,或针对PD-L2和CD40L等额外检查点的疗法,这些在散发性MSI肿瘤中可能尤为相关。通过更好地将治疗方案与每个肿瘤独特的免疫景观相匹配,临床医生或能提升并个体化结直肠癌的免疫治疗效果。
引用: Martin, S., Elomaa, H., Väyrynen, J.P. et al. Tumour immune contexture and immune evasion in sporadic and Lynch syndrome-associated microsatellite unstable colorectal cancers. Br J Cancer 134, 1019–1030 (2026). https://doi.org/10.1038/s41416-025-03302-z
关键词: 微卫星不稳定性结直肠癌, 林奇综合征, 肿瘤免疫微环境, 肿瘤相关巨噬细胞, 癌症免疫治疗