Clear Sky Science · zh
破骨细胞中离子通道和转运蛋白的谱系与功能
为什么我们的骨骼需要微小的门卫
我们的骨骼看起来坚固且不变,但实际上它不断被拆除并重建。被称为破骨细胞的专门细胞充当拆除队,溶解旧骨以便新骨形成。本文综述了一个隐秘的微观“门卫”阵容——离子通道和转运蛋白,它们允许带电原子和营养物质进出破骨细胞。通过理解这些微小通道如何控制骨质分解,科学家希望设计出更好的骨质疏松和其他骨病治疗方法。
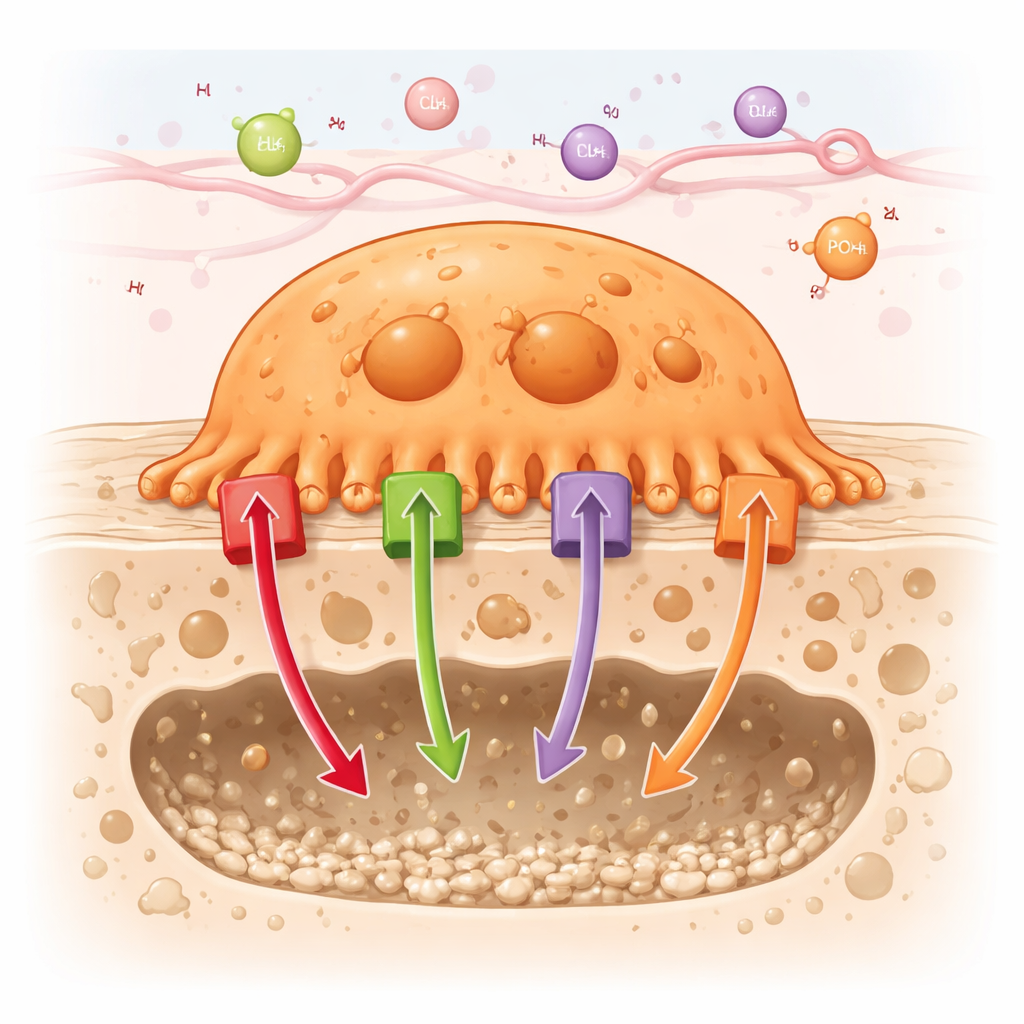
骨食细胞如何完成它们的工作
破骨细胞通过紧密附着在骨表面并形成一个密封的腔室来工作,在那里它们可以安全地溶解矿物并消化蛋白质。为了使这个微型“消化室”变得极其酸性,破骨细胞将大量质子(氢离子)泵入该腔。同时,它们将其他离子——如氯、钙和磷酸盐——在细胞膜和内部隔室之间转运。文章综述了约90种在破骨细胞中发现的不同通道和转运蛋白,并将它们分为六类,包括能量驱动的泵(ATP酶)、阳离子和阴离子通道、耦合转运体、营养载体以及ATP结合盒(ABC)转运蛋白。
酸、盐与能量:核心机械
有两种蛋白系统在骨吸收中尤为关键。首先,称为V-ATPase的液泡质子泵主动将质子推入吸收间隙,使其酸性足以溶解骨矿并激活蛋白酶。特定的V‑ATPase亚基,如a3、d2和若干V1组分,在破骨细胞的皱褶边缘和溶酶体中富集,这些亚基的基因缺陷可导致骨质脆弱或异常增厚。其次,一种称为ClC‑7的氯–质子交换体与名为OSTM1的蛋白配对,将氯离子带入同一区域。这有助于平衡电荷并允许持续的质子泵送。当ClC‑7发生突变时,人类和小鼠会出现成骨不全(骨质致密但脆弱)的症状,说明正常的离子流对骨骼健康至关重要。
钙、磷和其它支持性角色
除了酸的产生,破骨细胞还依赖精细调控的钙和磷处理。分布在细胞膜、内质网、溶酶体和线粒体的一系列钙通道和泵产生节律性的钙“振荡”,从而开启破骨细胞分化和融合的关键基因。位于皱褶边缘和细胞对侧的转运体将溶解的钙和磷转出,要么在细胞内回收,要么再输回血液。其它金属和矿物质——如锰、镁、锌、铜和铁——也由专门的转运蛋白控制,进而影响破骨细胞的吸骨活性。例如,铁以及与铁相关的某些细胞死亡形式可以增强或抑制破骨细胞活性,而锌转运蛋白则倾向于抑制过度的骨丢失。
细胞内的交通管控
离子通道并不局限于外膜。许多通道位于溶酶体、内体、高尔基体和线粒体等内部隔室,形成分层的转运网络。这些内部“门”有助于设定消化囊泡的pH、线粒体的能量产生,以及酶和碎屑的输送。综述强调了多种通道系统如何协同工作:钠–氢交换体调节内部酸度,钾–氯共转运体有助于维持膜电位和氯平衡,嘌呤能受体和机械敏感通道将化学或机械信号转化为骨吸收的变化。葡萄糖、氨基酸、核苷和维生素C的营养转运体进一步支持处于高能耗和高生物合成需求的活跃吸收破骨细胞。
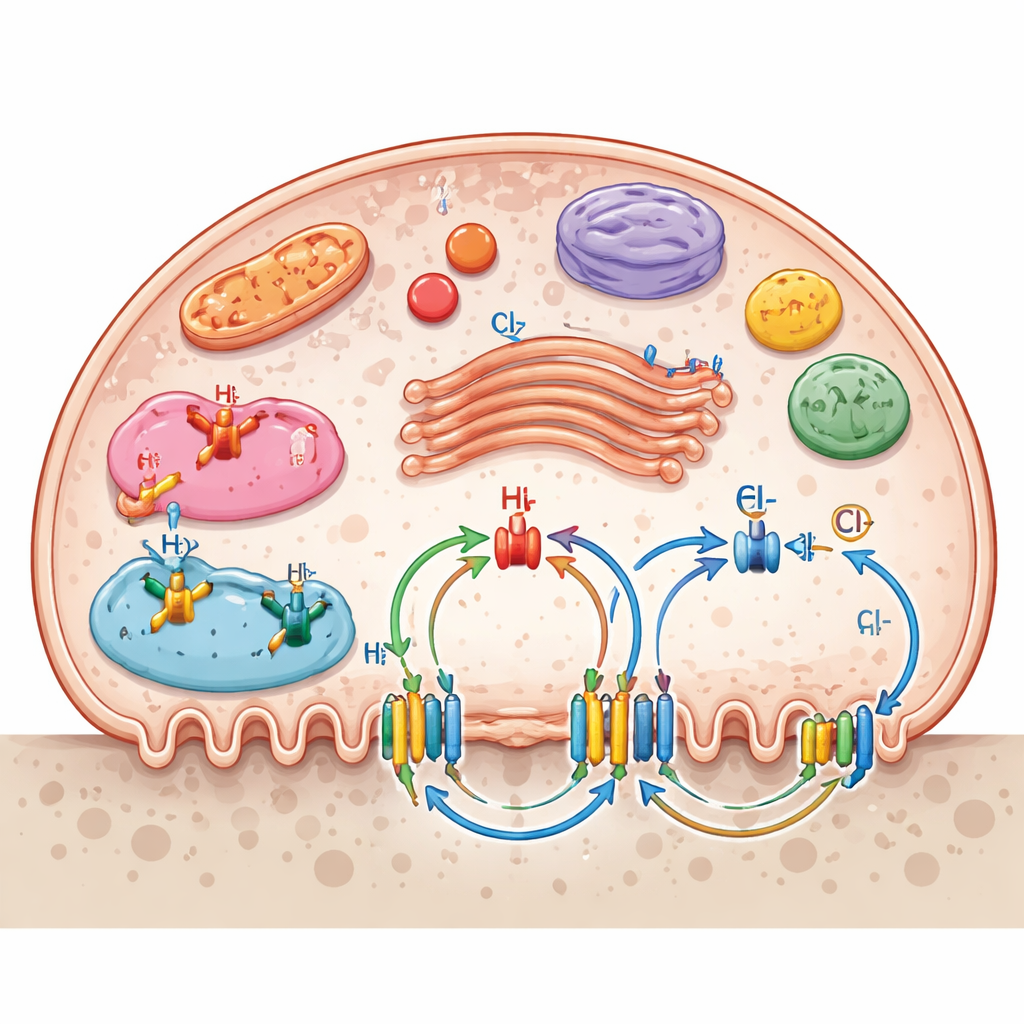
从基础生物学到新疗法
由于许多骨病源于破骨细胞过度或不足的活性,指导其行为的通道和转运蛋白成为有吸引力的药物靶点。作者回顾了现有和试验性化合物,这些化合物可以阻断V‑ATPase、TRP钙通道、氯交换体、嘌呤能受体及其他转运体,以及一些新思路,例如破坏特定亚基相互作用或使用定向纳米颗粒将药物直接递送到骨组织。他们强调,许多这些蛋白也存在于其他组织中,因此实现真正的破骨细胞特异性仍然是一个挑战。不过,随着基因组学和成像工具揭示这些通道的位置及其相互作用,不断扩展的破骨细胞“离子地图”有望为骨质疏松、炎性骨丢失和罕见遗传性骨病带来更精确的治疗方法。
引用: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
关键词: 破骨细胞, 离子通道, 骨吸收, V-ATPase, 骨质疏松