Clear Sky Science · zh
C/EBPβ 决定绝经后 FSHβ 的转录,阻断 AEP/C/EBPβ 通路可缓解骨质疏松
这项研究为何与绝经后生活相关
许多女性被告知,雌激素下降是绝经后骨骼脆弱的主要元凶。这项研究为这一难题补上了新的一块:另一种激素——促卵泡刺激素(FSH),以及在脑和骨骼中配合工作的蛋白对 C/EBPβ 与 AEP,共同加速骨质流失。更有趣的是,研究者在小鼠中展示,使用一种实验性口服药物阻断该通路能够像获批的骨质疏松药物一样有效地保护骨骼。
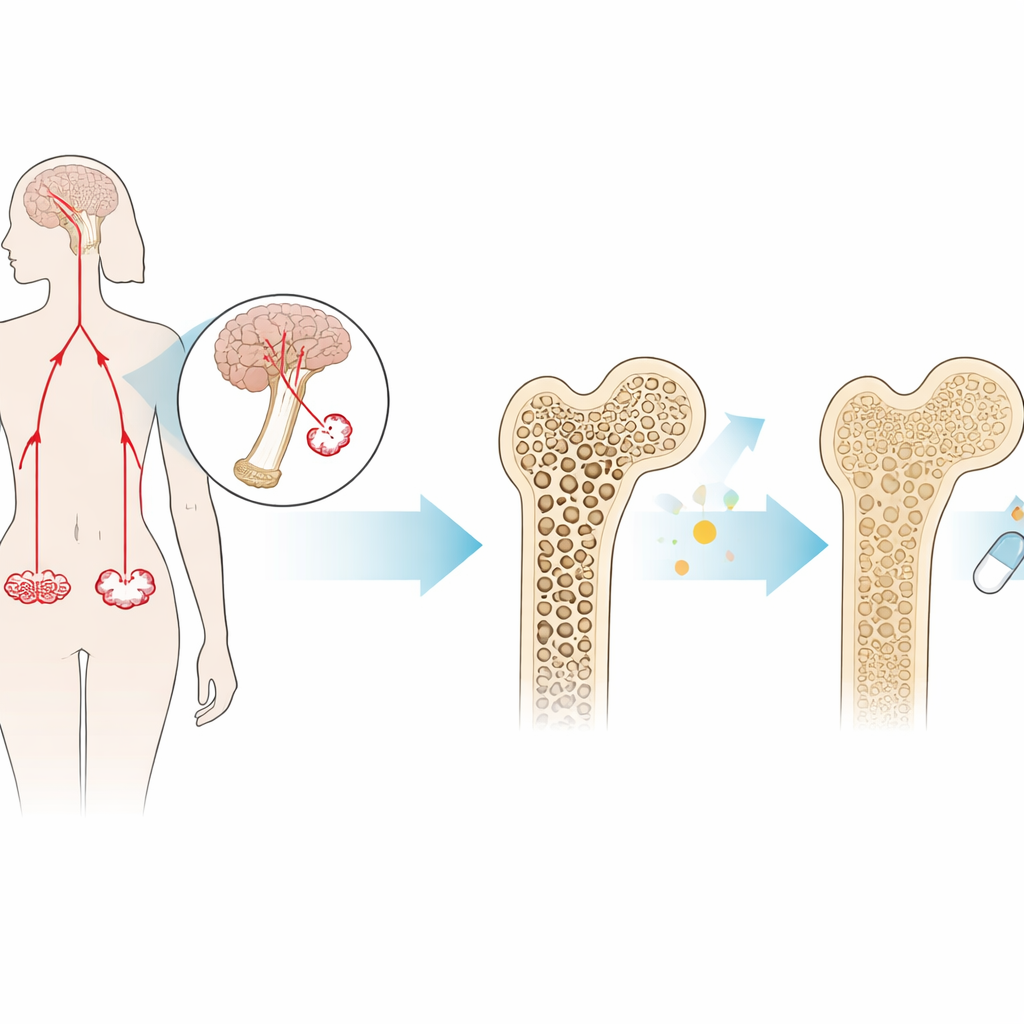
一种鲜为人知但对骨骼影响巨大的激素
FSH 在脑下垂体产生,最为人熟知的是其在生育中的作用。在接近绝经的女性中,FSH 水平会在最后一次月经前几年显著上升。除了生殖功能之外,FSH 还能直接作用于骨骼:它结合于破骨细胞(骨吸收细胞)表面的受体,推动这些细胞比骨形成更快地消耗骨质。以往研究显示,缺乏 FSH 或其受体的小鼠即便雌激素低下也能免于骨质流失。这提示 FSH 本身,而不仅仅是雌激素缺乏,能够驱动绝经后骨质疏松。
位于垂体的控制开关
这项新研究聚焦于 C/EBPβ,一种结合 DNA 并打开或关闭基因表达的蛋白。作者发现 C/EBPβ 直接结合到促卵泡刺激素β 亚基基因的调控区——决定该激素特性的一部分——并在垂体中增强其产量。在培养的垂体细胞中,上调 C/EBPβ 会增加 FSH,而沉默 C/EBPβ 则会减少 FSH,尤其是在细胞受到来自大脑生殖信号 GnRH 刺激时。在切除卵巢以模拟绝经状态的小鼠中,C/EBPβ 降低的动物在垂体和血液中的 FSH 显著减少。这些实验证明 C/EBPβ 是决定雌激素下降后 FSH 激增程度的关键开关。
自我强化的环路与新的药物靶点
C/EBPβ 还控制另一种称作 AEP 的蛋白,AEP 是一种切割酶,可激活或失活其他分子。在脑中,C/EBPβ–AEP 链条曾与类阿尔茨海默病的损伤有关。研究团队在此探究这条链是否会反馈影响 FSH 与骨。在缺失 AEP 的小鼠中,垂体中 C/EBPβ 与 FSH 水平均降低,切除卵巢后的骨质流失也减少。用一种名为 #11a 的小分子药物阻断 AEP 得到类似效果:经过数月治疗,切除卵巢的小鼠 FSH 降低,高分辨率扫描显示骨骼更强壮,过度活跃的破骨细胞也减少。另一类化合物——可间接抑制 AEP 的 TrkB 激活剂,在体外对骨细胞有益,但在动物体内无法降低 FSH,主要因为其靶受体在垂体中稀少。这一对比强化了结论:直接抑制 AEP 是从源头关闭 C/EBPβ–FSH 轴更有力的途径。
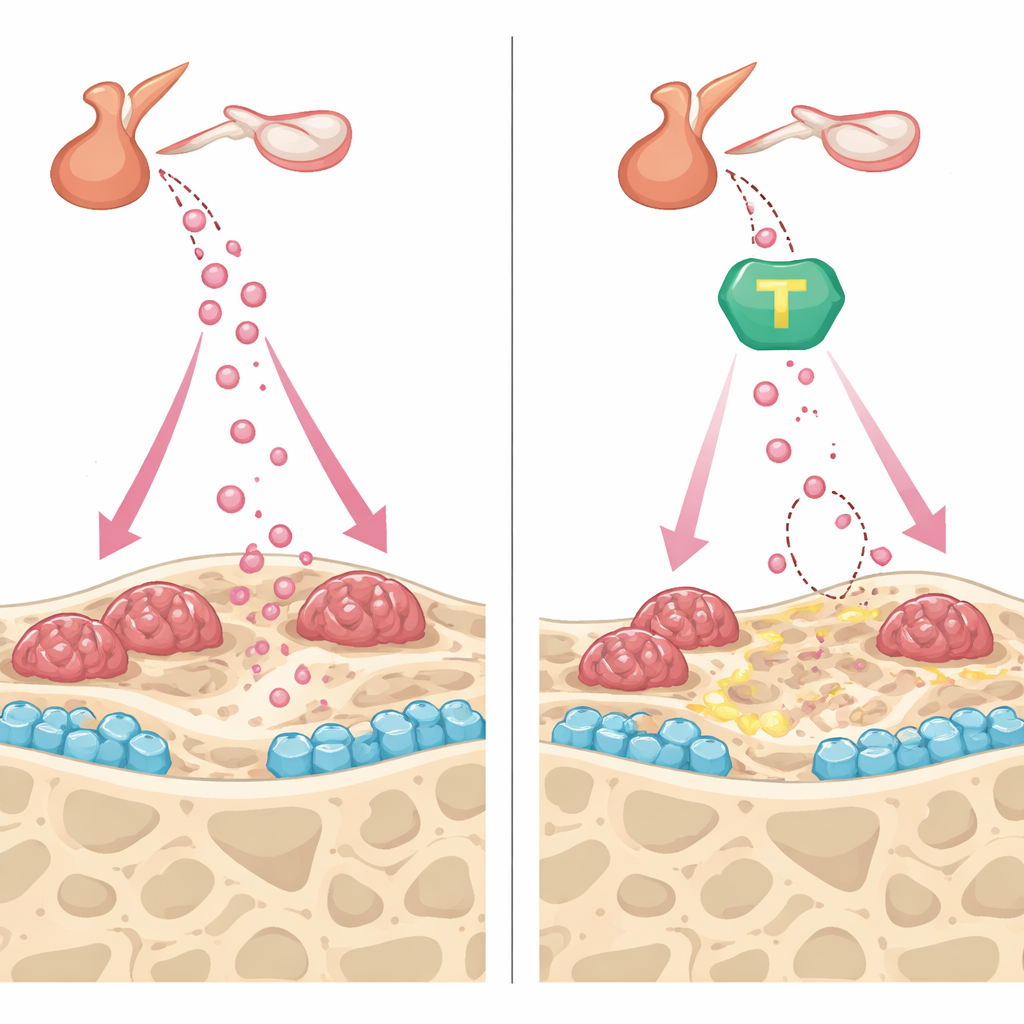
从两个角度保护骨骼
除了降低 FSH 外,#11a 与 TrkB 激活剂 CF3CN 在骨组织内也展现互补的益处。在骨形成细胞的培养中,这两种化合物都加速了细胞成熟和矿化沉积,部分机制是保留了纤连蛋白(一种 AEP 常常切割的结构蛋白),并增强了如骨保护素等促骨信号。在破骨细胞中,这些药物削弱了关键的骨吸收信号,减少了大型多核细胞的数量及其在骨片上刻蚀凹坑的能力。在活体小鼠中,#11a 与 CF3CN 均抑制了卵巢切除诱导的快速骨转换,稳定了骨密度与微结构。令人瞩目的是,在与 FDA 批准的注射用增骨药物特立帕肽的直接比较中,这种实验性口服药在恢复骨量和强度方面与特立帕肽不相上下。
这对未来骨质疏松护理意味着什么
对非专业读者而言,结论是:该研究识别出一条双重作用的通路,将与绝经相关的炎症、FSH 上升和骨损伤联系起来,并表明针对 AEP 可以中断这条链。在小鼠中,口服 AEP 抑制剂不仅降低了助长骨质流失的过量 FSH,还直接将骨内平衡向构建而非破坏转变。尽管这些发现仍需在人类中验证,但它们提示未来的骨质疏松治疗可能不再仅限于替代雌激素或刺激成骨,而是通过静默这一新绘制的激素与酶学回路来防治绝经后骨脆弱性。
引用: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
关键词: 绝经后骨质疏松, 促卵泡刺激素, C/EBPβ AEP 通路, 骨重塑, 激素靶向治疗