Clear Sky Science · zh
肥胖小鼠骨髓脂肪细胞扩增导致由PD-L1介导的骨髓免疫抑制和破骨细胞生成
为什么骨内脂肪很重要
大多数人把脂肪想象为皮下或腹部周围的组织,但我们的骨骼内部也含有专门的脂肪组织。本项小鼠研究表明,当骨髓脂肪在肥胖时扩增,会悄然重塑骨内的免疫环境并加速骨组织的分解。理解体重、免疫和骨强度间这一隐秘联系,有助于解释肥胖人群为何更易发生骨折,并可能指向通过靶向骨髓内脂肪和免疫通路来保护骨骼的新治疗策略。
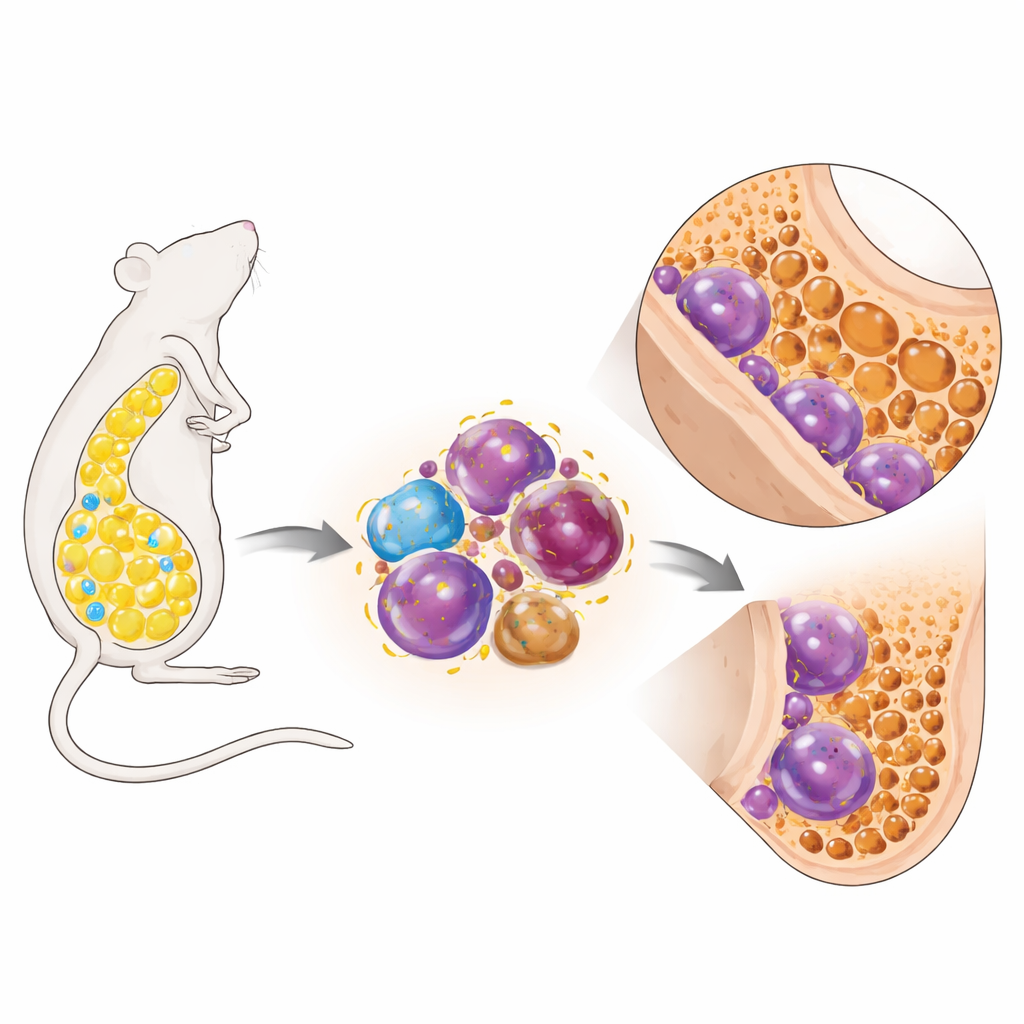
肥胖与骨骼变弱
曾有人认为肥胖会保护骨骼,因为更重的身体对骨骼施加更大负荷。然而,最新数据表明,肥胖人群常有较差的骨质量和更多骨折。在这项研究中,研究者用高脂饮食喂养小鼠,并根据体重和脂肪量的大幅增加严格划分哪些动物真正变得肥胖。这些肥胖小鼠大量丢失了松质骨(即骨的海绵状内层),雄性小鼠还出现致密皮质骨的变薄。骨质流失与破骨细胞数量和体积的增加以及成骨细胞功能下降相关——表明骨重建中分解与形成的平衡向有害方向偏移。
骨髓脂肪不仅仅是填充物
观察骨髓内部时,研究组发现肥胖小鼠的骨髓脂肪细胞显著扩增——数量增多且体积更大。在同样饮食但未变得肥胖的小鼠中,骨髓脂肪显著较少且骨容积更好,这提示骨髓脂肪本身可能在促成损害。将来自肥胖小鼠的骨髓脂肪细胞与可分化为破骨细胞的幼稚髓系细胞共培养时,脂肪细胞显著增强了成熟破骨细胞的数量与体积。出人意料的是,骨髓脂肪并未表现出明显的炎性表型;相反,这些脂肪细胞大量产生一种叫MCP‑1的信号分子,已知可吸引并扩增特定髓系细胞并促进其向破骨细胞分化。
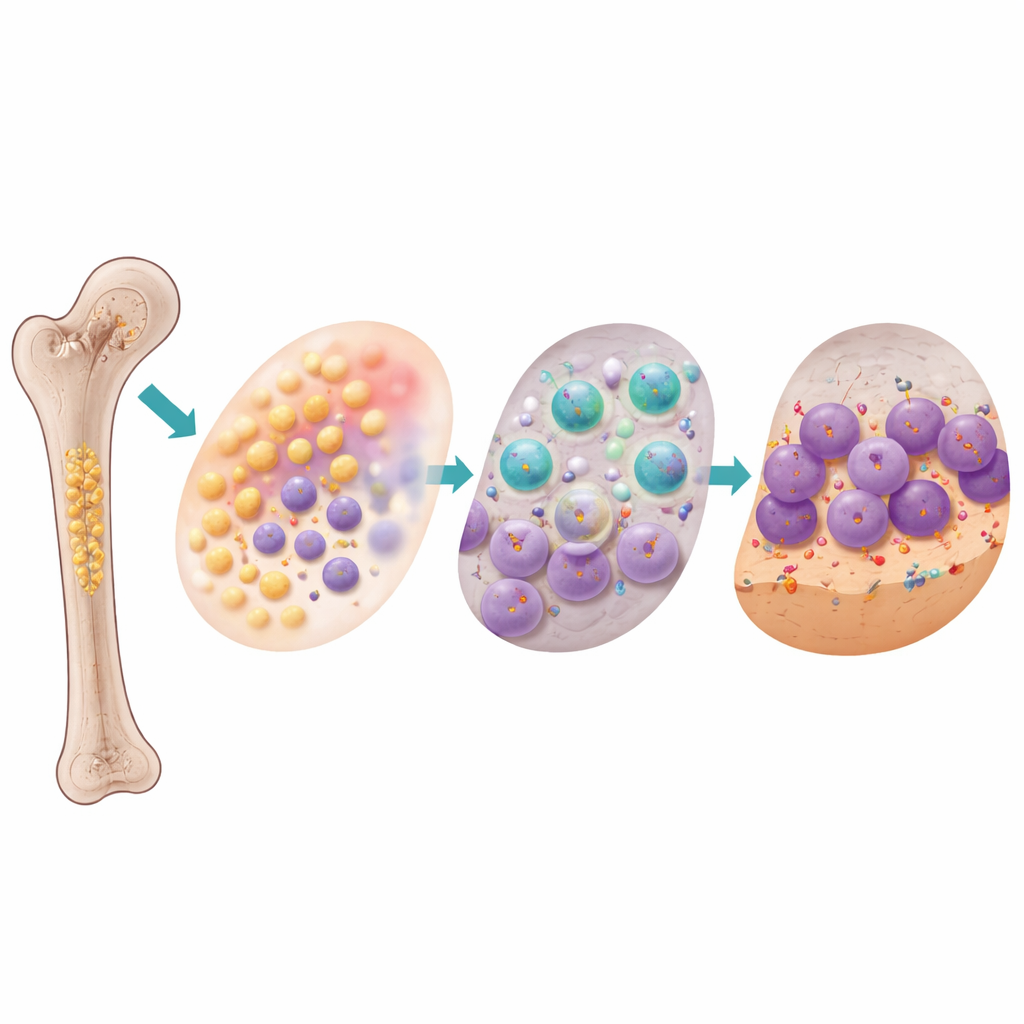
一种静默的免疫刹车却助长骨质流失
骨髓也是一个免疫器官,肥胖显著改变了其免疫构成。肥胖小鼠产生了更多的髓系祖细胞和更多在表面携带免疫“刹车”蛋白PD‑L1的成熟髓系细胞。与此同时,辅助性T细胞数量减少,暴露于这些富含PD‑L1的髓系细胞的T细胞停止分裂,显示出骨髓环境已转为免疫抑制。关键的是,研究者还发现一群携带PD‑1的破骨细胞前体细胞——PD‑1是PD‑L1的结合伙伴。当PD‑1与PD‑L1在破骨细胞发育早期相互作用时,它们并非起到刹车作用,而像踩下了油门:在细胞培养中阻断此相互作用(尤其是在分化的最初几天)会明显减少破骨细胞的数量、体积、融合以及参与骨吸收的基因表达。
抑制骨髓脂肪以保护骨骼
为验证骨髓脂肪是否真正位于这些免疫改变的上游,团队使用了基因改造小鼠,这些小鼠无法形成正常的充满脂质的骨髓脂肪细胞,但在高脂饮食下仍会肥胖。缺乏骨髓脂肪的肥胖小鼠体内PD‑L1阳性髓系细胞更少,携带PD‑1的破骨细胞前体更少,血液中的骨吸收标志物也较低。它们的松质骨体积明显高于具有完整骨髓脂肪的肥胖对照组,内骨结构更趋于板状、支撑性更强而非纤细成棒。成骨细胞并未被增强,但破骨细胞显著减少,表明简单地阻止骨髓脂肪扩增就能通过缓和骨髓免疫环境中促进破骨细胞的压力来减轻与肥胖相关的骨质流失。
这对骨骼健康意味着什么
总体而言,本研究表明在肥胖状态下,扩增的骨髓脂肪细胞有助于将骨髓转变为一个免疫抑制的小环境,充斥着表达PD‑L1的髓系细胞。这些细胞不仅抑制T细胞活性,还与破骨细胞前体上的PD‑1相互作用,推动它们更强烈地分化为骨吸收性破骨细胞。由此产生的破骨细胞过度活跃会侵蚀松质骨并削弱皮质骨,增加骨折风险。通过阻断骨髓脂肪形成或在破骨细胞发育的关键阶段干预PD‑1/PD‑L1信号通路,可能有助于在肥胖以及骨质疏松和某些伴随骨髓脂肪增加的癌症等疾病中保护骨骼。
引用: Costa, S.N., Chlebek, C., Gray, L. et al. Expansion of bone marrow adipocytes in obese mice leads to PD-L1-driven bone marrow immunosuppression and osteoclastogenesis. Bone Res 14, 32 (2026). https://doi.org/10.1038/s41413-026-00509-5
关键词: 骨髓脂肪, 肥胖与骨质流失, 免疫检查点, 破骨细胞, 骨骼健康