Clear Sky Science · zh
HIF-1α 与 BMAL1 在骨再生中的作用:低氧响应与昼夜节律的相互对话
为何骨折比你想象的更能愈合
当我们折断一块骨头或拔掉一颗牙时,体内会悄然启动一项高度协调的修复工程。在受伤部位深处,氧气水平下降,而我们的内在昼夜生物钟仍在持续运行。本文探讨了两大主控开关——感知低氧的 HIF‑1α 与核心时钟蛋白 BMAL1——如何协同工作,引导骨细胞经历炎症、新组织生长到最终强度恢复。理解这一合作关系有望改进骨折、骨质疏松、关节炎乃至牙科种植的治疗策略。
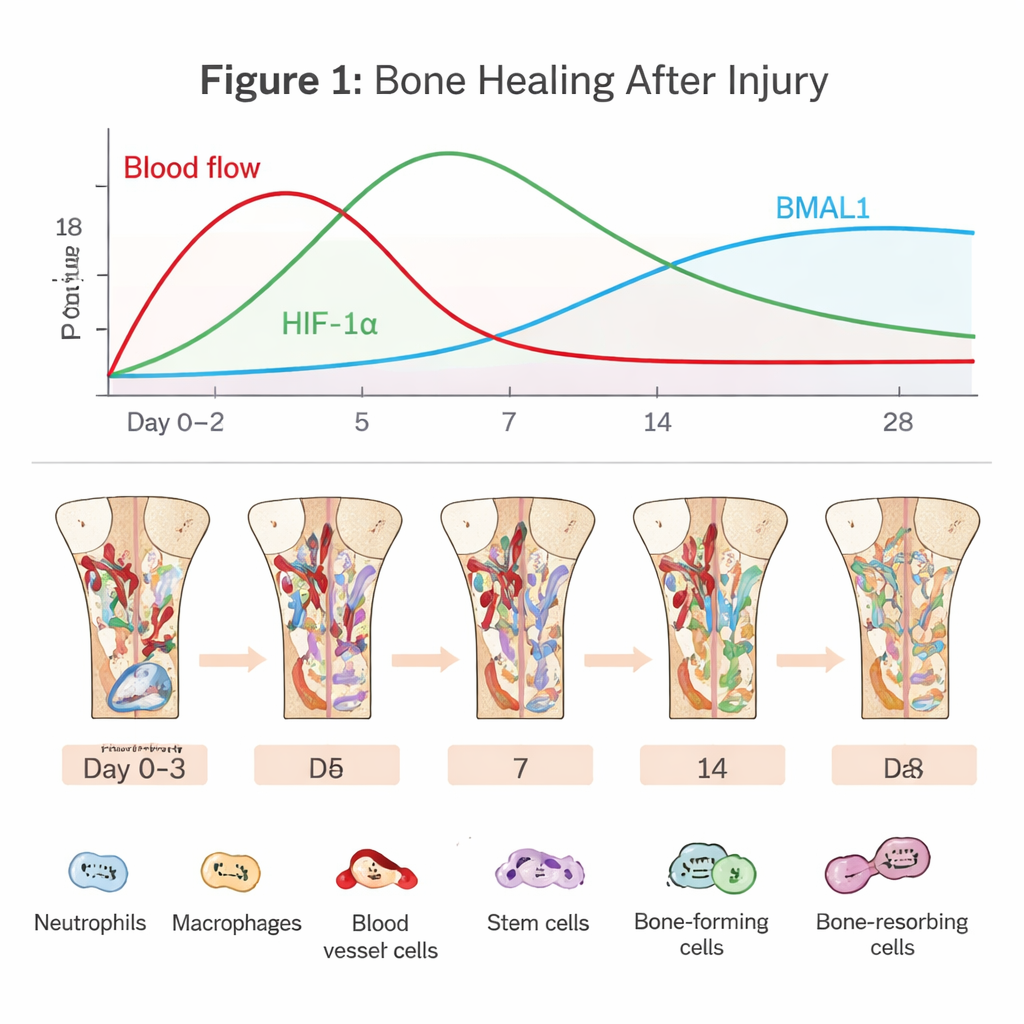
愈合骨骼内部的隐秘戏剧
骨再生从血管断裂的那一刻起便开始。血块形成,阻断了大部分氧气供应,造成一个严酷的低氧小环境。中性粒细胞和巨噬细胞等免疫细胞迅速涌入,清理碎片并抵御微生物。与此同时,骨髓干细胞和血管细胞被招募来重建受损区域。早期的“炎症期”是一把双刃剑:短暂且时机恰当的炎症可以启动修复,但若持续过久或过度激烈,愈合可能停滞或失败。文章强调,要在这条狭窄路径上稳妥前行,很大程度上取决于细胞如何感知氧气与时间。
细胞如何利用低氧为己所用
在缺氧的骨折区,HIF‑1α 蛋白稳定并启动帮助细胞适应的基因程序。它促使内皮细胞萌发新血管,确保新鲜的氧气和营养到达缺损处;同时将细胞代谢重编程为糖酵解,一种在氧气稀缺时仍能产生能量的方式。对干细胞和成骨细胞而言,适度激活 HIF‑1α 可促进增殖、迁移与成骨,部分通过提高 VEGF 等因子将血管形成与新骨连接起来。但若缺氧过于严重或持续时间过长,应激分子与活性氧会积累,促使成骨细胞走向凋亡并刺激破骨细胞活性。因此,同一低氧信号可根据其强度与持续性,要么支持愈合,要么破坏愈合。
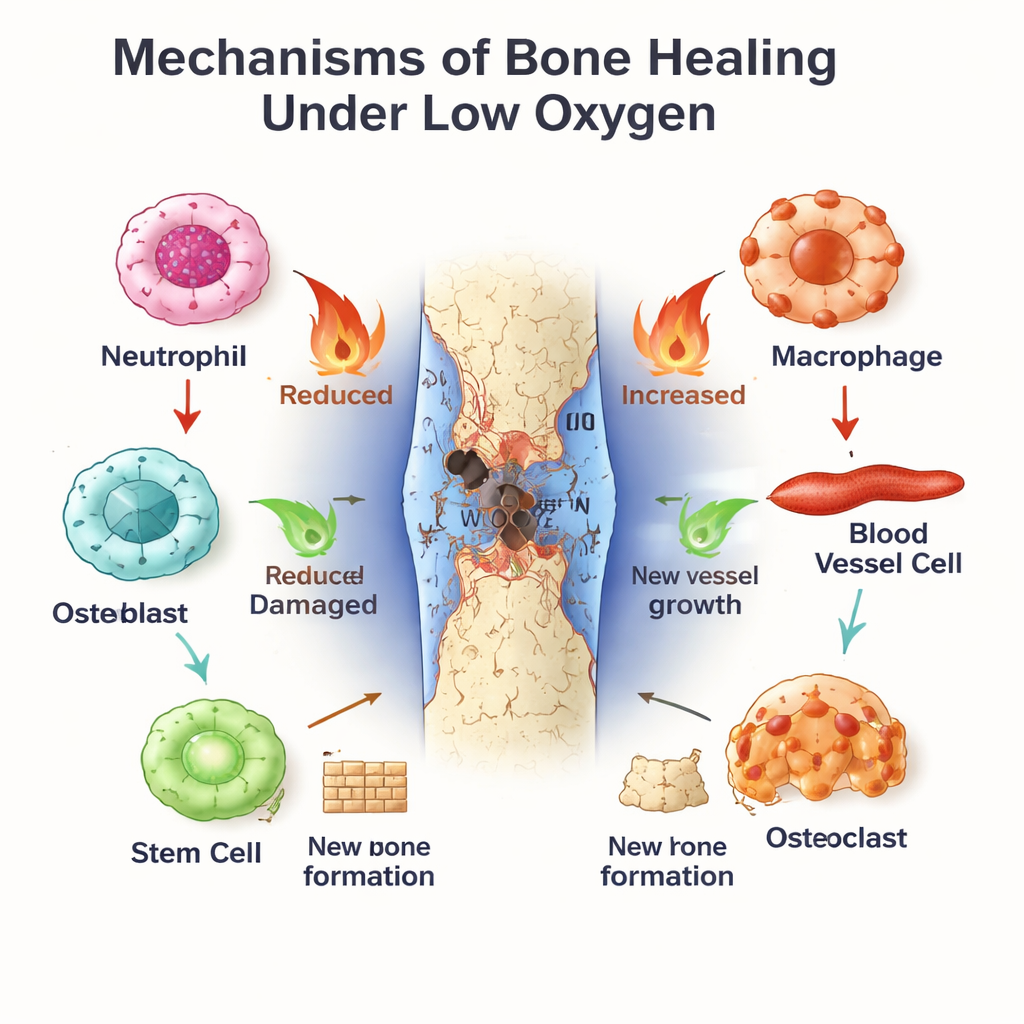
体内时钟作为骨修复的管理者
与此并行的是昼夜节律——存在于几乎所有细胞的分子计时器。BMAL1 作为其核心成分之一,有助于设定免疫活动、血管行为和干细胞分化的日节律。中性粒细胞和巨噬细胞在响应损伤的强度以及衰老或从促炎(类似 M1)向愈合(类似 M2)状态转变的速度上,表现出昼夜差异。在血管细胞和骨髓干细胞中,BMAL1 通过调节 Wnt 与 TGF‑β/SMAD 等生长通路,促进健康的增殖和有序的成骨。当 BMAL1 受损——无论是基因缺陷、夜班工作还是代谢疾病所致——骨密度往往下降,干细胞功能衰竭,成骨与骨吸收之间的平衡向丧失倾斜。
氧感应与体内时钟之间的对话
综述的核心是 HIF‑1α 与 BMAL1 之间新兴的“串话”概念。这两种蛋白具有相似结构,能够发生物理相互作用,甚至形成混合二聚体,结合 DNA 并共同调控部分重叠的基因组。它们彼此影响对方的产生与稳定性,形成将昼夜节律与细胞对缺氧反应相连的反馈回路。二者还共同调控细胞氧化还原平衡——即有害活性氧的产生与抗氧化能力之间的权衡——并协同调节决定细胞依赖氧气呼吸还是无氧糖酵解的关键酶。这样的共同控制有助于决定骨折微环境是偏向建设性的重建,还是走向过度炎症和骨质流失。
这对疾病与治疗有何意义
相同的 HIF‑1α–BMAL1 合作关系在许多与骨相关的情况中都可见端倪。在夜班工作者中,睡眠紊乱与光照干扰可能改变 BMAL1,增加氧化应激,并干扰 HIF‑1α 指导的修复,进而促成骨质疏松。在糖尿病中,高血糖削弱了时钟功能与缺氧信号,损害血管生长与干细胞驱动的成骨。在骨关节炎中,软骨细胞中 BMAL1 的丧失扰乱了它们的节律以及与 HIF‑1α 的保护性联系,加速软骨破坏。在钛植入体周围,受控的低氧与健康的昼夜节律似乎有利于更好的骨整合,这提示未来的植入物涂层或许可以设计为温和激活 HIF‑1α 与 BMAL1。总体而言,文章总结道,成功的骨再生不仅取决于存在哪些细胞,还在于它们如何解读氧气与时间——针对这种对话进行干预可能为更快、更强的愈合开辟新路径。
引用: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
关键词: 骨再生, 昼夜节律, 缺氧, 骨质疏松, 骨折愈合