Clear Sky Science · zh
用于骨骼衰老修复与再生的智能生物材料
在老龄化世界中更强壮的骨骼
许多人认为骨骼变弱和关节疼痛是衰老不可避免的部分。但科学家们正在设计“智能”材料,能够感知骨骼何时何地出现问题并帮助其自我修复。这些材料旨在更可靠地修复骨折、减缓或逆转骨质疏松和骨关节炎,并减少反复手术的需要——为老年人维持活动能力和独立生活提供更大可能。
骨骼如何衰老以及为何更易骨折
骨骼是不断重建的活组织,但随着年龄增长这种平衡会失衡。骨髓内的干细胞从生成成骨细胞转向产生更多脂肪细胞;成骨细胞疲惫而破骨细胞过度活跃。胶原与矿物构成的支持基质变得更干燥、更脆弱,微观“支架”也变薄。激素变化、慢性低度炎症、过量活性氧分子以及局部酸性环境都增加应激。从外观上看,这表现为骨质变薄、更具孔隙性、关节僵硬、脊柱弯曲,以及骨折和骨质疏松、骨关节炎等疾病风险上升。
为何现有治疗仍不充分
当前的主要治疗包括减缓骨丢失或刺激成骨的药物,外加手术和金属或陶瓷植入物以稳定骨折或置换受损关节。这些方法挽救了许多生命,但也有重要缺点。系统性药物通常到达骨组织的比例极小,并可能产生副作用,如颌骨问题、血栓,甚至长期使用增加癌症风险。干细胞疗法在动物实验中显示出潜力,但面临细胞存活率低、行为不可预测和潜在肿瘤形成等问题。传统植入物提供强度,但属于“无感知”的物体:它们无法感知周围环境,不能调节药物释放,并可能在脆弱的老年骨组织中失效。
巡逻全身的智能药物载体
智能生物材料将“智能”引入治疗体系。其中一大策略是使用纳米颗粒或软凝胶进行系统性“智能递送”,这些载体在血液中循环,仅在病变部位激活。这些载体可以设计成对内部信号做出响应,比如酸性环境、过量的氧化性分子或溶骨酶;也可以对外部刺激响应,如光、超声、热或磁场。例如,有些颗粒在正常组织中保持完整,但在酸性、富含酶的微环境中打开并释放药物,恰好针对过度活跃的破骨细胞所在的部位。另一些载体一边清除过量活性氧,一边缓慢释放抗炎药,或携带造影染料以便医生实时观察分布。通过叠加多重触发条件——例如同时对pH和氧化物敏感——研究人员可以提高靶向精度并减少副作用。
像临时智能骨一样的局部支架
当老化骨骼出现大缺损或复杂骨折时,可以将局部“智能支架”直接植入缺损处。这些由金属、陶瓷、高分子或其组合制成的三维结构,经过工程设计以匹配骨骼的强度、孔隙率和柔韧性。其海绵状结构允许血管和新骨生长,材料也会逐步溶解并被患者自身组织替代。 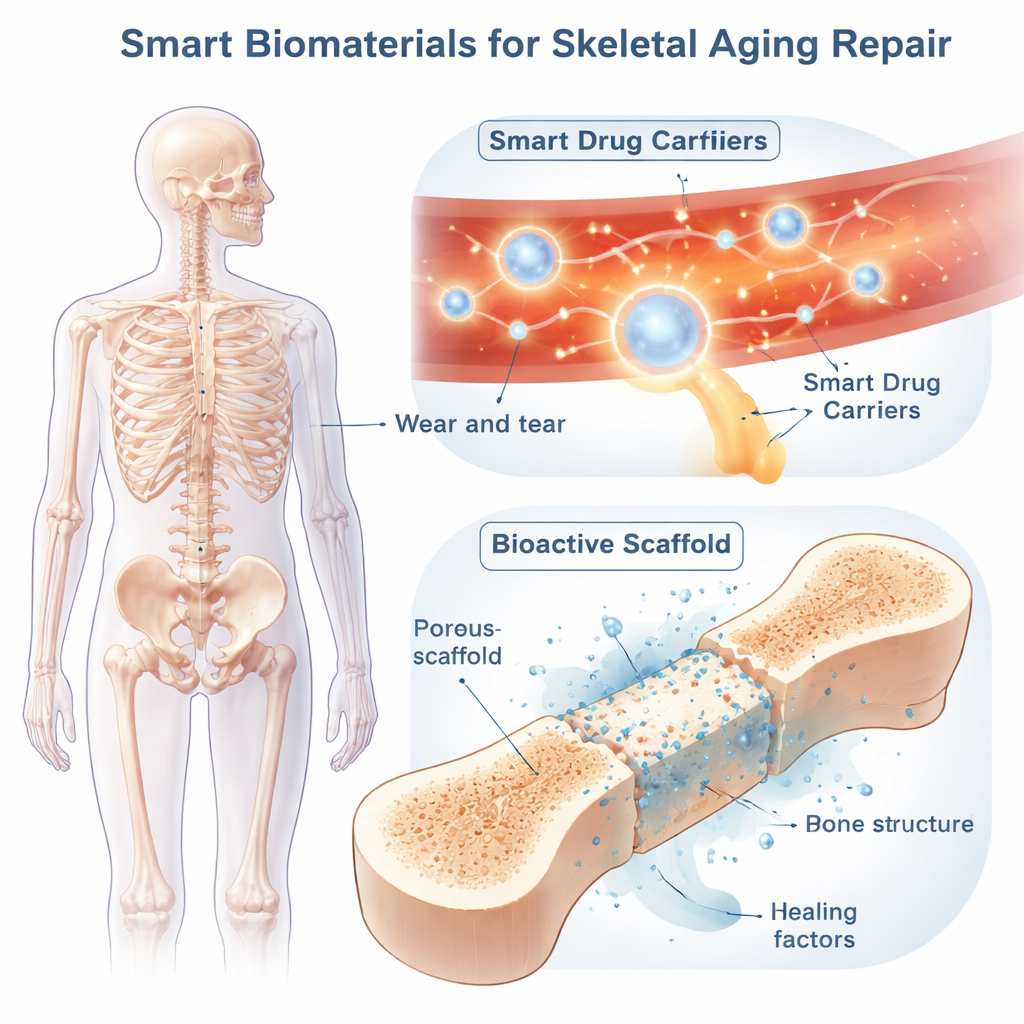
从实验室到临床:工具、障碍与未来方向
为制造这些复杂系统,科学家们使用先进制造技术,如3D打印和增材制造,以高精度调控孔径、刚度和药物载量。然而,要将智能生物材料转化为常规治疗仍面临挑战。大多数注射颗粒仍然在肝脏和脾脏等器官中积累,而非骨组织,且许多动物模型无法捕捉人类衰老的复杂性。大规模生产、质量控制、监管审批和成本仍是主要难题。研究者对将智能材料与人工智能结合以个性化支架设计和用药剂量抱有希望,并在于内置传感器以跟踪愈合并在“闭环”方式下自动调整治疗方面看到潜力。 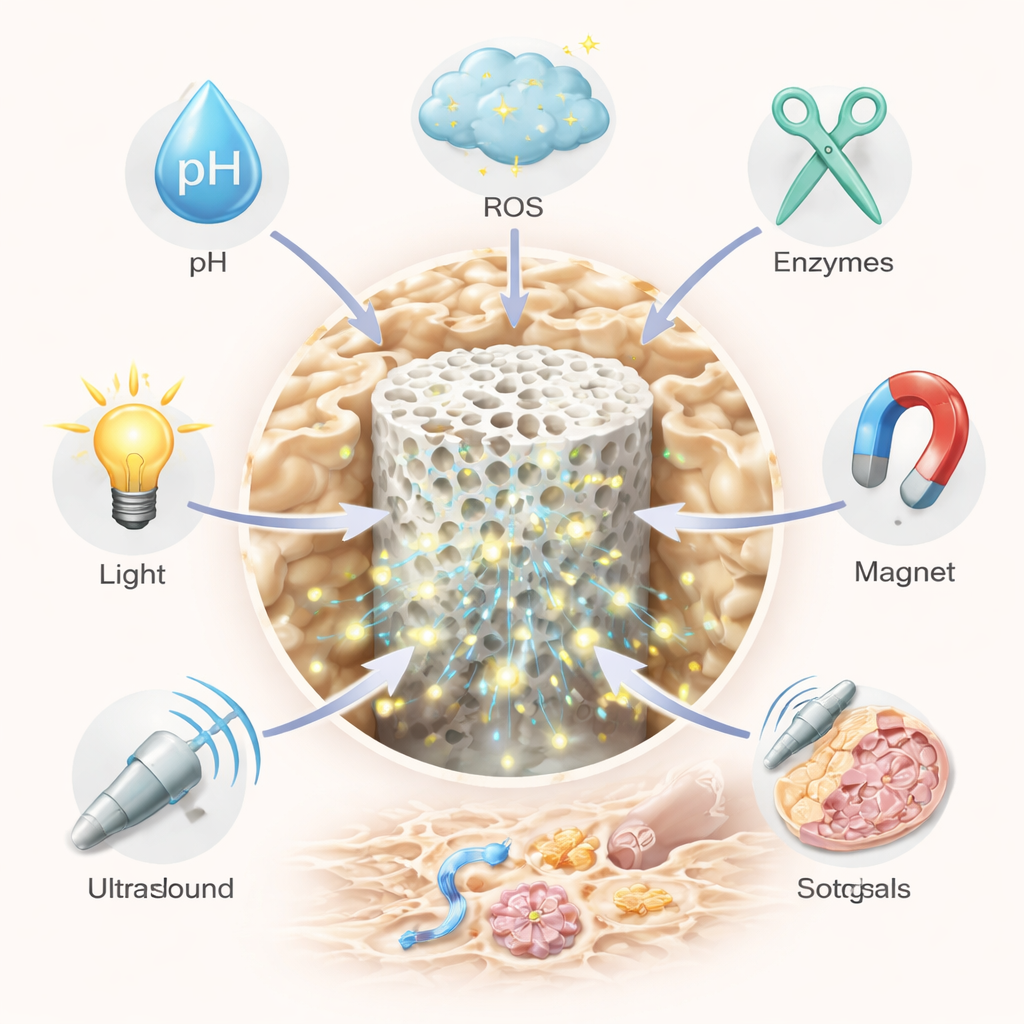
这对患者意味什么
本质上,这项工作表明老年骨脆弱并非单向不可逆的衰退,而是一个可能被工程手段解决的复杂问题。智能生物材料像微小且可编程的修复小队:在血液中巡逻、定居到受损部位,并在恰当的时间释放恰当的物质,以恢复骨组织的结构和功能。尽管这些技术大多仍处于研究阶段,但它们指向一个未来:骨折愈合更快、植入物寿命更长、治疗根据每个人独特的骨生物学定制——帮助更多人在高龄仍保持活动能力和独立性。
引用: Liang, D., Wang, H., Jiang, Y. et al. Smart biomaterials for skeletal aging repair and regeneration. Bone Res 14, 24 (2026). https://doi.org/10.1038/s41413-026-00505-9
关键词: 智能生物材料, 骨骼衰老, 骨再生, 骨质疏松, 刺激响应支架